Принцип работы аккумулятора
Для обеспечения электрическим током схем мобильных устройств и машин, применяются специальные изделия, способные аккумулировать энергию. Для того чтобы правильно эксплуатировать такие устройства, желательно ознакомиться с принципом работы батарей.
История развития АКБ
Первые электрические батарейки на основе солевого электролита были известны ещё в Древнем Багдаде, но новый толчок к развитию этой технологии был получен в начале XIX века.
Итальянский учёный Алессандро Вольта более 200 лет назад создал первый химический источник электрического тока.
Батарейку такой конструкции нельзя было перезарядить, но начиная с этого момента был заложен основательный фундамент изготовления портативных АКБ. Спустя некоторое время, изобретение Вольта были усовершенствованы Иоганном Вильгельмом Риттером, который собрал из медных пластин аккумулятор, который можно было использовать многократно.История развития автомобильного аккумулятора началась значительно позже, ведь во времена Алессандро Вольта самоходные повозки ещё не были изобретены. Даже после появления автомобилей, в которых воспламенение горючей смеси осуществлялось за счёт искровой свечи, большой необходимости в использовании аккумуляторных батарей не было, ведь генерация высокого напряжения осуществлялось с помощью механического магнето. В те времена пуск двигателя осуществлялся вручную, а мощность моторов была не настолько велика, чтобы сопротивление сжатия газа в цилиндрах существенно препятствовала проворачиванию коленвала с помощью специальной рукоятки.
Даже после появления автомобилей, в которых воспламенение горючей смеси осуществлялось за счёт искровой свечи, большой необходимости в использовании аккумуляторных батарей не было, ведь генерация высокого напряжения осуществлялось с помощью механического магнето. В те времена пуск двигателя осуществлялся вручную, а мощность моторов была не настолько велика, чтобы сопротивление сжатия газа в цилиндрах существенно препятствовала проворачиванию коленвала с помощью специальной рукоятки.
После изобретения звукового сигнала, фар, стеклоочистителей возникла необходимость в источнике тока, который обеспечил бы автомобиль электричеством в необходимом объёме. Первое время машины не имели генератора, поэтому заряжать источники питания приходилось от сети, но уже в 20-е годы прошлого столетия машина стала оснащаться генератором электрического тока, что позволило осуществлять зарядку батарей во время работы двигателя внутреннего сгорания.
С момента первой установки на машину конструкция АКБ практически не изменялась, но существенной модернизации подверглись материалы, из которых изготавливались аккумуляторы. Пластины первых батарей делали из чистого свинца, который очень быстро покрывался оксидным слоем, что существенно снижало эффективность работы устройства. В дальнейшем, для уменьшения негативных последствий решётки обрабатывались суриком, но большую распространённость получила технология, при которой для производства пластин использовался сурьмяно-свинцовый сплав. В современных батареях проблема окисления решёток решается добавлением в свинец легирующих компонентов. Сплавы свинца и кальция позволяют снизить интенсивность испарения воды, поэтому корпус таких аккумуляторов изготавливается полностью герметичным.
Для чего нужна аккумуляторная батарея
Основное назначение автомобильного аккумулятора – обеспечение электрическим током стартер. Это электрическое устройство приводится в движение, только посредством постоянного тока высокой мощности.
- Осветительные приборы.
- Звуковой сигнал.
- Стеклоочистители.
- Сигнализацию.
- Дополнительное электрическое оборудование.
Наибольшая потребность в АКБ возникает во время стоянки, ведь в этот момент генератор не вырабатывает электрический ток, а вся нагрузка полностью ложится на плечи химического элемента питания. Также аккумулятор берёт на себя «обязанность» по обеспечению автомобиля электричеством в момент, когда обороты двигателя слишком малы, чтобы раскрутить якорь генератора до определённых значений.
Если автомобиль с двигателем внутреннего сгорания нуждается в АКБ только в момент запуска, а также при отключённом генераторе, то такая разновидность машин, как электромобили использует электродвижущую силу батареи в качестве основного энергоносителя.
Свинцовые батареи практически не способны эффективно справиться с этой задачей, поэтому для питания мощных электромоторов применяются литий -ионные или кадмиевые батареи.
Принцип работы аккумуляторной батареи
Чтобы понять принцип работы аккумулятора автомобиля необходимо ознакомиться с устройством батареи. Автомобильный аккумулятор состоит из следующих элементов:
- Корпуса.
- Крышки.
- Отрицательных и положительных пластин.
- Сепараторов.
- Клемм.
- Электролита.
Если аккумулятор является обслуживаемым, то в крышке имеется 6 резьбовых пробок, которые открывают доступ к каждой банке батареи. Корпус современных изделий изготавливается из сверхпрочного пластика, крышка также делается из пластмассы, которая надёжно соединяется с основной коробкой методом пайки. Кроме корпуса, из кислотоустойчивой пластмассы изготавливаются сепараторы, которые устанавливаются между пластинами.
Разобравшись, из чего состоит автомобильный аккумулятор можно приступать к изучению механизма накопления электрического тока. Работа АКБ зависит от возможности протекания химической реакции между свинцовыми пластинами и электролитом.
Работа АКБ зависит от возможности протекания химической реакции между свинцовыми пластинами и электролитом.
При подключении к АКБ потребителей электроэнергии происходит окисление свинца на положительной решётке, при этом на отрицательной пластине восстанавливается диоксид свинца.
Если аккумулятор заряжается от генератора или сетевого адаптера, то происходит обратный процесс. То есть, на отрицательных решётках уменьшается количество вещества, а на положительных – увеличивается.Если известно из чего состоит АКБ, а также изучен принцип работы аккумулятора, то не составит большого труда разобраться в особенностях современных разновидностей таких изделий.
Типы современных АКБ
Устройство современного аккумулятора автомобиля отличается от источников тока, изготавливаемых в прошлом столетии, прежде всего, по наличию необслуживаемого корпуса. Практически все АКБ, предназначенные для легкового автотранспорта, выпускаются без пробок в верхней крышке. К такому технологическому решению удалось прийти только после того, как было снижено газообразование внутри корпуса батареи. Таким неоспоримым достоинством обладают АКБ следующих типов:
Таким неоспоримым достоинством обладают АКБ следующих типов:
- Кальциевые (Ca/Ca).
- Гибридные.
- Гелевые.
- Литий-ионные.
- Щелочные.
Гибридные АКБ представляют собой средние по качеству батареи. Отрицательные пластины таких аккумуляторов также изготавливаются по кальциевой технологии, а положительные – из сурьмянистого сплава. Гибридные изделия существенно дешевле кальциевых АКБ, а зарядный ток на их контакты можно подавать с использованием даже старых моделей ЗУ.
Отрицательные пластины таких аккумуляторов также изготавливаются по кальциевой технологии, а положительные – из сурьмянистого сплава. Гибридные изделия существенно дешевле кальциевых АКБ, а зарядный ток на их контакты можно подавать с использованием даже старых моделей ЗУ.
В гелевой батареи аккумуляторный электролит представляет собой желеобразную массу.
Благодаря такой особенности батарея может прослужить более десяти лет, а при глубоком разряде рабочая поверхность пластин длительное время не будет покрываться оксидным слоем.
Несмотря на перечисленные преимущества, существенным недостатком таких изделий является высокая стоимость.AGM- аккумуляторы представляют собой устройство, которое очень напоминает гелевую конструкцию АКБ. В корпусе из пластика находятся свинцовые пластины, которые погружены в ватоподобную стекловолоконную массу, которая пропитывается электропроводящим составом. Благодаря использованию такой технологии удаётся также добиться низких показателей испарения жидкости, а также устойчивости к механическому воздействию.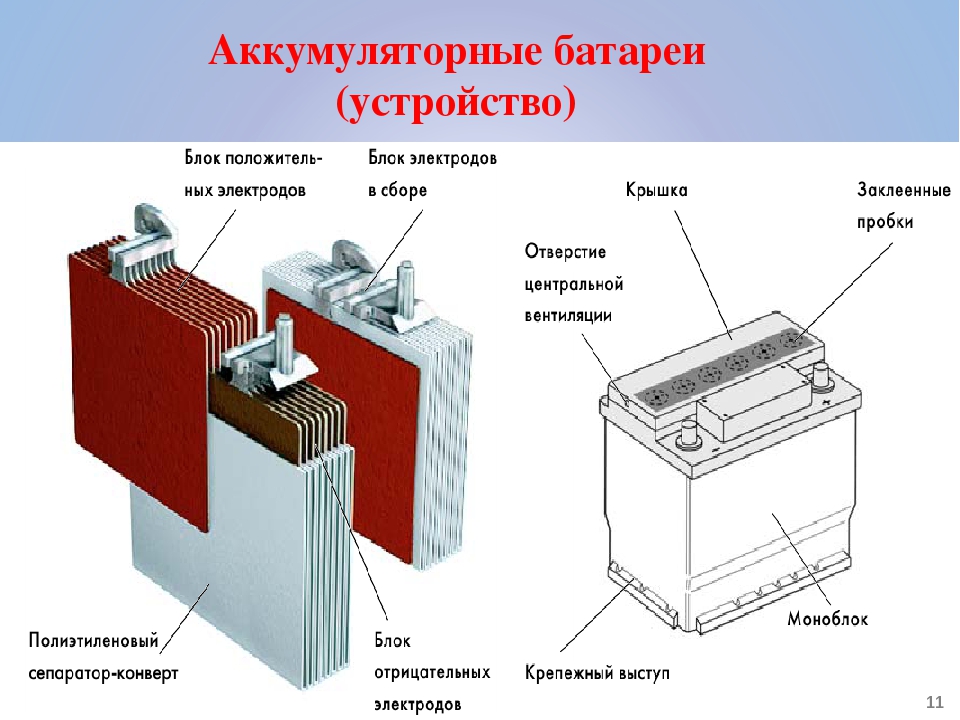
Литий-ионные аккумуляторы могут состоять только из ионов этого металла, поэтому при эксплуатации батарей значительно снижается вероятность их воспламенения даже под большой нагрузкой.
Благодаря этому преимуществу их можно использовать не только в качестве накопителя электроэнергии для машин с двигателем внутреннего сгорания, но и как основной источник энергии для электромобилей.
В современных щелочных аккумуляторах, также как и раньше, в качестве электролита используются едкий калий и едкий натрий. Достоинства таких батарей заключается в том, что в процессе эксплуатации не происходит снижения количества химических веществ внутри корпуса. Кроме этого, изделия имеют минимальный саморазряд и длительный срок эксплуатации. В различных самоходных установках такие модели АКБ применяются, в основном, в качестве тяговых аккумуляторов.
Принцип работы аккумулятора несложен, но разобраться в нём всё-таки стоит. Несмотря на то, что в необслуживаемую АКБ невозможно даже долить воды, знание особенностей процесса зарядки и разрядки, позволит не допустить серьёзных ошибок во время эксплуатации батареи.
Принцип работы и устройство аккумулятора автомобиля
Исправно работающая аккумуляторная батарея — такой же неотъемлемый атрибут, как рулевое управление или колёса с нормальным давлением в шинах. Они выпускаются сегодня в разных интерпретациях, требуют определённого ухода и отличаются конструктивными особенностями.
Назначение аккумулятора в автомобиле
Главные функции, которые призван выполнять автомобильный аккумулятор, заключаются в том, чтобы запускать двигатель машины и ещё обеспечивать током некоторые приборы-потребители. Это источник тока, который относится к возобновляемым, то есть, ёмкость батареи может и должна восстанавливаться, если она исправна. Каждая АКБ превращает электроэнергию в химическую, а впоследствии этот процесс происходит в обратном порядке.
Более всего это устройство востребовано на этапе запуска двигателя внутреннего сгорания. Однако аккумулятор также отвечает за работоспособность и питание всего электрооборудования на борту транспортного средства. Как только запущен мотор, то питание приборов осуществляется уже за счёт генератора, который одновременно заряжает и аккумулятор, ведь каждый запуск приводит к уменьшению его ёмкости.
Как только запущен мотор, то питание приборов осуществляется уже за счёт генератора, который одновременно заряжает и аккумулятор, ведь каждый запуск приводит к уменьшению его ёмкости.
За последние годы автомобили всех марок активно насыщаются электроприборами, системами климатического контроля, звука и видео, а все они питаются за счёт бортового электрического тока. Если генератор не справляется с его поставкой, то дополнительно идёт подпитка от батареи. Однако ключевая задача её заключается всё-таки в подаче тока для запуска стартера. Наибольший разряд АКБ случается в холодное время года, когда и возникает большинство проблем у автолюбителей.
Параметры АКБ
Необходимость знать основные параметры аккумулятора важна не только на этапе его покупки, но и в процессе обслуживания. Одной из ключевых характеристик считается ёмкость этого оборудования, которая даст информацию о длительности его бесперебойной работы. Для измерения используется такая единица, как ампер-часы, показывающая срок, в течение которого изделие может работать без дозаряда, расходуя свою ёмкость.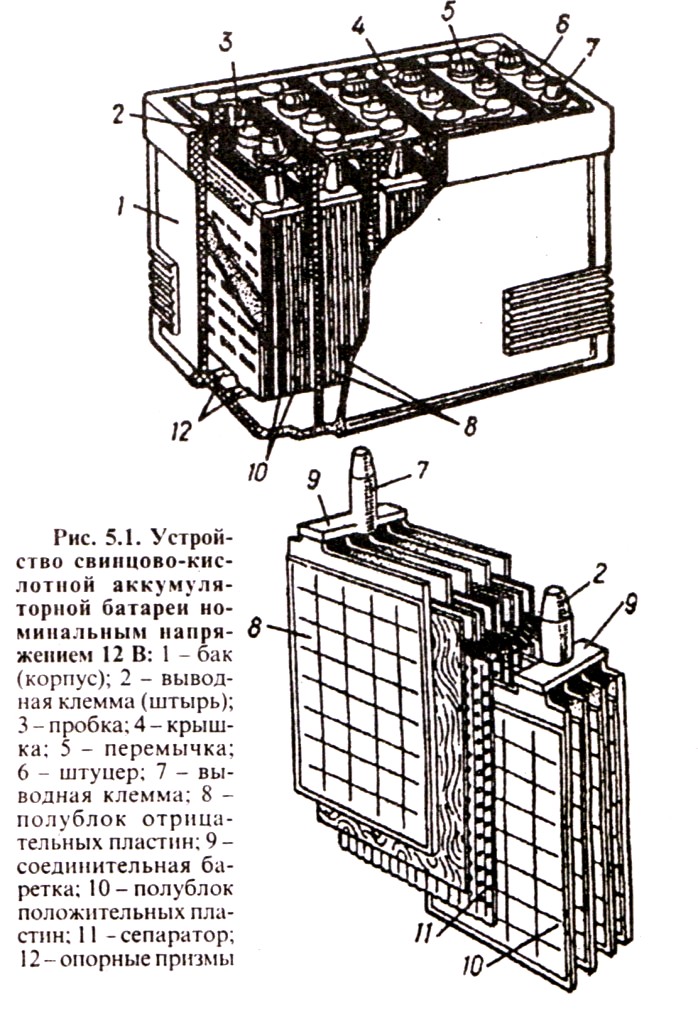 На само значение ёмкости оказывают влияние внешние факторы: температура окружающего воздуха, сила тока и особенности конструкции.
На само значение ёмкости оказывают влияние внешние факторы: температура окружающего воздуха, сила тока и особенности конструкции.
Другой важный критерий называют пусковой силой тока АКБ. Для того чтобы его узнать, измеряют значение, которое обеспечивает батарея при температуре 18 по Цельсию. Именно показатель пусковой силы тока берут во внимание, когда хотят определить исправность оборудования. Нормальное напряжение обычно находится около отметки в 12,6 В, но может колебаться в пределах 13–14 В, в зависимости от модели.
Каждая банка должна давать напряжение порядка 2В, а измерить его можно при помощи специальной нагрузочной вилки. Она устанавливает сопротивление, которое приходится на каждую из банок, учитывая также их ёмкость.
Важно помнить: перезарядка тоже нежелательна для аккумулятора, как и слабый заряд. Если не отключить вовремя зарядное устройство, это может спровоцировать закипание электролита.
Мощность заряда батареи можно получить, перемножив между собой напряжение и силу пускового тока. Однако, чтобы говорить о мощности, следует ещё учитывать температуру воздуха за окном машины. Слишком холодая погода отрицательно влияет на мощность. Потребуется больше тока для запуска, а потому зимой нужна большая мощность, нежели в тёплое время года.
Однако, чтобы говорить о мощности, следует ещё учитывать температуру воздуха за окном машины. Слишком холодая погода отрицательно влияет на мощность. Потребуется больше тока для запуска, а потому зимой нужна большая мощность, нежели в тёплое время года.
Чтобы узнать детальные характеристики, лучше обратиться к маркировке — как правило, она наносится на корпусе изделия. На ней можно найти производителя и год выпуска, товарный знак и тип аккумулятора, вес, количество банок и другие необходимые стандарты. Основным материалом может выступать эбонит, термопласт или пластмасса, прошедшая специальную обработку. Вес батареи не относится к базовым характеристикам и может даже отличаться от того значения, что заявил производитель. Это может произойти из-за того, что свинцовые пластины взаимодействуют с электролитом и постепенно разрушаются.
Устройство аккумулятора
Разберёмся далее, как устроен автомобильный аккумулятор. Он состоит из нескольких гальванических элементов, которые ещё принято называть банками.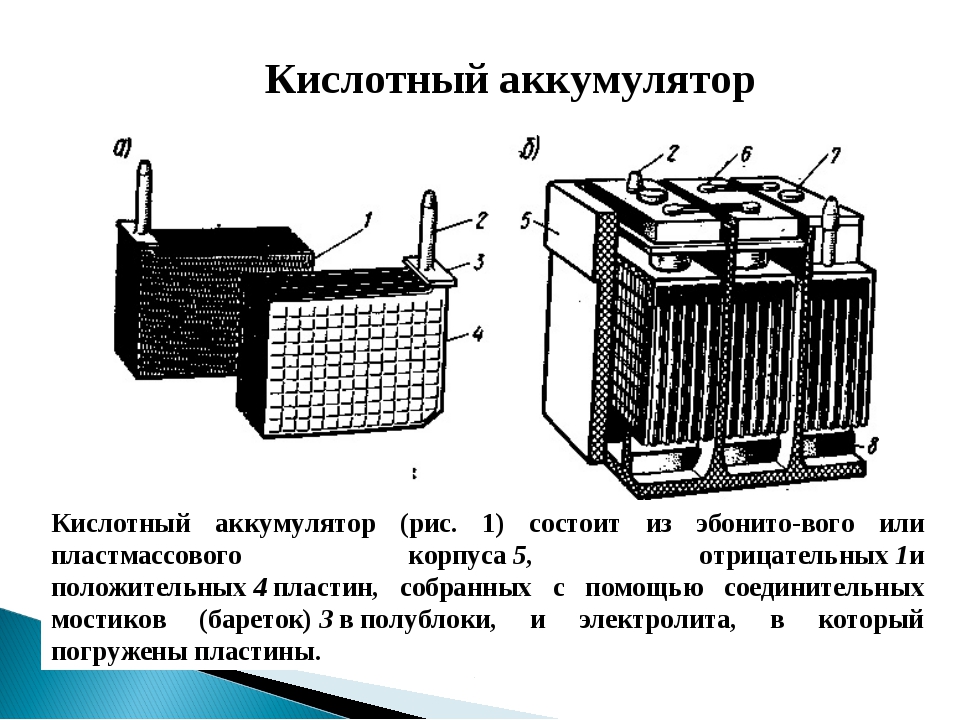 Они находятся в отдельных ячейках изолированно друг от друга. Каждая из таких ячеек содержит в себе блок с электродами, часть из которых аноды, а другая часть — катоды. Полублок состоит из большого количества тонких пластин, которые обладают сетчатой структурой. Чтобы разделить между собой анод и катод, применяется специальный материал-сепаратор.
Они находятся в отдельных ячейках изолированно друг от друга. Каждая из таких ячеек содержит в себе блок с электродами, часть из которых аноды, а другая часть — катоды. Полублок состоит из большого количества тонких пластин, которые обладают сетчатой структурой. Чтобы разделить между собой анод и катод, применяется специальный материал-сепаратор.
В полость заливают раствор разбавленной серной кислоты, которая хорошо проводит электрический ток. В традиционных аккумуляторах требовалось доливать дистиллированную воду. Из-за вступания в реакцию молекул кислорода и водорода плотность электролита постепенно повышалась. Современные батареи не требуют вмешательства человека, потому их принято называть необслуживаемыми. Излишек газов, который образуется под крышкой, автоматически выходит наружу при помощи специальных клапанов.
Разбирая устройство автомобильного аккумулятора, нужно заглянуть под его крышку. Там мы увидим 6 банок, которые подключены последовательно в одну цепь. Сам корпус устойчив к воздействию серной кислоты, а производится он обычно из специального пластика или другого изолята. В каждую из банок помещаются как положительные, так и отрицательные электроды, а на каждый из них, в свою очередь, наносится активная обмазочная масса.
Сам корпус устойчив к воздействию серной кислоты, а производится он обычно из специального пластика или другого изолята. В каждую из банок помещаются как положительные, так и отрицательные электроды, а на каждый из них, в свою очередь, наносится активная обмазочная масса.
Электрическое замыкание аккумуляторной батареи машины не происходит из-за разделяющих элементов, сепараторов. Для производства проводящих ток электродов чаще всего используется свинец с определёнными добавками. Если соединить его с кальцием, это позволит понизить уровень саморазряда и необходимость частого долива дистиллята.
Решётки электродов также могут быть изготовлены по разнообразным технологиям. Главная их задача заключается в отводе тока для снижения внутреннего сопротивления изделия. В конструкцию решётки для придания ей большей прочности вставляют направляющие и опорную раму. Иногда их могут располагать вертикально или в шахматном порядке — это тоже делает конструкцию более прочной. Чтобы улучшить взаимодействие с веществом-электролитом, на решётки наносят активную обмазку.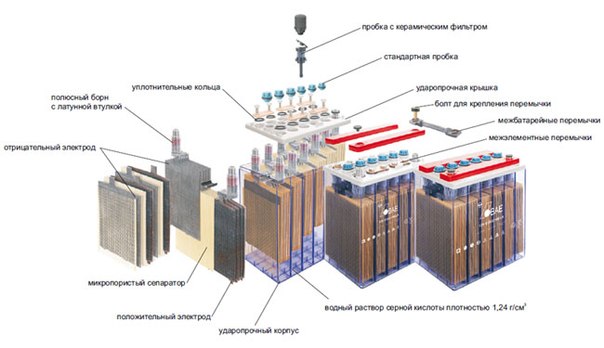 В случае с положительными пластинами – это диоксид свинца, в случае с отрицательными — свинец губчатый.
В случае с положительными пластинами – это диоксид свинца, в случае с отрицательными — свинец губчатый.
Подавляющее большинство современных автомобилей работает на батареях свинцово-кислотного типа, основу которых составляет жидкий электролит, помещённый под крышку корпуса. Однако за последние пару десятилетий широкое признание получили принципиально новые конструкции, избавленные от многих недостатков.
Кроме изделий с классическим жидким электролитом, на рынке можно встретить АКБ типа AGM или GEL. В них производитель также помещает электролит, но уже в связанном состоянии. Материал наподобие стекловолокна пропитывается электролитом и за счёт своей пористой структуры держит его как губка. В таком виде он и прилегает к пластинам. В другие типы аккумуляторов помещают гелеобразный электролит благодаря оксиду кремния, который добавляют в серную кислоту.
Принцип работы
Даже опытные автолюбители не всегда в полном объёме представляют себе принцип работы автомобильного аккумулятора. Основу составляет электрохимическая окислительная реакция свинца, которая происходит в растворе разбавленной водой серной кислоты. Когда происходит заряд, снижается количество диоксида свинца на пластине со знаком «минус». В это же самое время на положительной пластине количество свинца возрастает. При разряде аккумулятора осуществляются обратные процессы. Одновременно, когда АКБ автомобиля разряжается, возрастает объём воды в банках, а объём серной кислоты улетучивается. В большей степени это касалось батарей обслуживаемого типа.
Основу составляет электрохимическая окислительная реакция свинца, которая происходит в растворе разбавленной водой серной кислоты. Когда происходит заряд, снижается количество диоксида свинца на пластине со знаком «минус». В это же самое время на положительной пластине количество свинца возрастает. При разряде аккумулятора осуществляются обратные процессы. Одновременно, когда АКБ автомобиля разряжается, возрастает объём воды в банках, а объём серной кислоты улетучивается. В большей степени это касалось батарей обслуживаемого типа.
Итак, принцип работы аккумулятора в машине можно свести к сложным химическим реакциям. Как только включается любой электропотребитель (стартер на запуске или другой прибор), батарея начинает утрачивать свою ёмкость. Диоксид свинца, помещённый на пластины со знаком «плюс», а также свинец обычный на отрицательных, вступают во взаимодействие с раствором серной кислоты. Как результат — появляются вода и сульфат свинца. Одновременно электролит становится менее плотным.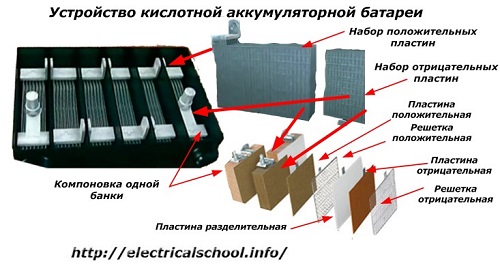
Когда мы подключаем аккумуляторную батарею своего автомобиля к зарядному устройству, начинается противоположная реакция. Накопленный сульфат свинца и дистиллированная вода обратно преобразовываются в серную кислоту и свинцовый диоксид. Чем дольше идёт заряд АКБ, тем большей становится плотность электролита. Одновременно происходит процесс сульфатации пластин.
Во время поездок на автомобиле происходит непрерывный, хотя и не быстрый, заряд аккумулятора, если, конечно, мы имеем дело с исправным генератором. То есть, восстанавливается его максимальная ёмкость, которую можно возобновить и принудительно, но для этого придётся снимать батарею и подключать её к зарядному устройству.
Немалое значение отводится температуре окружающего воздуха. Если она повышена, то мощность возрастает, но вместе с ней увеличиваются расход воды и разряд. Во время пониженной температуры все эти химические реакции замедляются, но вместе с ними уменьшаются ёмкость и значения пускового тока. В обычных условиях эксплуатации длительность службы АКБ не превышает 3–5 лет.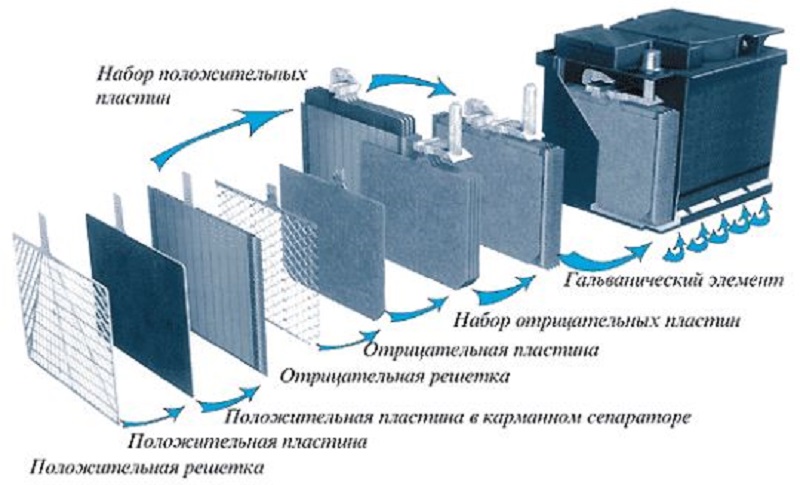 Многое зависит от типа батареи и входящих в состав пластин добавок, а также от ухода за ней и климатических условий эксплуатации.
Многое зависит от типа батареи и входящих в состав пластин добавок, а также от ухода за ней и климатических условий эксплуатации.
Чтобы алгоритм работы любой АКБ не нарушался, водитель должен уметь её обслуживать и соблюдать некоторые рекомендации для продления эксплуатационного срока службы. Они сводятся к следующим правилам:
- если оборудование относится к категории обслуживаемых, периодически проверяем уровень электролита в нём;
- клеммы и их наконечники должны быть сухими и чистыми, гарантировать хороший контакт;
- при окислении проводов или их наконечников их следует осторожно отсоединить, зачистить и проверить надёжность контакта;
- корпус батареи нужно держать в чистоте и сухости, убирать лишнюю пыль или следы масла.

Это основные советы для поддержания АКБ в своем автомобиле в исправном состоянии, что одновременно поможет продлить его эксплуатационный ресурс.
Как работает автомобильный аккумулятор 🚩 аккумулятор принцип работы 🚩 Запчасти и аксессуары
Устройство аккумулятора
Автомобильный аккумулятор или аккумуляторная батарея (АКБ) обычно состоит из 6 элементов. Общее напряжение АКБ — 12 вольт. Соответственно каждый элемент вырабатывает по 2 вольта.
Каждый элемент аккумулятора это свинцовая пластина, которая покрыта специальным активным веществом.
В аккумуляторе есть отрицательные и положительные пластины. Разница между ними заключается в веществе, которым они покрыты. Положительные обычно покрываются двуокисью свинца, а отрицательные мелкопористым или губчатым свинцом.
Ёмкость аккумуляторной батареи заполнена специальным электролитом на основе серной кислоты. Свинцовые элементы погружены в этот электролит.
Работа аккумулятора
Когда к АКБ подключают какую-либо нагрузку, она начинает вырабатывать электрический ток.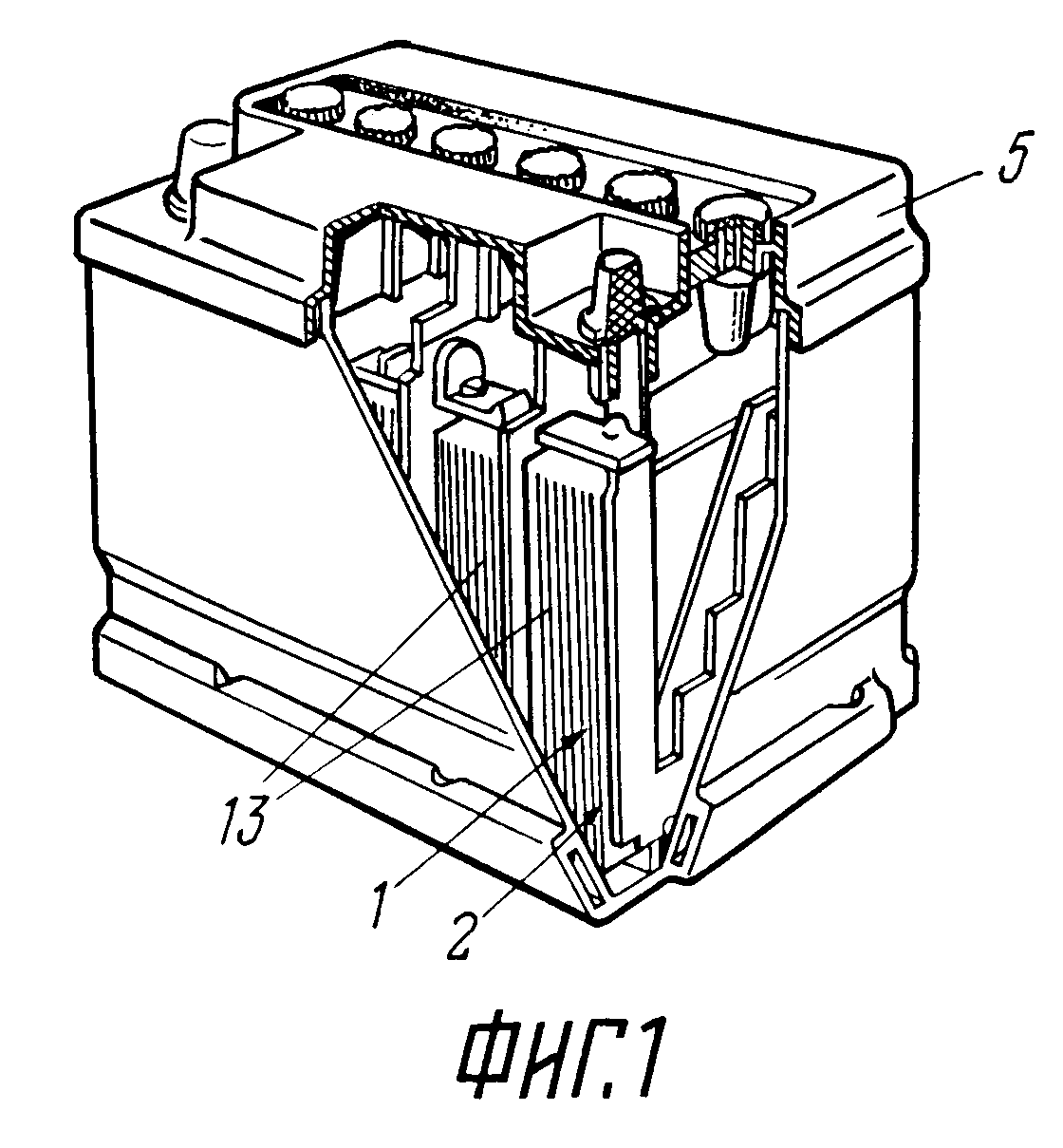 Происходит это в результате химической реакции между серной кислотой и активным веществом, которым покрыты пластины.
Происходит это в результате химической реакции между серной кислотой и активным веществом, которым покрыты пластины.
В процессе химической реакции электролитический раствор становится менее концентрированным, а на пластинах выпадает в осадок соль, а именно, сульфат свинца.
Чем больше соли осело на пластинах и чем меньше концентрация электролита, тем меньший электрический ток вырабатывает аккумулятор. Чтобы восстановить его нормальную работу, аккумулятор необходимо подключить к зарядному устройству.
Когда аккумулятор заряжается химическая реакция проходит в обратном направлении. Соль растворяется в электролите, что возвращает его концентрацию, а активное вещество на пластинах восстанавливается.
После зарядки АКБ возвращает свою способность вырабатывать электрический ток.
Выход из строя аккумуляторной батареи
В принципе, в аккумуляторе нет элементов, которые могли бы сломаться. Обычно его неисправности связаны не с его собственными дефектами, а с малым зарядом.
Аккумулятор быстро разряжается, если на нем имеются дополнительные нагрузки во время стоянки: оставленные включенными габариты или автомагнитола, ток утечки, который является частым явлением на старых автомобилях.
Сама АКБ в процессе службы, конечно же, изнашивается. Рано или поздно пластины подвергаются коррозии, активное покрытие на них обедняется, происходит истощение электролита.
Когда аккумулятор находится долгое время в разряженном состоянии, износ его элементов происходит намного быстрее.
Для увеличения срока службы аккумулятора его всегда необходимо поддерживать в заряженном состоянии.
Наибольший износ аккумуляторных батарей происходит при воздействии высоких температур, то есть летом, однако сказывается этот износ только в зимнее время.
Что такое аккумулятор? Принцип действия.
Аккумулятор — важный компонент электромобиля. Он служит для обеспечения запуска двигателя. Кроме того, аккумулятор является поставщиком электроэнергии в бортовую сеть автомобиля.
Обычно аккумулятор состоит из контейнера, который разделен перегородками на ячейки. В этих ячейках, называемых банками, расположено несколько связанных между собой специальных единиц. 12-вольтовый автомобильный аккумулятор имеет 6 таких ячеек.Каждый из этих блоков содержит набор положительных и отрицательных электродов. Между разнополюсными электродами, состоящими из свинцовых сеток, смазанных активным веществом, установлены сепараторы из непроводящего материала.
При отливке аккумулятора в рабочем состоянии внутрь канистр заливают электролит (смесь серной кислоты и воды), после чего заряжают с помощью специального зарядного устройства. В процессе увеличения плотности заряда электролита внутри аккумулятора происходят определенные химические реакции, в результате которых происходит накопление энергии.
Принцип действия АКБ
Принцип действия свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислой среде.
Энергия образуется в результате окисления свинца серной кислотой до сульфата. Электродом из оксида свинца может быть графит с выделением водорода. Оксид свинца нужен только для предотвращения выделения водорода на электроде. Водород реагирует с кислородом оксида и образует воду, восстанавливая оксид металла и, возможно, обеспечивает дополнительный выход энергии за счет окисления водорода.
Во время разряда происходит восстановление диоксида свинца на катоде и окисление на анодном свинце. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном. В результате получается, что при разряде аккумулятора серная кислота с одновременным образованием воды (и плотность электролита падает) расходуется, а при заряде наоборот вода «расходуется» на образование серной кислоты (плотность электролит растет).По окончании заряда при некоторых критических значениях концентрации сульфата свинца на электродах начинает преобладать процесс электролиза воды. При этом на катоде выделяется водород, на аноде — кислород. При зарядке нельзя допускать электролиза воды, иначе ее необходимо добавить.
Как работает система зарядки
Внутри генератора переменного тока ротор с ременным приводом становится электромагнитом, когда к нему подается ток. По мере вращения ротора в обмотках статора генерируется более высокий ток.Автомобиль потребляет довольно много электроэнергии для работы зажигание и другое электрооборудование.
Если питание было от обычного аккумулятор , он скоро закончится. Итак, в машине есть аккумуляторная аккумулятор и система зарядки, чтобы поддерживать его в рабочем состоянии.
Батарея имеет пары выводов тарелки погружают в смесь серной кислоты и дистиллированной воды.
Половина пластин соединена с каждой Терминал . Электричество, подводимое к батарее, вызывает химическую реакцию, в результате которой на один набор пластин откладывается дополнительный свинец.
Когда батарея выдает электричество, происходит прямо противоположное: лишний свинец растворяется с пластин в реакции, которая производит электрический ток. текущий .
Аккумулятор заряжается генератор на современных автомобилях или динамо-машиной на более ранних. Оба типа генератор , и приводятся в движение ремнем от двигатель .
генератор состоит из статор — стационарный комплект проволоки катушка обмотки, внутри которых вращается ротор.
Ротор электромагнит подается небольшое количество электроэнергии через углерод или медь-углерод кисти (контакты) касаются двух вращающихся металлических контактные кольца на его валу.
Вращение электромагнита внутри катушек статора генерирует гораздо больше электричества внутри этих катушек.
Электричество переменный ток — его направление потока меняется назад и вперед каждый раз при вращении ротора. Должно быть исправленный — превратились в односторонний поток, или постоянный ток .
Динамо-машина выдает постоянный ток, но она менее эффективна, особенно при малых двигатель скорости и весит больше, чем генератор.
Предупреждающая лампа на приборная доска светится, когда аккумулятор недостаточно заряжен, — например, при остановке двигателя.
Также может быть амперметр чтобы показать, сколько электричества вырабатывается, или индикатор состояния батареи, показывающий состояние батареи заряжать .
Как работает генератор
Как протекает ток в генераторе
При перемещении магнита мимо замкнутой проволочной петли в проволоке течет электрический ток. Представьте себе петлю из проволоки с магнитом внутри.
Северный полюс магнита проходит через верх петли как Южный полюс проходит его нижнюю часть.Оба прохода заставляют ток течь в одном направлении по контуру.
Полюса удаляются, и ток перестает течь до тех пор, пока южный полюс не достигнет вершины, а северный полюс — основания.
Это заставляет ток снова течь, но в противоположном направлении.
Автомобильный генератор переменного тока использует электромагнит для увеличения выработки электрического тока.
Как работает динамо
Обмотки возбуждения внутри корпуса — это электромагнит динамо.Ток генерируется во вращающемся якоре.В динамо-машине электромагниты неподвижны и называются поле катушки. Ток вырабатывается в арматура — еще один набор катушек, намотанных на вал и вращающихся внутри катушек возбуждения.
Принцип такой же, как у генератора переменного тока, но ток идет на коммутатор — металлическое кольцо, разделенное на сегменты, которые касаются угольных щеток, установленных в подпружиненный гиды. Два сегмента касаются пары щеток и подают к ним ток.
При вращении якоря ток меняет направление. Но к тому времени под щетки попала еще одна пара сегментов коммутатора, и эта пара подключена наоборот, поэтому выходящий ток всегда течет в одном направлении.
Регулировка тока к батарее
Ток от генератора выпрямляется в постоянный ток с помощью набора диоды которые позволяют току течь через них только в одном направлении.
Для зарядки аккумулятора подаваемое на него напряжение не должно быть слишком низким или слишком высоким.
Генератор имеет управляемое транзистором устройство управления, которое регулирует напряжение, подавая больший или меньший ток — по мере необходимости — на электромагнит.
Выпрямитель и регулятор обычно находятся внутри корпуса генератора переменного тока, но на некоторых генераторах переменного тока они находятся снаружи и установлены на корпусе генератора.
Динамо-машине не нужен выпрямитель — есть регулятор напряжения в отдельной коробке, в которой реле .
Одно реле контролирует уровень напряжения путем кратковременного отключения тока в катушках возбуждения.
Второе реле предотвращает перезарядку динамо-машины и повреждение аккумулятора.
Как работает аккумулятор — Любопытно
Представьте себе мир без батарей. Все те портативные устройства, от которых мы так зависим, были бы настолько ограничены! Мы сможем доставить наши ноутбуки и телефоны настолько далеко, насколько это досягаемо для их кабелей, что сделает это новое работающее приложение, которое вы только что загрузили на свой телефон, практически бесполезным.
К счастью, батарейки у нас есть. Еще в 150 г. до н.э. в Месопотамии парфянская культура использовала устройство, известное как багдадская батарея, сделанное из медных и железных электродов с уксусом или лимонной кислотой.Археологи считают, что на самом деле это не батареи, а в основном они использовались для религиозных церемоний.
Изобретение батареи в том виде, в котором мы ее знаем, приписывают итальянскому ученому Алессандро Вольта, который собрал первую батарею, чтобы доказать свою точку зрения другому итальянскому ученому Луиджи Гальвани. В 1780 году Гальвани показал, что лапы лягушек, подвешенных на железных или медных крючках, подергиваются при прикосновении к зонду из какого-либо другого металла. Он считал, что это вызвано электричеством из тканей лягушек, и называл это «животным электричеством».
Луиджи Гальвани обнаружил, что лапы лягушек, подвешенных на латунных крючках, дергались, когда их толкали зондом из другого металла. Он думал, что эта реакция была вызвана «животным электричеством» внутри лягушки. Источник изображения: Луиджи Гальвани / Wikimedia Commons.Вольта, первоначально впечатленный открытиями Гальвани, пришел к выводу, что электрический ток исходит от двух разных типов металла (крючки, на которых висели лягушки, и другой металл зонда) и просто передается через них, а не через них. из тканей лягушек.Он экспериментировал со стопками слоев серебра и цинка, перемежаемых слоями ткани или бумаги, пропитанной соленой водой, и обнаружил, что электрический ток действительно протекает через провод, приложенный к обоим концам стопки.
Volta также обнаружил, что, используя различные металлы в свае, можно увеличить количество напряжения.Он описал свои открытия в письме к Джозефу Бэнксу, тогдашнему президенту Лондонского королевского общества, в 1800 году. Это было довольно большое дело (Наполеон был весьма впечатлен!), И его изобретение принесло ему устойчивое признание в честь «вольта». ‘(мера электрического потенциала), названная в его честь.
Я сам, шутя в сторону, поражен тем, как мои старые и новые открытия … чистого и простого электричества, вызванного контактом металлов, могли вызвать такое волнение.Алессандро Вольта
Так что же именно происходило с этими слоями цинка и серебра и с дрожащими лягушачьими лапами?
Химия батареи
Аккумулятор — это устройство, которое накапливает химическую энергию и преобразует ее в электричество.Это известно как электрохимия, а система, лежащая в основе батареи, называется электрохимическим элементом. Батарея может состоять из одного или нескольких (как в оригинальной куче Вольты) электрохимических ячеек. Каждая электрохимическая ячейка состоит из двух электродов, разделенных электролитом.
Итак, откуда электрохимический элемент получает электричество? Чтобы ответить на этот вопрос, нам нужно знать, что такое электричество. Проще говоря, электричество — это тип энергии, производимый потоком электронов.В электрохимической ячейке электроны образуются в результате химической реакции, которая происходит на одном электроде (подробнее об электродах ниже!), А затем они перетекают на другой электрод, где расходуются. Чтобы понять это правильно, нам нужно поближе взглянуть на компоненты клетки и то, как они собраны вместе.
Электроды
Чтобы создать поток электронов, вам нужно где-то, чтобы электроны текли из , а где-то электроны текли с на .Это электроды ячейки. Электроны текут от одного электрода, называемого анодом (или отрицательным электродом), к другому электроду, называемому катодом (положительный электрод). Как правило, это разные типы металлов или другие химические соединения.
В котле Вольта анодом служил цинк, от которого электроны текли по проволоке (при соединении) с серебром, которое было катодом батареи. Он сложил много этих ячеек вместе, чтобы получилась общая свая, и поднял напряжение.
Но откуда анод вообще берет все эти электроны? И почему они так счастливы, что их отправили в веселый путь к катоду? Все сводится к химии, происходящей внутри клетки.
Нам необходимо понять несколько химических реакций. На аноде электрод реагирует с электролитом в реакции, в которой образуются электроны. Эти электроны накапливаются на аноде. Между тем, на катоде одновременно происходит другая химическая реакция, которая позволяет этому электроду принимать электроны.
Технический химический термин, обозначающий реакцию, которая включает обмен электронами, — это реакция окисления-восстановления, обычно называемая окислительно-восстановительной реакцией. Вся реакция может быть разделена на две половинные реакции, и в случае электрохимической ячейки одна полуреакция происходит на аноде, а другая — на катоде. Уменьшение — это усиление электронов, и это то, что происходит на катоде; мы говорим, что катод восстанавливается во время реакции. Окисление — это потеря электронов, поэтому мы говорим, что анод окисляется.
Каждая из этих реакций имеет определенный стандартный потенциал. Думайте об этой характеристике как о способности / эффективности реакции либо производить, либо поглощать электроны — ее силе в электронном перетягивании каната.
- Стандартные потенциалы полуреакций
Ниже приведен список половинных реакций, в которых происходит высвобождение электронов из чистого элемента или химического соединения. Рядом с реакцией указано число (E 0 ), которое сравнивает силу электрохимического потенциала реакции с силой готовности водорода расстаться со своим электроном (если вы посмотрите вниз по списку, вы увидите, что водородный полуреактор имеет нулевое значение E 0 ).E 0 измеряется в вольтах.
Причина, по которой этот список настолько интересен, заключается в том, что если вы выберете две реакции из списка и объедините их в электрохимическую ячейку, значения E 0 скажут вам, в каком направлении будет протекать общая реакция: реакция с более отрицательной реакцией. Значение E 0 отдает свои электроны другой реакции, и это определяет анод и катод вашей ячейки. Разница между двумя значениями E 0 говорит вам об электрохимическом потенциале вашей ячейки, который в основном представляет собой напряжение ячейки.
Итак, если вы возьмете литий и фторид и сумеете объединить их, чтобы сделать элемент батареи, у вас будет самое высокое напряжение, теоретически достижимое для электрохимического элемента. Этот список также объясняет, почему в котле Вольта цинк был анодом, а серебро — катодом: полуреакция цинка имеет более низкое (более отрицательное) значение E 0 (-0,7618), чем полуреакция серебра (0,7996). .
Источник: UC Davis ChemWiki
Любые два проводящих материала, которые вступают в реакцию с разными стандартными потенциалами, могут образовывать электрохимическую ячейку, потому что более сильный из них сможет забирать электроны у более слабого.Но идеальным выбором для анода был бы материал, который вызывает реакцию со значительно более низким (более отрицательным) стандартным потенциалом
Как работает интеллектуальная батарея? — Батарейный университет
Узнайте о различных шинных системах и их ограничениях.
Спикер на конференции по батареям однажды сказал: «Батарея — это дикое животное, и искусственный интеллект приручил ее». Батарея иллюзорна и не показывает видимых изменений в процессе использования; он выглядит одинаково, когда он полностью заряжен или пустой, новый или старый и требует замены.Для сравнения, автомобильная шина деформируется при низком уровне воздуха и указывает на окончание срока службы при износе протектора.
Недостатки батареи можно резюмировать следующими тремя проблемами: [1] Пользователь не знает, сколько времени автономной работы осталось у батареи; [2] хост не уверен, может ли батарея удовлетворить потребность в энергии; и [3] зарядное устройство должно быть адаптировано для каждого размера и химического состава батареи. Решения сложны, и «умная» батарея обещает уменьшить некоторые из этих недостатков.
Пользователи аккумуляторов представляют себе аккумуляторную батарею как накопитель энергии, который напоминает топливный бак, подающий жидкое топливо.По соображениям простоты аккумулятор можно рассматривать как таковой; однако измерение запасенной энергии электрохимического устройства намного сложнее.
В то время как обычный датчик уровня топлива измеряет входящую и выходящую жидкость из бака известного размера с минимальными потерями, датчик уровня заряда батареи имеет неподтвержденные определения и показывает только напряжение холостого хода (OCV), которое является непостоянным отражением. заряда (SoC). Проблема усугубляется тем, что аккумулятор — это негерметичный и сжимающийся сосуд, который теряет энергию и потребляет меньше энергии с каждым зарядом.По мере уменьшения емкости указанный рейтинг в Ач (ампер-часах) больше не соответствует действительности. Датчик уровня топлива не может сам по себе оценить емкость; после перезарядки показание всегда показывает полный, даже если емкость упала до половины указанного Ач.
Самый простой метод измерения состояния заряда — это считывание напряжения, но это может быть неточным, поскольку токи нагрузки снижают напряжение во время разряда. Самая большая проблема — это плоская кривая напряжения разряда для большинства литиевых и никелевых батарей.Температура тоже играет роль; тепло повышает напряжение, а холодная — понижает. Перемешивание из-за предыдущей зарядки или разрядки вызывает дальнейшие ошибки, и батарее требуется несколько часов отдыха для нейтрализации. (См. BU-903: Как измерить уровень заряда.)
Большинство батарей для медицинских, военных и вычислительных устройств являются «умными». Это означает, что между аккумулятором, оборудованием и пользователем происходит некоторый уровень связи. Определения «умного» различаются между производителями и регулирующими органами, и самая простая интеллектуальная батарея может содержать не что иное, как микросхему, которая настраивает зарядное устройство на правильный алгоритм зарядки.В глазах форума Smart Battery System (SBS) эти батареи нельзя назвать умными. На форуме SBS говорится, что интеллектуальная батарея должна отображать состояние заряда.
Безопасность — ключевая цель дизайна, и концепция SBS заключается в размещении системного интеллекта внутри аккумуляторной батареи. Таким образом, батарея SBS взаимодействует с микросхемой управления зарядом по замкнутому контуру. Несмотря на это цифровое наблюдение, большинство зарядных устройств SBS также полагаются на аналоговые сигналы от химической батареи для прекращения заряда, когда батарея полностью заряжена.Кроме того, по соображениям безопасности добавлено избыточное измерение температуры.
Benchmarq была первой компанией, предложившей датчик уровня топлива в 1990 году. Сегодня многие производители предлагают микросхемы интегральных схем (ИС) в однопроводных и двухпроводных системах, также известные как Syst
Механизм и принцип кондиционирования воздуха — Easy Diagrammatic Explanation
Вы когда-нибудь задумывались, как получить прохладный ветерок от кондиционера. Какой механизм на самом деле задействован в производстве холодного воздуха жарким летом? Вот простое схематическое объяснение принципа работы кондиционера.Независимо от того, какой тип кондиционера вы используете, с окнами, на раздельной стене (PTAC), в напольном шкафу или на крыше, основной принцип для всех них одинаков. Даже инверторный кондиционер, который претерпел изменения в примитивной конструкции, все еще следует тому же принципу и законам термодинамики.
Основной механизм и принцип
Как работает кондиционер — Схема
Пояснение: Каждый кондиционер (также произносится как AC, A / C или Air Cooler в некоторых регионах мира) имеет внутри компрессор.Он работает для сжатия и перекачки хладагента. При сжатии хладагента выделяется тепло. Чтобы отвести это тепло, сжатый хладагент перекачивается в змеевики конденсатора, где вентилятор выдувает тепло во внешнюю атмосферу. Во время этого процесса хладагент принимает жидкую форму. Этот жидкий хладагент перекачивается к расширительному клапану. К расширительному клапану подключен датчик температуры, который работает в соответствии с настройками термостата. Расширительный клапан подает необходимое количество хладагента в испаритель (охлаждающие змеевики), где сжиженный хладагент принимает газообразную форму.Преобразование из жидкого в газообразное состояние из-за расширения вызывает охлаждение, поскольку энергия поглощается из окружающей среды. Воздух, проходя через ребра (прикрепленные к змеевикам), охлаждается и выдувается в комнату. Затем газообразный хладагент в охлаждающих змеевиках поступает в компрессор и снова сжимается. Цикл продолжается, пока компрессор не отключен.
В двух словах, кондиционер забирает тепло из помещения и отдает его наружу. Внутри помещения действует как источник, а снаружи как приемник тепла.
В автомобильных кондиционерах между конденсатором и расширительным клапаном устанавливается ресивер-осушитель. Он служит для сбора излишков хладагента, когда он не требуется для охлаждения. Он также имеет влагопоглотитель, который поглощает влагу, присутствующую в хладагенте.
Кондиционеры с инвертором: В этих кондиционерах используется инвертор для управления скоростью компрессора. Электричество сначала выпрямляется в постоянный ток (постоянный ток), а затем обратно обратно до требуемой частоты переменного тока (переменного тока) с использованием широтно-импульсной модуляции.
