Как защитить металл от коррозии в домашних условиях
Минувший век характеризуется возникновением огромного количества принципиально новых материалов, нашедших широкое применение в разнообразнейших отраслях человеческой жизнедеятельности, включая и строительную. Собственно говоря, в материаловедении произошла подлинная революция, причем значительное внимание было уделено вопросам предотвращения коррозии металлов и разработке материалов, необходимых для достижения этой цели. Так, например, появились различные композитные панели, гальванические покрытия, облицовочные материалы из строительной керамики (керамогранит, облицовочный кирпич и т. д.), прочие современные строительные материалы, не нуждающиеся в защите путем дополнительной обработки.
Применение в строительстве металлических изделий, как и прежде, остается востребованным чрезвычайно широко. Перила, декоративные решетки и ограждения даже сегодня чаще всего изготавливают из металлов, которые подвержены коррозии. Так, отделка фасадов, которую в наше время осуществляют посредством использования тех или иных материалов, устойчивых к воздействию атмосферной влаги, все же не обходится без применения крепежа, узлов ввода-вывода коммуникаций, иных скрытых элементов. Данные компоненты наиболее часто выполняются из металла, а потому жизненно нуждаются в антикоррозионной защите.
Так, отделка фасадов, которую в наше время осуществляют посредством использования тех или иных материалов, устойчивых к воздействию атмосферной влаги, все же не обходится без применения крепежа, узлов ввода-вывода коммуникаций, иных скрытых элементов. Данные компоненты наиболее часто выполняются из металла, а потому жизненно нуждаются в антикоррозионной защите.
Хорошо известно, что основной причиной коррозии является вода, которая неминуемо попадает на металлические поверхности даже в помещениях. А потому наиболее эффективным и, пожалуй, единственным способом защиты металлов, подверженных коррозии, является нанесение изолирующих составов и химических покрытий.
К традиционным способам предохранения металлических изделий от коррозии относится механическая зачистка старой ржавчины, а также нанесение преобразователей ржавчины, позволяющих удалить ее остатки, после чего поверхность металла покрывается грунтом и лакокрасочным защитным слоем.
Некоторые из производителей лакокрасочных материалов рекомендуют осуществить завершение этого процесса путем нанесения поверх слоя краски специального защитного состава. При этом основное внимание необходимо обратить на то, чтобы грунтовки, краски и лаки были качественными. На упаковках с грунтами указываются виды специальных добавок, улучшающих свойства состава: изолирующих, фосфатирующих, пассивирующих и протектирующих.
При этом основное внимание необходимо обратить на то, чтобы грунтовки, краски и лаки были качественными. На упаковках с грунтами указываются виды специальных добавок, улучшающих свойства состава: изолирующих, фосфатирующих, пассивирующих и протектирующих.
Как видим, окраска металлических поверхностей «по старинке» — процесс достаточно сложный и трудоемкий, отнимающий много сил и времени. Ныне компании-производители рекомендуют разработанные ими антикоррозионные составы, отличающиеся большей универсальностью, применение которых позволяет одновременно решать не какую-либо одну, а сразу несколько задач. Наиболее популярными среди потребителей являются так называемые средства «два в одном» и «три в одном». Краска «два в одном» сочетает в себе находящиеся в одной емкости грунтующий и окрашивающий составы, при помощи которых возможно выполнение как грунтования, так и окончательной окраски металлических поверхностей.
Нередко производителями подобных красок рекомендуется использование составов типа «два в одном» по предварительно огрунтованным поверхностям, работающим в агрессивных средах, к примеру для кровли.
Композиции «три в одном», кроме грунта и краски, включают в свой состав также и преобразователь ржавчины. Их целесообразно использовать при окрашивании сильно заржавевших поверхностей, при этом необходимо удалить лишь верхний рыхлый слой ржавчины. На упаковках подобных составов обычно можно видеть надпись — непосредственно на ржавчину.
Может ли вода защитить металл от коррозии?
Казалось бы как вообще такое возможно? Этого не может быть, потому что этого быть не может никогда! Однако прогресс не стоит на месте. Он стремительно движется вперед во всех отраслях, в т. ч. и в сфере разработок новых видов лакокрасочных материалов.
Преимущества, которыми обладают лакокрасочные материалы (ЛКМ) на основе водных полимеров, способствуют ежегодному росту их производства и применения. На состоявшейся 3–4 декабря 2013 г. в г. Дюссельдорфе (Германия) конференции European Coatings Conference «Waterborne coatings» были рассмотрены достижения, проблемы и пути их решения в области водных ЛКМ.
Высокое качество водных 2К полиуретановых систем в сочетании с низкой эмиссией растворителей вызывает большой спрос промышленности. Эти материалы успешно зарекомендовали себя во многих сегментах рынка, поскольку они позволяют преодолеть разрыв между растущей потребностью в «зеленых» решениях и требованиями к качеству со стороны промышленности и профессионалов. Поставщики лакокрасочных материалов (ЛКМ) постоянно совершенствуют качество водных систем, а сырьевая отрасль развивает инновационные концепции как для смол, так и для отвердителей.
В докладе д-ра Кристофа Ирла (Christoph Irle), Bayer Material Science (Германия), особое внимание было уделено производству и надежности таких составов. Рассмотрение этих вопросов в дальнейшем поможет получить водные 2К системы, близкие к самой высокой отметке, которая уже многие десятилетия установлена для 2К полиуретановых систем. Продолжил тему полиуретанов д-р Норберт Питшман (Norbert Pietschmann), Institute fur Lack und Fabric (Германия), выступив с докладом «Водные УФ-отверждаемые ЛКМ для защиты стали от коррозии».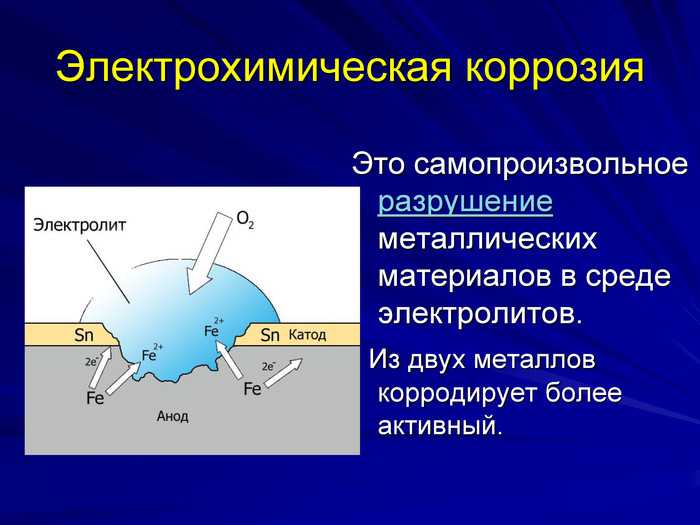 При испытаниях противокоррозионных свойств пигментов, ингибиторов, связующих или их комбинаций он использовал электрохимические измерения, обеспечивающие более быстрое получение результатов. Этим методом
При испытаниях противокоррозионных свойств пигментов, ингибиторов, связующих или их комбинаций он использовал электрохимические измерения, обеспечивающие более быстрое получение результатов. Этим методом
Защита металла от коррозии в домашних условиях
Существуют ли «народные» средства против ржавчины?
И обычное железо, и даже высококачественная сталь во влажном воздухе, который наверняка присутствует в гаражах, сараях и прочих подсобных помещениях подвергаются коррозии — постепенно покрываются буро-коричневой рыхлой пленкой ржавчины.
Секреты удаления ржавчины есть. Ржавчину проще всего снять обработкой разбавленным водным раствором соляной или серной кислоты, содержащим ингибитор кислотной коррозии уротропин. Ингибиторы (от латинского «ингибео» — останавливаю, сдерживаю) — вещества, тормозящие химическую реакцию (в данном случае реакцию растворения металла в кислоте). Но ингибитор коррозии не мешает взаимодействию кислоты с оксидом и гидроксидом железа, из которых состоит ржавчина.
Если заржавели оконные шпингалеты, мелкие детали велосипеда, болты или гайки, их погружают в 5% раствор кислоты с добавкой 0,5 г уротропина на литр, а на крупные вещи такой раствор наносят кистью.
Использовать растворы сильных кислот без ингибитора рискованно: можно растворить не только ржавчину, но и само изделие, поскольку железо — активный металл и взаимодействует с сильными кислотами с выделением водорода и образованием солей. В качестве ингибитора кислотной коррозии при удалении ржавчины можно использовать и картофельную ботву. Для этого в стеклянную банку кладут свежие или засушенные листья картофеля и заливают 5-7%-й серной или соляной кислотой так, чтобы уровень кислоты был выше примятой ботвы. После 15-20-минутного перемешивания содержимого банки кислоту можно сливать и использовать для обработки ржавых железных изделий.
Преобразователь ржавчины превращает ее в прочное покрытие поверхности коричневого цвета. На изделие кистью или пульверизатором наносят 15-30%-й водный раствор ортофосфорной кислоты и дают изделию высохнуть на воздухе. Еще лучше использовать ортофосфорную кислоту с добавками, например, 4 мл бутилового спирта или 15 г винной кислоты на 1 л раствора ортофосфорной кислоты. Ортофосфорная кислота переводит компоненты ржавчины в ортофосфат железа FePO4 , который создает на поверхности защитную пленку. Одновременно винная кислота связывает часть производных железа в тартратные комплексы.
Ортофосфорная кислота переводит компоненты ржавчины в ортофосфат железа FePO4 , который создает на поверхности защитную пленку. Одновременно винная кислота связывает часть производных железа в тартратные комплексы.
Металлические поверхности, сильно изъеденные ржавчиной, обрабатывают:
- смесью 50 г молочной кислоты и 100 мл вазелинового масла. Кислота превращает метагидроксид железа из ржавчины в растворимую в вазелиновом масле соль — лактат железа. Очищенную поверхность протирают тряпочкой, смоченной вазелиновым маслом;
- раствором 5 г хлорида цинка и 0,5 г гидротартрата калия в 100 мл воды. Хлорид цинка в водном растворе подвергается гидролизу и создает кислую среду. Метагидроксид железа растворяется за счет образования в кислой среде растворимых комплексов железа с тартрат-ионами;
Отворачивать приржавевшие гайки помогает смачивание керосином, скипидаром или олеиновой кислотой. Через некоторое время гайку удается отвернуть. Затем можно поджечь керосин или скипидар, которым ее смачивали. Обычно этого достаточно для разъединения гайки и болта. Самый последний способ: к гайке прикладывают сильно нагретый паяльник. Металл гайки расширяется, и ржавчина отстает от резьбы; теперь в зазор между болтом и гайкой можно впустить несколько капель керосина, скипидара или олеиновой кислоты, и на этот раз гайка отвернется ключом.
Затем можно поджечь керосин или скипидар, которым ее смачивали. Обычно этого достаточно для разъединения гайки и болта. Самый последний способ: к гайке прикладывают сильно нагретый паяльник. Металл гайки расширяется, и ржавчина отстает от резьбы; теперь в зазор между болтом и гайкой можно впустить несколько капель керосина, скипидара или олеиновой кислоты, и на этот раз гайка отвернется ключом.
Есть и другой способ разъединения ржавых гайки и болта. Вокруг заржавевшей гайки делают «чашечку» из воска или пластилина, бортик которой выше уровня гайки на 3-4 мм. Заливают в чашечку разбавленную серную кислоту и кладут кусочек цинка. Через сутки гайка легко отвернется ключом. Чашечка с кислотой и металлическим цинком на железном основании — это миниатюрный гальванический элемент. Кислота растворяет ржавчину, и образовавшиеся катионы железа восстанавливаются на поверхности цинка; в то же время металл гайки и болта не растворяется в кислоте до тех пор, пока у кислоты есть контакт с цинком, поскольку цинк более активный в химическом отношении металл, чем железо.
Чтобы предохранить от ржавления столярный или слесарный инструмент, его смазывают с помощью кисточки раствором 10 г воска в 20 мл бензина. Воск растворяют в бензине на водяной бане, не используя открытого огня (бензин огнеопасен).
Полированный инструмент защищают, нанося на его поверхность раствор 5 г парафина в 15 мл керосина. А старинный рецепт мази для защиты металла от ржавчины таков: растапливают 100 г свиного жира, добавляют 1,5 г камфоры, снимают с расплава пену и смешивают его с графитом, растертым в порошок, чтобы состав стал черным. Остывшей мазью смазывают инструмент и оставляют его на сутки, а потом полируют металл шерстяной тряпочкой.
Чтобы в будущем не мучиться, отворачивая крепежные изделия с проржавевшей резьбой, ее заранее смазывают смесью вазелина с графитовым порошком. Вместо вазелина можно взять и любую другую жировую смазку нейтрального или слабощелочного типа. Болты и гайки на такой смазке легко отворачиваются даже через несколько лет пребывания под открытым небом.
Методы предотвращения образования ржавчины при жидкостной абразивоструйной обработке стали
3,1 %
галлонов в сутки
Расходы на устранение последствий коррозии для США в 2015 году:
более
500 000 000 000 дол. США
По словам политиков, ремонт разрушающейся инфраструктуры — одна из величайших проблем Америки,
и ими выделяются средства на это.
Это отличная новость для операторов абразивоструйной обработки.
Подготовка поверхности и защитные покрытия являются одними из немногих отраслей промышленности, которые выигрывают от подобного
ухудшения в мировом масштабе. Эта ситуация дает возможность роста для операторов абразивоструйной обработки, которые
понимают, как подготовить поверхности для защиты от ржавчины.
1760 дол. США
на человека
ЧТО ТАКОЕ РЖАВЧИНА?
КАК ФОРМИРУЕТСЯ РЖАВЧИНА?
КАК ПРЕДОТВРАТИТЬ РЖАВЧИНУ?
ЧТО ТАКОЕ РЖАВЧИНА?
Все металлы корродируют вследствие химических реакций с окружающей средой (за исключением четырех редких металлов: иридия, ниобия, осмия и тантала).
Когда железо и сплавы железа корродируют, мы называем это ржавлением.
Продуктом коррозии является ржавчина, она же гидратированный оксид железа:
ОКСИД ЖЕЛЕЗА: FE203
Fe2O3.xh3O
Кислород стремится
объединиться в пару с
этими двумя
электронами
ПОЧЕМУ ОБРАЗУЕТСЯ РЖАВЧИНА?
Кислород (O) является высоко реактивным элементом. Только один элемент (фтор) имеет более высокую электроотрицательность — то есть больше склонен к «краже» электронов, чем кислород. Кислород будет формировать устойчивые связи практически со всеми другими элементами для образования оксидов.
Железо стремится
«отдать» эти
два электрона
Железо (Fe) является неблагородным металлом, что означает, что оно склонно к тому, чтобы отказываться от электронов (в отличие от благородных металлов, таких как золото и платина, которые не отдают электроны, не вступают в реакцию и не корродируют при нормальных условиях). Железо — самый распространенный элемент на Земле, по массе.
Железо — самый распространенный элемент на Земле, по массе.
При встрече кислорода и железа, кислород забирает электроны железа и они связываются, образуя оксид железа.
Реакция окисления происходит везде, где кислород сталкивается с поверхностью, образуя тонкую пленку на подложке (толщиной менее 0,005 микрона / 0,0002 мил). Такой пассивирующий слой предотвращает дальнейший контакт и реакцию кислорода с металлом.
Кислород и железо образуют на поверхности пассивирующий слой оксида железа, который препятствует дальнейшему окислению — но не в достаточной степени.
Почти все металлы образуют пассивирующие оксидные слои. Медь имеет зеленую патину. Серебро имеет тусклый оттенок. На нержавеющей стали пассивирующий слой оксида хрома защищает сталь от коррозии.
Однако в случае с железом и углеродистой сталью пассивирующий оксидный слой не так полезен. Хрупкий и громоздкий слой оксида железа не только не прилипает к подложке, не обеспечивая таким образом защиту для лежащего в его основе железа, но и также является гигроскопичным , то есть вытягивает влагу из воздуха.
Наличие воды на поверхности само по себе не является достаточным для того, чтобы вызвать коррозию.* Но когда вода содержит растворенные соли, или является кислой или основной, то появляются условия для образования коррозионного элемента.
*Если чистая вода попадает в трещину или щель, кислородная недостаточность может вызвать накопление ионов водорода, создавая кислый раствор, который может привести к коррозии.
Внутри коррозионного элемента
Коррозионный элемент образуется при наличии раствора электролита, т. е. соли, растворенной в воде, которая инкапсулирует два участка на металлической поверхности с различными электрическими потенциалами, например:
- На границе встречи между двумя разнородными металлами, между двумя зернами внутри одного и того же металла или между двумя полостями примесей в сплаве
- Вокруг краев и углов деформированных кристаллических структур
[1] В этих условиях железо (Fe) на аноде отдает свои электроны, разделяясь на ионы Fe2+ .
[2] Fe2+ и OH связываются в последовательности реакций, которые в конечном итоге производят ржавчину, также известную как гидратированный оксид железа.
[3] Ионы ОН проходят через раствор электролита к новому, противоположно заряженному Fe2+ ионы на аноде.
Электроны [4] движутся от анода [6] к катоду [7], где они вступают в реакцию с молекулами воды и кислорода для производства ионов гидроксида [5], OH.**.
**Это реакция в нейтральном или основном растворе. В кислом растворе два иона водорода обращаются в молекулу газа водорода.
ФОРМЫ КОРРОЗИИ
NACE распознает десять форм коррозии.
Наиболее актуальны для операторов абразивоструйной обработки:
Сплошная коррозия
Коррозия, которая появляется равномерно на большей части или на всей поверхности, благодаря «танцующему» движению анодов и катодов по поверхности. Равномерная коррозия приводит к большей потере металла, чем любая другая форма, но ее последствия с меньшей вероятностью вызовут разрушение структуры, чем локальные формы коррозии — но все же это возможно, если допустить бесконтрольное протекание.
Щелевая коррозия
Коррозия, имеющая место в тесных промежутках между поверхностями. Форма щели препятствует проникновению кислорода и распространению ионов водорода (процесс, называемый гидролизом), создавая кислотный раствор, который ускоряет коррозию. Скорость коррозии в трещинах может быть до 400 раз выше по сравнению со скоростью коррозии на плоской поверхности.
Заполняющая ржавчина
Оставленные без контроля скопления ржавчины в щели могут привести к появлению массы ржавчины, которая деформирует поверхности, разрывает на части пластины и разрушает структуры.
Коррозионное растрескивание под напряжением
Эта трудно обнаруживаемая форма коррозии может иметь катастрофические последствия. Поскольку структурные напряжения создают трещины в базовом металле, в трещинах образуется ржавчина, ослабляющая структуру из-за потери металла. Поскольку оксиды железа занимают больше объема, чем железо, ржавчина в трещине создает дополнительное давление, которое усугубляет проблему.
Электрохимическая коррозия.
Коррозия, возникающая на границе встречи двух разных металлов. Разница в напряжении металлов вызывает формирование анода на менее благородном металле, с катодом на благородном металле. Напомним, что неблагородные металлы склонны отдавать электроны, становиться ионами и окисляться.
Точечная коррозия
При точечной коррозии потери металла на аноде вызывают коррозионное углубление в подложке, что может привести к перфорации металла. Легко недооценить серьезность точечной коррозии при визуальном осмотре, поскольку углубление может образовывать полость под поверхностью, а устье углубления может быть затемнено ржавчиной. При оставлении без контроля, точечная коррозия может привести к структурному разрушению.
Точечная коррозия является особенностью всех локальных коррозионных атак. Она ускоряется, когда агрессивные ионы, такие как хлорид (Cl-), присутствуют в растворе, т. е. соль (NaCl), растворена в воде, поскольку агрессивные ионы атакуют и растворяют пассивирующий слой.
Ионы хлорида проникают в пассивирующий слой, разрушая молекулы оксида железа и подвергая воздействию лежащий в основе металл.
Как хлорид атакует пассивирующий слой.
После кислорода следующим наиболее реактивным (электроотрицательным) элементом является хлор. Ионы хлорида стремятся отдавать электроныи испытывают сильное притяжение к противоположно заряженным ионам железа на поверхности.
Подталкиваемые к поверхности, ионы хлорида проникают сквозь пассивирующий слой оксида железа, реагируя с ним и заставляя его растворяться до тех пор, пока поверхность металла не подвергнется воздействию раствора электролита и не образуется коррозионный элемент.
Мгновенная ржавчина
Точечная ржавчина является общим воздействием коррозии, которая представляет собой значительную проблему для операторов абразивоструйной обработки.
Абразивоструйная обработка механически повреждает пассивирующий слой, который защищает металл от коррозии. В случае гидроабразивной обработки вода также присутствует на поверхности и находится в прямом контакте с металлом через разрушенный пассивирующий слой.
В случае гидроабразивной обработки вода также присутствует на поверхности и находится в прямом контакте с металлом через разрушенный пассивирующий слой.
Если на поверхности есть соли, они растворяются в воде, формируя раствор электролита и образуя коррозионный элемент. Такая быстродействующая атака может вызвать видимую ржавчину уже через 30 минут.
Мгновенная ржавчина также является проблемой для сухой абразивной обработки – и любого вида подготовки поверхности. При высокой влажности соли будут притягивать влагу из атмосферы на поверхность металла, образуя коррозионный элемент. Хлорид натрия может вытягивать влагу из атмосферы при относительной влажности 75 %. Другие, менее обильные соли притягивают влагу при относительной влажности всего в 25–35 %. При чистом воздухе (и бессолевой поверхности) атмосферная коррозия не будет иметь место при относительной влажности менее 45 %. Но с увеличением относительной влажности скорость коррозии возрастает в геометрической прогрессии.
Если вы проводите абразивоструйную обработку в помещении, влажность можно контролировать с помощью осушителей. Избегайте абразивоструйной обработки под дождем. Тем, кто привык проводить абразивоструйную обработку ранним утром, следует проявлять осторожность: роса на стали, только что прошедшей абразивоструйную обработку, является проблемой. При нагревании атмосферы металл дольше остается холодным, и на стали образуется конденсат.
Какое количество мгновенной ржавчины допустимо?
В то время как для некоторых покрытий некоторый невысокий уровень мгновенной ржавчины может находиться в пределах допусков, во всех случаях мгновенная ржавчина ухудшает адгезию. Нанесение покрытия поверх значительной мгновенной ржавчины приведет к выходу покрытия из строя, а также к началу дальнейших коррозионных реакций.
Узнайте у производителя покрытия о допустимых уровнях мгновенной ржавчины. В технических характеристиках покрытий может быть указан допустимый промежуток времени между абразивоструйной обработкой и нанесением покрытия.
| Легкий | Средний | Тяжелый |
| Поверхность видна. Наблюдается небольшое количество ржавчины. | Поверхность затемнена. Ржавчина хорошо прилегает. | Поверхность затемнена. Ржавчина свободно прилегает |
Нитевидная коррозия
Эта форма щелевой коррозии скапливается под краской после того, как покрытие смачивается водой.Коррозия принимает вид нитей, так как ржавеет поверхность, подверженная осмотическому вспучиванию.
Осмотическое вспучивание
Растворимые соли (нитевидная коррозия)
Эта форма щелевой коррозии скапливается под краской после того, как покрытие смачивается водой.Коррозия принимает вид нитей, так как ржавеет поверхность, подверженная осмотическому вспучиванию. Несмотря на то, что хлориды, сульфаты и нитраты не имели достаточно плохой репутации, они также являются причиной разрушения покрытия, называемого осмотическим вспучиванием.
Покрытие представляет собой полупроницаемую мембрану, которая пропускает воду, но не другие растворимые ионы, такие как соль или хлористоводородная кислота. Когда вода, проходя через мембрану, растворяет ионы на поверхности металла, она снижает давление паров раствора под покрытием, и вода «застревает» под вспучиванием.Ионы не могут пройти через мембрану, чтобы выровнять давление, но это не мешает воде пытаться дальше. В участок вспучивания попадает больше воды, чем выходит из него, что приводит к отслоению покрытия. Внутри участка вспучивание образуется коррозионный элемент.
Ультраточечная ржавчина
В отличие от других видов коррозии, ультраточечная ржавчина — это рельеф, а не процесс. Когда глубинный профиль анкерного рельефа превышает глубину сухой пленки наносимого покрытия, покрытие не покрывает пиков. Пленка на этом участке становится сверхтонкой и быстро портится, подвергая подложку коррозии.
Чтобы надежно предотвратить ультраточечную ржавчину, необходимо использовать анкерный рельеф, составляющий 25–30 % от глубины толщины сухой пленки всей системы покрытия. См. спецификации покрытий для рекомендованных производителем профилей глубины.
См. спецификации покрытий для рекомендованных производителем профилей глубины.
ЧАСТЬ II
РЕШЕНИЯ
Удаление соли
Чистая вода на чистой, плоской металлической поверхности не вызовет коррозии. Коррозионный элемент требует электролита, а соль – враг номер один.
Соль не только вытягивает влагу из атмосферы, но и при растворении в растворе, ее агрессивные ионы разрушают пассивирующий слой, обнажая металл, и полученный раствор электролита способствует ионному потоку, необходимому для образования коррозионных элементов.
Поэтому первая линия защиты от ржавчины – это удаление растворимых солей с поверхности.
Механические методы (ручной и электроинструмент, сухая абразивная обработка) оказались в значительной степени неэффективными при удалении солей. Но поскольку соли растворимы, предпочтительным методом является их растворение в воде.
Именно здесь отличные результаты демонстрирует гидроабразивная обработка. Водяная струя под давлением не только транспортирует абразив, но и растворяет соль и смывает ее.
Водяная струя под давлением не только транспортирует абразив, но и растворяет соль и смывает ее.
Азот на органической пассиваторной молекуле связывается с ионами FE. Углеводородная цепь блокирует кислород и хлорид от контакта с поверхностью железа.
Ингибиторы коррозии
Ингибиторы коррозии могут добавляться в сеть водоснабжения установки гидроабразивной обработки для предотвращения мгновенной ржавчины, но они также могут иметь нежелательные побочные эффекты.
Пассиваторы создают защитную пленку между поверхностью и окружающей средой. Органические молекулы, такие как амины, имеют свободные пары электронов, которые связываются с металлом, а также длинный углеводородный хвост для ингибирования адсорбции поступающих агрессивных ионов на поверхность металла.
Тем не менее, известно, что пассиваторы препятствуют адгезии покрытия и эффективности антикоррозионных грунтов, особенно содержащих цинк, которые должны входить в контакт с металлом для получения гальванизирующего эффекта.
Удалители соли имеют соответствующий химический состав для растворения солей. Эти растворы разрушают оксидный слой для непосредственного взаимодействия с металлом. Однако, если их не смывать, такие часто кислые добавки могут оставлять на поверхности нежелательные осадки, которые могут вызвать осмотическое вспучивание.
Поверхностно-активные вещества снижают поверхностное натяжение воды, делая ее «более влажной», что позволяет воде лучше проникать и растворять солевые отложения. Они также могут способствовать испарению и не оставляют никаких остаточных загрязнений на поверхности.
Существуетболее 200 разновидностей ингибиторов ржавчины. Многие покрытия не выдерживают их, не все являются экологически чистыми, а некоторые являются известными канцерогенами. Перед использованием ингибитора коррозии обратитесь за рекомендациями к производителю покрытия.
Правило № 1 – Как можно быстрее применяйте грунт.
Наиболее эффективным способом предотвращения ржавчины является нанесение в кратчайшие сроки грунта, указанного производителем покрытия.
Существуют влагостойкие грунты, которые можно наносить на влажную сталь. Грунты на основе цинка обеспечивают дополнительную защиту от ржавчины, образуя оцинкованное соединение с поверхностью.
Изучите технические характеристики покрытий производителя на предмет рекомендаций по грунту.
ЛУЧШИЕ МЕТОДЫ
Для получения наилучших результатов для защиты от ржавчины и адгезии покрытия следуйте этим методам:
- Используйте правильный анкерный рельеф.
- Оставляйте поверхность как можно более чистой.
- Осуществляйте абразивоструйную обработку в условиях низкой влажности.
- Наносите грунт как можно скорее.
- Работайте в соответствии с техническими условиями, предоставляемыми производителем покрытия.
Как предотвратить ржавчину
Сталь и железо — два самых полезных и распространенных материала.
Основное различие между железом и сталью заключается в том, что железо — это элемент (вспомните периодическую таблицу на уроке химии), а сталь — это соединение железа и углерода. Хотя чистое железо само по себе хрупкое, мы добавляем его к углероду, чтобы создать очень прочную и очень полезную сталь, из которой строятся многие наши повседневные ценные предметы, такие как уличная мебель, бытовая техника, велосипеды, автомобили, машины, мосты, железные дороги, здания. и даже вышки сотовой связи.
Хотя чистое железо само по себе хрупкое, мы добавляем его к углероду, чтобы создать очень прочную и очень полезную сталь, из которой строятся многие наши повседневные ценные предметы, такие как уличная мебель, бытовая техника, велосипеды, автомобили, машины, мосты, железные дороги, здания. и даже вышки сотовой связи.
Когда металлы, особенно сталь, не обрабатываются должным образом, они ржавеют. Ржавчину легко определить. Он красноватый или коричневатый и имеет шероховатую текстуру и может появиться на металлах через некоторое время. Ржавчина, однако, больше, чем бельмо на глазу. Он фактически разъедает металл понемногу, вызывая его разрушение и превращение в сухой порошок, нарушая целостность его структуры.
После того, как сталь подверглась коррозии и не поддается ремонту, она может быть чрезвычайно дорогой, и ее чрезвычайно трудно заменить. Поэтому мы, очевидно, хотим защитить его от ржавчины в первую очередь. Проблема решена, верно?
Предотвращение ржавчины начинается со знания того, как она начинается.
Ржавчина является результатом процесса окисления при соединении железа и кислорода. В основном это происходит, когда у вас есть агрессивная среда: соль, химикаты, кислоты, экстремальные температуры или перепады температур, влага, сырость и влажность. Они могут нанести ущерб металлу, особенно стали, вызывая его быстрое окисление и коррозию.
Теперь, когда мы лучше понимаем процесс коррозии, мы можем предотвратить его появление.
Основные способы защиты стали от ржавчины:Уменьшение повреждений. Устраните любые мелкие повреждения, такие как царапины и вмятины, до того, как влага попадет на металл.
Держите его сухим. Сохраняйте стальные изделия сухими, храня их вдали от дождя и влаги.
Раскрась. Окрашивая металл, вы можете создать барьер, который удерживает корродирующие элементы от незащищенной стали.
В то время как эти варианты являются быстрыми и простыми для небольших предметов домашнего обихода, они не совсем осуществимы для больших стальных предметов, которые необходимо обрабатывать элементами ежедневно в течение длительных периодов времени. Просто невозможно уследить за каждой царапиной, а постоянное повторное нанесение свежих слоев краски до появления ржавчины требует огромных затрат времени и средств.
Просто невозможно уследить за каждой царапиной, а постоянное повторное нанесение свежих слоев краски до появления ржавчины требует огромных затрат времени и средств.
Для более крупных проектов и структур решающее значение имеет долгосрочное решение.
Лучшим способом защиты от ржавчины является цинкование.Цинкование – это нанесение цинкового покрытия на сталь или железо для защиты от ржавчины или коррозии. Существует два типа:
Горячее цинкование производится на заводе-изготовителе. Это процесс погружения железа или стали в расплавленный цинк для создания защитного гальванического экзоскелета.
A Состав для холодного цинкования — это богатое цинком антикоррозионное покрытие, которое наносится как краска прямо из баллончика. Это более простой, удобный, но надежный процесс, чем горячее цинкование, которое можно выполнять на месте для предотвращения ржавчины всего проекта, а не только подкрашивания.
Продукты ZRC для холодного цинкования содержат 95% металлического цинка по весу в высушенной пленке после нанесения. Они признаны в рамках Компонентной программы Underwriter’s Laboratories, Inc. эквивалентом горячего цинкования. Это означает, что вы можете получить тот же уровень защиты, который обеспечивает процесс горячего цинкования погружением в легкость банки; отправлены вам для применения непосредственно на месте. Составы для холодного цинкования соответствуют тому же уровню федеральных спецификаций, что и продукты для горячего цинкования (DOD-P-21035A, формально MIL-P21035A).
Холоднооцинкованные компаунды могут спасти проект!
Если металл для проекта оказывается неоцинкованным, у вас есть два варианта: отправить его обратно производителю для горячего цинкования и иметь дело с длительными задержками завершения вашего проекта, или использовать высококачественный состав для холодного цинкования, который отвечает тем же требованиям и поддерживает ваш проект.
Хотя составы для холодного цинкования являются идеальным решением для предотвращения коррозии железа и стали, не все продукты одинаковы. Состав для холодного цинкования должен содержать достаточное количество цинка в высушенной пленке по весу — в негерметизирующей связующей системе — для обеспечения того же уровня защиты, что и при горячем цинковании. Узнайте больше о ZRC и смесях для холодного цинкования здесь.
Предотвратить ржавчину, пока не стало слишком поздноСталь и железо могут быть разными по своей природе, но и то, и другое необходимо обрабатывать, чтобы ржавчина не сокращала срок их службы. В конце концов, защита от ржавчины продлевает целостность металла, продлевает срок его службы и, в конечном итоге, экономит ваше время, деньги и нервы в долгосрочной перспективе.
6 способов предотвратить ржавление металлов
14 апреля 2021 г. 14 апреля 2021 г. | 9:49 утра
Ржавлением называют образование коричневатых частиц оксида железа на поверхности металлов, содержащих железо, которые вступают во взаимодействие с воздухом и водой. Эта форма коррозии чрезвычайно разрушительна и непривлекательна.
Эта форма коррозии чрезвычайно разрушительна и непривлекательна.
Наша металлическая продукция для ваших нужд Наша металлическая продукция для ваших нужд
Ржавчина возникает при контакте железных металлов с кислородом, который содержится в воде, соленой воде, кислотных и опасных веществах. Когда частицы оксида железа разлетаются с поверхности металла, они обнажают незатронутый слой молекул железа, что позволяет протекать реакции. Большие площади металлической ржавчины могли привести к тому, что весь металл образовался до фрагмента 9.0083 Черный металл — это тот, который содержит железо, которое может ржаветь. Обычные черные металлы, в том числе углеродистая сталь марки 1018 и 12L 14, легированная сталь марки 4130 и нержавеющая сталь марки 304, 316. Цветной металл, такой как алюминий и медь, имеет небольшое количество железа, которое обычно не ржавеет, но проходит через него. коррозия.
Вот несколько советов по предотвращению коррозии металлов.
- Выберите правильный тип металла в соответствии с его применением.
Основным преимуществом использования металлов, таких как нержавеющая сталь, дуплекс и супердуплекс, сплав никеля и 6% молибдена, является их коррозионная стойкость. Это самый простой способ избежать ржавчины металлов. Эти металлы изготовлены с более высокой способностью противостоять ржавчине. Эти металлы также не нуждаются в дополнительных мерах защиты. - Использование нержавеющей стали
Сплавы из нержавеющей стали содержат железо, устойчивое к коррозии, поскольку часто содержит большое количество хрома, который более устойчив, чем железо. Хром в сплаве легко окисляется, образуя прочное покрытие из оксида хрома на поверхности металла, предотвращая контакт кислорода со сталью. - Сохранение металла в сухости и чистоте
Когда дело доходит до ржавчины, наибольшую опасность представляет вода, поскольку кислород в молекулах воды связывается с железом с образованием оксида железа.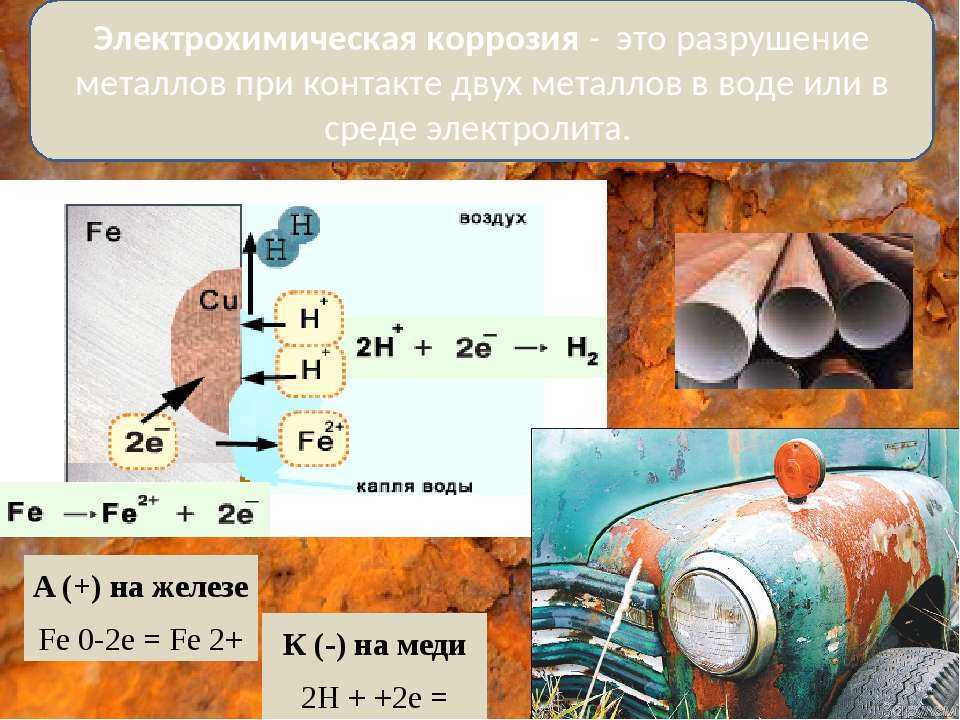 В результате металлы, оставленные снаружи, такие как транспортные средства, ворота или резервуары, более подвержены коррозии. Поскольку любая грязь или гравий, прилипшие к поверхности, будут задерживать воду, важно содержать металлы в чистоте. Установка осушителя отлично подойдет для помещений с повышенной влажностью.
В результате металлы, оставленные снаружи, такие как транспортные средства, ворота или резервуары, более подвержены коррозии. Поскольку любая грязь или гравий, прилипшие к поверхности, будут задерживать воду, важно содержать металлы в чистоте. Установка осушителя отлично подойдет для помещений с повышенной влажностью. - Предотвращение появления царапин на металлической поверхности.
Царапины или отверстия на стали обнажают больше металла и задерживают воду, заставляя ее оставаться в контакте с железом. Вот почему холоднокатаная сталь более устойчива к ржавчине, чем горячекатаная; холодная прокатка дает более чистую поверхность без текстуры, которая может задерживать и удерживать воду. - Ингибиторы коррозии
Это химические вещества, которые реагируют на металлическую поверхность, связанную с газами, которые реагируют на электрохимические реакции, приводящие к коррозии. Методы дисперсии можно использовать в качестве растворителя или защитной изоляции. Механизм, известный как пассивация, обычно используется для использования ингибиторов коррозии.
Механизм, известный как пассивация, обычно используется для использования ингибиторов коррозии. - Защитные покрытия
Ржавление металлов можно предотвратить путем нанесения слоя защитных красок. Окрашивание металлической поверхности может служить в качестве щита, предотвращая передачу электрических и химических зарядов коррозионному веществу и металлу под ним. Другой способ избежать ржавчины — нанесение порошкового покрытия для очистки металлической поверхности. Металл нагревают, чтобы связать порошок в гладкий непрерывный слой, который работает как коррозионно-стойкий щит. Можно использовать следующие порошкообразные композиции: акрил, полиэстер, нейлон и т. д.
Погружение металлических деталей в вороненые растворы кислот, гидроксида натрия и нитрата калия обеспечивает превосходную коррозионную стойкость. Средства или спреи для защиты от ржавчины, такие как аэрозольные спреи или тканевые салфетки.
Наша металлическая продукция для ваших нужд Наша металлическая продукция для ваших нужд
Piping Mart
Pipingmart – это портал B2B, специализирующийся на промышленных, металлических и трубопроводных изделиях.
