Катализатор | это… Что такое Катализатор?
У этого термина существуют и другие значения, см. Катализатор (значения).
Схема протекания реакции с катализатором
Катализа́тор — химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции[1]. Количество катализатора, в отличие от реагентов, после реакции не изменяется. Важно понимать, что катализатор не участвует в реакции. Они обеспечивают более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно повторяется.
Содержание
|
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO [1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции [2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Основная статья: Каталитический конвертер
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счёт неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.
 [4]
[4]
Источники
- ↑ 1 2 3 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru. Архивировано из первоисточника 25 августа 2011.
См. также
- Ингибитор
- Ферментативный ингибитор
- Активатор (катализ)
- Энергия активации
- Катализ
Ссылки
Катализатор | это.
 .. Что такое Катализатор?
.. Что такое Катализатор?У этого термина существуют и другие значения, см. Катализатор (значения).
Схема протекания реакции с катализатором
Катализа́тор — химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции[1]
Содержание
|
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO [1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции [2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Основная статья: Каталитический конвертер
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счёт неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.
 [4]
[4]
Источники
- ↑ 1 2 3 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru. Архивировано из первоисточника 25 августа 2011.
См. также
- Ингибитор
- Ферментативный ингибитор
- Активатор (катализ)
- Энергия активации
- Катализ
Ссылки
Катализатор | это.
 .. Что такое Катализатор?
.. Что такое Катализатор?У этого термина существуют и другие значения, см. Катализатор (значения).
Схема протекания реакции с катализатором
Катализа́тор — химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции[1]. Количество катализатора, в отличие от реагентов, после реакции не изменяется. Важно понимать, что катализатор не участвует в реакции. Они обеспечивают более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно повторяется.
Содержание
|
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO [1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции [2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Основная статья: Каталитический конвертер
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счёт неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.

Источники
- ↑ 1 2 3 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru. Архивировано из первоисточника 25 августа 2011.
См. также
- Ингибитор
- Ферментативный ингибитор
- Активатор (катализ)
- Энергия активации
- Катализ
Ссылки
Катализатор | это.
 .. Что такое Катализатор?
.. Что такое Катализатор?У этого термина существуют и другие значения, см. Катализатор (значения).
Схема протекания реакции с катализатором
Катализа́тор — химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции[1]. Количество катализатора, в отличие от реагентов, после реакции не изменяется. Важно понимать, что катализатор не участвует в реакции. Они обеспечивают более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно повторяется.
Содержание
|
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO [1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции [2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Основная статья: Каталитический конвертер
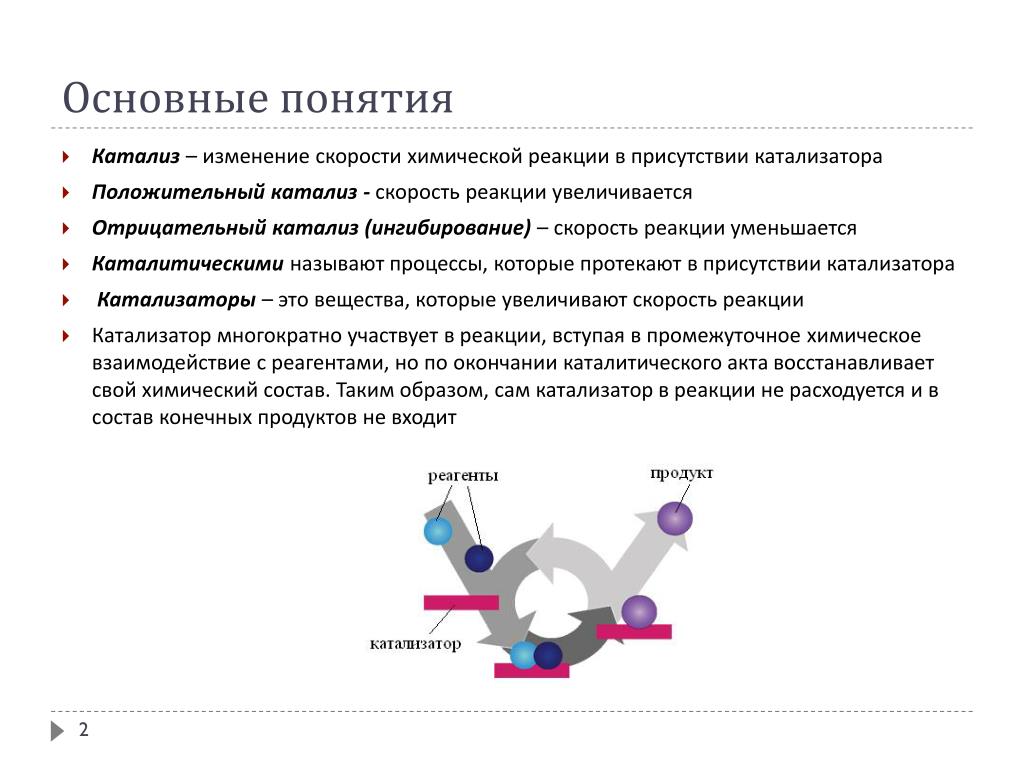
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счёт неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.
 [4]
[4]
Источники
- ↑ 1 2 3 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru. Архивировано из первоисточника 25 августа 2011.
См. также
- Ингибитор
- Ферментативный ингибитор
- Активатор (катализ)
- Энергия активации
- Катализ
Ссылки
Катализаторы | это.
 .. Что такое Катализаторы?
.. Что такое Катализаторы?Катализа́тор — вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции (Химическая энциклопедия). Количество катализатора, в отличие от других реагентов, при реакции не изменяется. Обеспечивая более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно (сотни, миллионы раз) повторяется.
Содержание
|
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный – образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества (Химическая энциклопедия). Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO (Химическая энциклопедия).
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-востановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции (Имянитов, Temkin). Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
На дороги ежедневно выезжают миллионы автомобилей, и каждый из них — источник загрязнения воздуха. Особенно это чувствуется в крупных городах, где выхлопные газы автомобилей могут создавать большие проблемы.
В современных автомашинах присутствует каталитический преобразователь или автомобильный катализатор. Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счет неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.[1]
Источники
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru.
Литература
- Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443 — 1454. — 0132-344X.

- Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
Ссылки
- Сайт про автомобильный катализатор и глушитель
- всё про аVтокатализатор и глушитель на сайте аVтокатализатор.ru
См. также
- Ингибитор
- Ферментативный ингибитор
- Активатор (катализ)
- Энергия активации
- Катализ
Катализаторы и ферменты • Джеймс Трефил, энциклопедия «Двести законов мироздания»
200 законов мироздания > Химия
Катализатором, или ферментом (в случае биохимической реакции), называется вещество, помогающее протеканию химической реакции, но не изменяющееся в ходе нее.
Скорость протекания химической реакции можно значительно увеличить, если добавить вещество, которое участвует в этой реакции, но при этом само не расходуется. Чтобы лучше это понять, представим себе работу брокера по операциям с недвижимостью. Брокер находит и собирает вместе людей, желающих продать какое-либо имущество, и людей, желающих его купить, таким образом способствуя его продаже и передаче другому владельцу. При этом сам брокер в ходе сделки ничего реально не покупает и не продает. Так же и катализатор, или фермент, способствует протеканию реакции между двумя веществами, но к концу реакции остается в первоначальном виде.
Чтобы лучше это понять, представим себе работу брокера по операциям с недвижимостью. Брокер находит и собирает вместе людей, желающих продать какое-либо имущество, и людей, желающих его купить, таким образом способствуя его продаже и передаче другому владельцу. При этом сам брокер в ходе сделки ничего реально не покупает и не продает. Так же и катализатор, или фермент, способствует протеканию реакции между двумя веществами, но к концу реакции остается в первоначальном виде.
Подалуй, самый известный катализатор находится у нас в машине, в каталитическом нейтрализаторе отработавших газов. Он представляет собой мелкоячеистую металлическую сетку, сделанную из палладия и платины, через которую пропускаются выхлопы из автомобильного двигателя. Эти металлы катализируют ряд химических взаимодействий. Во-первых, они абсорбируют окись углерода (CO), окись азота (NO) и кислород, причем каждая молекула NO распадается на составляющие ее атомы. CO соединяется с атомом кислорода, образуя диоксид углерода, а атомы азота соединяются, и получаются молекулы азота. В то же время избыток кислорода дает возможность углеводородам, не до конца сгоревшим в автомобильных цилиндрах, полностью окислиться до диоксида углерода и воды. Вот так выхлопные газы, которые содержат окись углерода (смертельный яд) и вещества, приводящие к кислотным дождям, а также несгоревшие фрагменты исходных молекул бензина, превращаются в относительно безвредную смесь диоксида углерода, азота и воды.
В то же время избыток кислорода дает возможность углеводородам, не до конца сгоревшим в автомобильных цилиндрах, полностью окислиться до диоксида углерода и воды. Вот так выхлопные газы, которые содержат окись углерода (смертельный яд) и вещества, приводящие к кислотным дождям, а также несгоревшие фрагменты исходных молекул бензина, превращаются в относительно безвредную смесь диоксида углерода, азота и воды.
Чтобы понять действие ферментов, необходимо знать, что для взаимодействия сложных органических молекул недостаточно их простого контакта. Чтобы реакция протекала, определенные атомы в сближающихся молекулах должны быть правильно сориентированы друг относительно друга (так же как ключ определенным образом должен быть вставлен в замок), только тогда смогут образоваться химические связи. То есть для химических процессов, протекающих в биологических системах (см. Биологические молекулы), чрезвычайно важную роль играет пространственная геометрия.
В биохимии крайне мала вероятность того, что две сложные молекулы, предоставленные сами себе, случайно окажутся друг относительно друга в правильной ориентации, необходимой для взаимодействия. Чтобы такая реакция протекала с ощутимой скоростью, нужна помощь молекул определенного типа — ферментов. Фермент притягивает к себе две другие молекулы и удерживает их в правильном положении, чтобы взаимодействие состоялось. Как только реакция произошла, фермент освобождается и повторяет те же действия с другим набором молекул. Все ферменты в биологических системах представляют собой белки, которые могут принимать разнообразные сложные формы. Как и все белки, они закодированы в ДНК и в качестве ферментов управляют скоростью протекания химических реакций.
Чтобы такая реакция протекала с ощутимой скоростью, нужна помощь молекул определенного типа — ферментов. Фермент притягивает к себе две другие молекулы и удерживает их в правильном положении, чтобы взаимодействие состоялось. Как только реакция произошла, фермент освобождается и повторяет те же действия с другим набором молекул. Все ферменты в биологических системах представляют собой белки, которые могут принимать разнообразные сложные формы. Как и все белки, они закодированы в ДНК и в качестве ферментов управляют скоростью протекания химических реакций.
См. также:
1930-е | Химические связи |
6
Показать комментарии (6)
Свернуть комментарии (6)
Флогистон 02.12.2005 08:21 Ответить
Если это сайт для ученых, а не для школьников, то и определения должны
быть не списаны из школьных учебников!
Например, первая строчка «Катализатором, или ферментом (в случае биохимической реакции), называется вещество, помогающее протеканию химической реакции, но не изменяющееся в ходе нее. «
«
Но почему же не так: «Катализатором называется вещество, способствующее увеличению скорости химической реакции путем снижения энергии активационного барьера, и тем самым обеспечивающее более быстрое достижение состояния термодинамического равновесия. Как правило, катализатор не претерпевает химических превращений в ходе химической реакции. Ферменты или биокатализаторы — это вещества белковой природы, катализирующие биохимические реакции. В отличи от небелковых катализаторов ферменты (энзимы) крайне реакционно-специфические катализаторы, т.е. фермент способен катализировать лишь очень небольшое число реакций, часто только одну.Ответить
algen Флогистон 02.12.2005 11:23 Ответить
Вообще-то, сайт для всех. Для ученых одни разделы, для школьников — другие. Энциклопедия — это базовый научно-популярный материал для начинающих.
 А для ученых есть разделы «Научный календарь», «Наука и право», «Научные блоги». Раздел «Библиотека» — тоже интересен для ученых, хотя там научно-популярные статьи. И новости науки тоже зачастую довольно глубокие.
А для ученых есть разделы «Научный календарь», «Наука и право», «Научные блоги». Раздел «Библиотека» — тоже интересен для ученых, хотя там научно-популярные статьи. И новости науки тоже зачастую довольно глубокие.Но все же не стоит путать научность с наукообразием. Вовсе не в том цель, чтобы каждое объяснение было фундаментальным. Обычно гораздо важнее, чтобы оно было понятным.
Ответить
Флогистон algen 02.12.2005 12:14 Ответить
Спасибо за информацию! Полезу в соответствующий раздел.
Но по поводу «Обычно гораздо важнее, чтобы оно было понятным» позвольте не согласиться — гораздо важнее, что бы объяснение было правильным и не грешило двусмысленностью.Ответить
algen Флогистон 02.12.2005 13:01 Ответить
Какова ценность точного объяснения, если оно осталось непонятым? Человеческое понимание устроено так, что сразу воспринять предельно точные формулировки трудно.
 Поэтому сначала обычно дается некая неточная, но наводящая на правильные представления мысль. Потом, по мере того, как у человека накапливается опыт, а практика показывает недостаточность упрощенного объяснения, появляется нужда в уточнении. Главное, что читатель в этот момент готов к восприятию более точного понятия, он правильно поймет и оценит все тонкости формулировки. А если дать такое объяснение раньше времени, то возникнет ощущение сумбура и человек ничего не поймет и не запомнит.
Поэтому сначала обычно дается некая неточная, но наводящая на правильные представления мысль. Потом, по мере того, как у человека накапливается опыт, а практика показывает недостаточность упрощенного объяснения, появляется нужда в уточнении. Главное, что читатель в этот момент готов к восприятию более точного понятия, он правильно поймет и оценит все тонкости формулировки. А если дать такое объяснение раньше времени, то возникнет ощущение сумбура и человек ничего не поймет и не запомнит.Ответить
Флогистон algen 02.12.2005 13:41 Ответить
Я преподаватель ВУЗа с немалым стажем, точная формулировка с последующим объяснением — это лучшее, что может дать учитель ученику. А Ваш подход — он повсеместно реализован в наших школах. И детишек потом приходится переучивать, предлагая забыть «..некая неточная, но наводящая на правильные представления мысль..», поскольку неподготовленый человек никогда не будет заниматься обдумыванием и додумыванием самостоятельно, и запоминать сразу точное и, главное, правильное определение.
 В итоге имеет место колоссальный разрыв между школой и ВУЗом, из-за которого вчерашние отличники превращаются в неуспевающих студентов. Специфика любого научного знания — это чистая, незамутненная мысль, и к этому нужно готовить сразу, а не потом.
В итоге имеет место колоссальный разрыв между школой и ВУЗом, из-за которого вчерашние отличники превращаются в неуспевающих студентов. Специфика любого научного знания — это чистая, незамутненная мысль, и к этому нужно готовить сразу, а не потом.
И с чего это Вы взяли, что «Человеческое понимание устроено так, что сразу воспринять предельно точные формулировки трудно»? То что есть естественники и гуманитарии — это давно известно, но Ваш сайт не на школьников-гуманитариев ориентирован я надеюсь 🙂Ответить
alexsmail Флогистон 16.09.2006 18:51 Ответить
Как выпускник гимназии с углубленным изучением математики, физики и английского, а также как выпускнив ВУЗа (за рубежом) по математике и компьютерным наукам позвольте с вами не согласиться. Когда слышишь первый раз определение хочется услышать именно «..некая неточная, но наводящая на правильные представления мысль.
 .». Затем можно привести несколько примеров, показывающие недостатки данного определния и дать правильное, точно определение. С лекции студент должен уйти именно с неточным определением и чётким предствалением, какие у него есть изъяны. Затем, дома или перед сессией, студент выучит точное определение.
.». Затем можно привести несколько примеров, показывающие недостатки данного определния и дать правильное, точно определение. С лекции студент должен уйти именно с неточным определением и чётким предствалением, какие у него есть изъяны. Затем, дома или перед сессией, студент выучит точное определение.
В школе же нужно говорить правильные вещи. Например, говорить, что «квадратное уравнение с отрицательной дискриминантой не имеет решения» не верно. Нужно говорить «квадратное уравнение с отрицательной дискриминантой не имеет решения в действительных числах». И не важно, что дать вразумительный ответ школьнику, почему эта оговорка важна, сложно, я бы сказал не возможно, ведь он других чисел не знает, поэтому даже дача абсолютно точного определения действительного числа не поможет. Если этого не делать, то школьник, столкнувший с комплексными, числами испытает шок, он будет считать, что его обманывали.Ответить
Написать комментарий
1854 | Катализаторы и ферменты |
1937 | Гликолиз и дыхание |
начало 1950-х | Белки |
1953 | ДНК |
1925
Квантовая механика
1981
Инфляционная стадия расширения Вселенной
Новостная рассылка
«Элементы» в соцсетях:
Объяснитель: Что такое катализатор?
Катализаторы — невоспетые герои химических реакций, которые заставляют человеческое общество двигаться. Катализатор – это некий материал, который ускоряет химические реакции. С помощью катализатора молекулы, на взаимодействие которых могли уйти годы, теперь могут сделать это за секунды.
Катализатор – это некий материал, который ускоряет химические реакции. С помощью катализатора молекулы, на взаимодействие которых могли уйти годы, теперь могут сделать это за секунды.
Заводы полагаются на катализаторы, чтобы производить все, от пластика до лекарств. Катализаторы помогают перерабатывать нефть и уголь в жидкое топливо. Они являются ключевыми игроками в технологиях экологически чистой энергии. Природные катализаторы в организме, известные как ферменты, играют важную роль в пищеварении и многом другом.
Во время любой химической реакции молекулы разрывают химические связи между своими атомами. Атомы также образуют новые связи с другими атомами. Это как поменяться партнерами на кадриль. Иногда такое партнерство легко разорвать. Молекула может обладать определенными свойствами, которые позволяют ей переманивать атомы из другой молекулы. Но в стабильных партнерских отношениях молекулы довольны такими, какие они есть. Оставшись вместе в течение очень длительного периода времени, некоторые из них могут в конечном итоге поменяться партнерами. Но нет массового безумия разрыва и восстановления связей.
Но нет массового безумия разрыва и восстановления связей.
Катализаторы делают такое разрушение и восстановление более эффективным. Они делают это, снижая энергию активации для химической реакции. Энергия активации – это количество энергии, необходимое для протекания химической реакции. Катализатор просто меняет путь к новому химическому партнерству. Он строит эквивалент шоссе с твердым покрытием, чтобы объехать ухабистую грунтовую дорогу. Однако катализатор не расходуется в реакции. Подобно ведомому, он побуждает другие молекулы к реакции. Как только они это сделают, он кланяется.
Педагоги и родители, подпишитесь на шпаргалку
Еженедельные обновления, которые помогут вам использовать Science News Explores в учебной среде
Спасибо за регистрацию!
При регистрации возникла проблема.
Ферменты — это естественные биологические катализаторы. Они играют роль во всем, от копирования генетического материала до расщепления пищи и питательных веществ. Производители часто создают катализаторы для ускорения процессов в промышленности.
Производители часто создают катализаторы для ускорения процессов в промышленности.
Одной из технологий, для работы которой требуется катализатор, является водородный топливный элемент. В этих устройствах газообразный водород (H 2 ) реагирует с газообразным кислородом (O 2 ) с образованием воды (H 2 O) и электричества. Эти системы можно найти в водородном транспортном средстве, где они вырабатывают электричество для питания двигателя. Топливный элемент должен разделить атомы в молекулах водорода и кислорода, чтобы эти атомы могли перетасовываться для создания новых молекул (воды). Однако без посторонней помощи эта перетасовка происходила бы очень медленно. Таким образом, топливный элемент использует катализатор — платину — для запуска этих реакций.
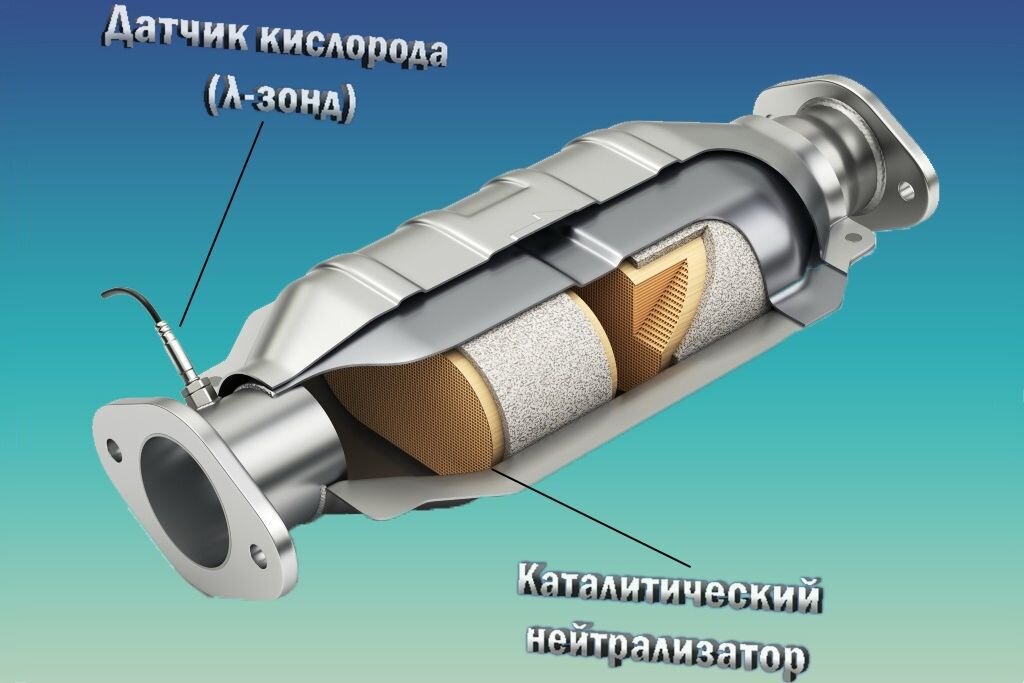
В современных автомобилях используется каталитический нейтрализатор, подобный показанному здесь в разрезе. Такие устройства помогают расщеплять выхлопные газы на химические вещества (например, воду), менее токсичные для окружающей среды. Поверхность платины притягивает молекулы газа. По сути, он притягивает их ближе друг к другу, так что поощряет — ускоряет — их реакцию. Затем он позволяет своим творениям свободно плавать.
Поверхность платины притягивает молекулы газа. По сути, он притягивает их ближе друг к другу, так что поощряет — ускоряет — их реакцию. Затем он позволяет своим творениям свободно плавать.В течение многих лет другие технологии также полагались на платиновые катализаторы. Например, для удаления вредных загрязняющих веществ из выхлопных газов автомобили теперь используют каталитические нейтрализаторы .
Но у платины есть и недостатки. Это дорого, например. (Людям нравится использовать его в модных украшениях.) И его нелегко получить.
Некоторые другие катализаторы получили статус суперзвезд. К ним относятся металлы с химическими свойствами, подобными платине. Среди них палладий и иридий. Однако, как и платина, оба они дороги и труднодоступны. Вот почему ведется поиск менее дорогих катализаторов для использования в топливных элементах.
Некоторые ученые считают, что молекулы углерода могут работать. Они, безусловно, были бы менее дорогостоящими и легко доступными. Другим вариантом может быть использование ферментов, подобных тем, которые находятся внутри живых существ.
Другим вариантом может быть использование ферментов, подобных тем, которые находятся внутри живых существ.
Силовые слова
Подробнее о сильных словахэнергия активации (в химии) Минимальная энергия, необходимая для протекания конкретной химической реакции.
атом Основная единица химического элемента. Атомы состоят из плотного ядра, содержащего положительно заряженные протоны и нейтрально заряженные нейтроны. Вокруг ядра вращается облако отрицательно заряженных электронов.
связь (в химии) Полупостоянное соединение между атомами или группами атомов в молекуле. Он формируется силой притяжения между участвующими атомами. После соединения атомы будут работать как единое целое. Чтобы разделить атомы компонентов, к молекуле должна быть подведена энергия в виде тепла или другого вида излучения.
углерод Химический элемент с атомным номером 6. Является физической основой всей жизни на Земле. Углерод существует свободно в виде графита и алмаза. Он является важной частью угля, известняка и нефти и способен к самосвязыванию химическим путем с образованием огромного количества химически, биологически и коммерчески важных молекул.
Является физической основой всей жизни на Земле. Углерод существует свободно в виде графита и алмаза. Он является важной частью угля, известняка и нефти и способен к самосвязыванию химическим путем с образованием огромного количества химически, биологически и коммерчески важных молекул.
катализатор Вещество, ускоряющее протекание химической реакции. Примеры включают ферменты и элементы, такие как платина и иридий.
каталитический нейтрализатор Устройство из керамических конструкций в форме сот, которое надевается на выхлопную трубу автомобиля. Когда выхлопные газы проходят через него, они сталкиваются с двумя разными типами катализаторов, каждый из которых может способствовать разным типам химической реакции. Один или несколько металлов, обычно платина, родий, палладий, а иногда даже золото, покрывают внутреннюю часть системы. Все стенки сотовой структуры устройства значительно увеличивают площадь покрытых катализатором поверхностей, которые теперь доступны для взаимодействия с выхлопными газами. Когда газы двигателя попадают на эти покрытые металлом поверхности, они разрушают загрязняющие вещества, превращая их в менее вредные материалы. Датчик в нейтрализаторе также измеряет количество кислорода в выхлопных газах. Если он находит слишком много, он сообщает компьютеру отрегулировать соотношение воздуха и топлива в двигателе, чтобы он сгорал более чисто.
Когда газы двигателя попадают на эти покрытые металлом поверхности, они разрушают загрязняющие вещества, превращая их в менее вредные материалы. Датчик в нейтрализаторе также измеряет количество кислорода в выхлопных газах. Если он находит слишком много, он сообщает компьютеру отрегулировать соотношение воздуха и топлива в двигателе, чтобы он сгорал более чисто.
химический Вещество, состоящее из двух или более атомов, которые объединяются (связываются вместе) в фиксированной пропорции и структуре. Например, вода — это химическое вещество, состоящее из двух атомов водорода, связанных с одним атомом кислорода. Его химический символ — H 2 O. Химический также может быть прилагательным, описывающим свойства материалов, которые являются результатом различных реакций между различными соединениями.
химические связи Силы притяжения между атомами, достаточно сильные для того, чтобы связанные элементы функционировали как единое целое.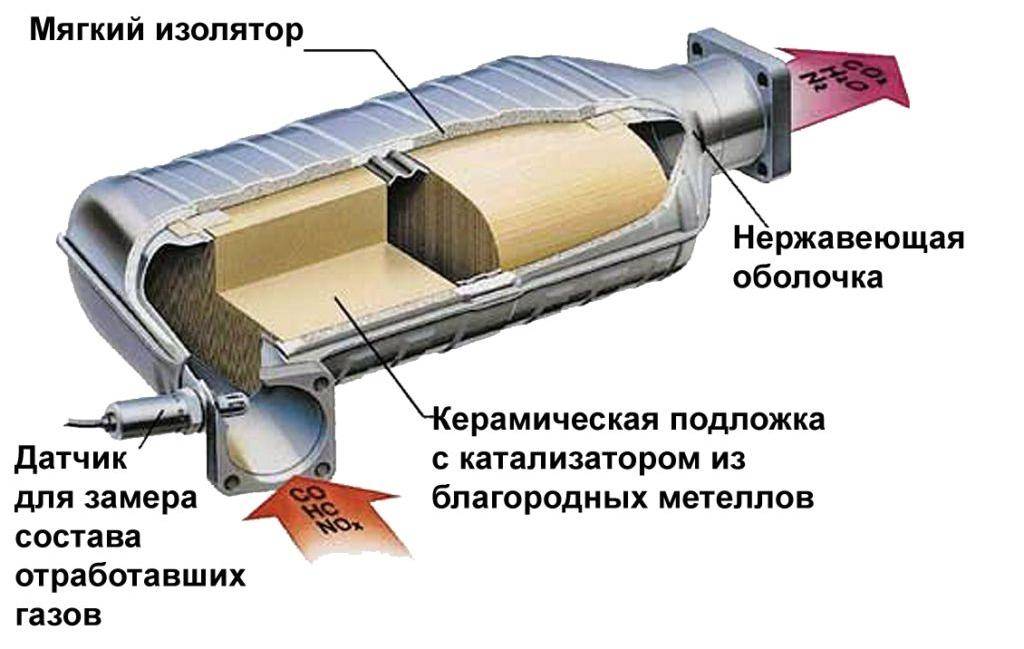 Некоторые из сил притяжения слабы, некоторые очень сильны. Все связи, по-видимому, связывают атомы посредством совместного использования — или попытки поделиться — электронами.
Некоторые из сил притяжения слабы, некоторые очень сильны. Все связи, по-видимому, связывают атомы посредством совместного использования — или попытки поделиться — электронами.
химическая реакция Процесс, включающий перестройку молекул или структуры вещества в отличие от изменения физической формы (например, из твердого состояния в газообразное).
электричество Поток заряда, обычно возникающий в результате движения отрицательно заряженных частиц, называемых электронами.
двигатель Машина, предназначенная для преобразования энергии в полезное механическое движение. Иногда двигатель называют мотором.
ферменты Молекулы, созданные живыми существами для ускорения химических реакций.
выхлоп (в машиностроении) Газы и мелкие частицы, выбрасываемые — часто с высокой скоростью и/или давлением — при сгорании (горении) или нагревании воздуха. Выхлопные газы обычно представляют собой отходы.
Выхлопные газы обычно представляют собой отходы.
топливный элемент Устройство, преобразующее химическую энергию в электрическую. Наиболее распространенным топливом является водород, который выделяет в качестве побочного продукта только водяной пар.
генетический Относится к хромосомам, ДНК и генам, содержащимся в ДНК. Область науки, занимающаяся этими биологическими инструкциями, известна как генетика. Люди, которые работают в этой области, являются генетиками.
водород Самый легкий элемент во Вселенной. В виде газа он бесцветен, не имеет запаха и легко воспламеняется. Это неотъемлемая часть многих видов топлива, жиров и химических веществ, из которых состоят живые ткани.
иридий Обнаруженный в 1803 году, его название происходит от латинского слова «радуга». Это твердый, хрупкий и устойчивый к коррозии металл из семейства платиновых. Слегка желтоватый, этот элемент в основном используется в качестве отвердителя для платины. Действительно, его температура плавления превышает 2400° по Цельсию (4350° по Фаренгейту). Атомный номер элемента — 77.
Слегка желтоватый, этот элемент в основном используется в качестве отвердителя для платины. Действительно, его температура плавления превышает 2400° по Цельсию (4350° по Фаренгейту). Атомный номер элемента — 77.
производство Изготовление вещей, обычно в больших масштабах.
металл Что-то, что хорошо проводит электричество, имеет тенденцию быть блестящим (отражающим) и податливым (это означает, что ему можно придать форму с помощью тепла, а не слишком большого усилия или давления).
молекула Электрически нейтральная группа атомов, представляющая минимально возможное количество химического соединения. Молекулы могут состоять из атомов одного или разных типов. Например, кислород в воздухе состоит из двух атомов кислорода (O 2 ), но вода состоит из двух атомов водорода и одного атома кислорода (H 2 O).
питательное вещество Витамины, минералы, жиры, углеводы или белки, которые необходимы растению, животному или другому организму в составе пищи для выживания.
кислород Газ, составляющий около 21 процента атмосферы. Все животные и многие микроорганизмы нуждаются в кислороде для подпитки своего метаболизма.
палладий Мягкий, пластичный, стальной белый, устойчивый к потускнению металлический элемент, встречающийся в природе с платиной, особенно в золотых, никелевых и медных рудах.
нефть Густая горючая жидкая смесь углеводородов. Нефть — это ископаемое топливо, которое в основном находится под поверхностью Земли. Это источник химических веществ, используемых для производства бензина, смазочных масел, пластмасс и многих других продуктов.
пластик Любой из серии легко деформируемых материалов; или синтетические материалы, изготовленные из полимеров (длинных цепочек молекул из строительных блоков), которые имеют тенденцию быть легкими, недорогими и устойчивыми к деградации.
платина Природный серебристо-белый металлический элемент, который остается стабильным (не подвергается коррозии) на воздухе. Он используется в ювелирных изделиях, электронике, химической обработке и некоторых зубных коронках.
Он используется в ювелирных изделиях, электронике, химической обработке и некоторых зубных коронках.
загрязнитель Вещество, которое загрязняет что-либо, например воздух, воду, наши тела или продукты. Некоторые загрязняющие вещества представляют собой химические вещества, такие как пестициды. Другие могут быть излучением, включая избыточное тепло или свет. Даже сорняки и другие инвазивные виды можно считать одним из видов биологического загрязнения.
14.7: Катализ — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 25181
Цели обучения
- Понять, как катализаторы увеличивают скорость реакции и селективность химических реакций.

Катализаторы – это вещества, которые увеличивают скорость химической реакции, не расходуясь в процессе. Катализатор, таким образом, не входит в общую стехиометрию реакции, которую он катализирует, но он должен присутствовать хотя бы в одной из элементарных реакций механизма катализируемой реакции. Катализированный путь имеет более низкую E a , но чистое изменение энергии в результате реакции (разница между энергией реагентов и энергией продуктов) не зависит от присутствия катализатора ( Рисунок \(\PageIndex{1}\)). Тем не менее, из-за его более низкой E a скорость катализируемой реакции выше, чем скорость некаталитической реакции при той же температуре. Поскольку катализатор снижает высоту энергетического барьера, его присутствие увеличивает скорость как прямой, так и обратной реакции на одинаковую величину. В этом разделе мы рассмотрим три основных класса катализаторов: гетерогенные катализаторы, гомогенные катализаторы и ферменты.
Катализатор влияет на E a , а не на Δ E .
Гетерогенный катализ
В гетерогенном катализе катализатор находится в другой фазе, чем реагенты. По крайней мере, один из реагентов взаимодействует с твердой поверхностью в физическом процессе, называемом адсорбцией, таким образом, что химическая связь в реагенте становится слабой, а затем разрывается. Яды — это вещества, которые необратимо связываются с катализаторами, препятствуя адсорбции реагентов и, таким образом, снижая или разрушая эффективность катализатора.
Примером гетерогенного катализа является взаимодействие газообразного водорода с поверхностью металла, такого как Ni, Pd или Pt. Как показано в части (а) на рисунке \(\PageIndex{2}\), связи водород-водород разрываются и образуются отдельные адсорбированные атомы водорода на поверхности металла. Поскольку адсорбированные атомы могут перемещаться по поверхности, два атома водорода могут столкнуться и образовать молекулу газообразного водорода, которая затем может покинуть поверхность в обратном процессе, называемом десорбцией. Адсорбированные атомы H на поверхности металла значительно более реакционноспособны, чем молекула водорода. Поскольку относительно прочная связь H–H (энергия диссоциации = 432 кДж/моль) уже разорвана, энергетический барьер для большинства реакций H 2 находится значительно ниже на поверхности катализатора.
Рисунок \(\PageIndex{2}\): Гидрирование этилена на гетерогенном катализаторе. Когда молекула водорода адсорбируется на поверхности катализатора, связь Н–Н разрывается и образуются новые связи М–Н. Отдельные атомы H более реакционноспособны, чем газообразные H 2 . Когда молекула этилена взаимодействует с поверхностью катализатора, она взаимодействует с атомами водорода в ступенчатом процессе с образованием этана, который высвобождается. (CC BY-NC-SA; анонимно)
Отдельные атомы H более реакционноспособны, чем газообразные H 2 . Когда молекула этилена взаимодействует с поверхностью катализатора, она взаимодействует с атомами водорода в ступенчатом процессе с образованием этана, который высвобождается. (CC BY-NC-SA; анонимно)На рисунке \(\PageIndex{2}\) показан процесс, называемый гидрированием , в котором атомы водорода добавляются к двойной связи алкена, такого как этилен, с получением продукта, содержащего одинарные связи C–C, в в данном случае этан. Гидрогенизация используется в пищевой промышленности для превращения растительных масел, состоящих из длинных цепей алкенов, в более коммерчески ценные твердые производные, содержащие алкильные цепи. Гидрогенизация некоторых двойных связей в полиненасыщенных растительных маслах, например, дает маргарин, продукт с температурой плавления, текстурой и другими физическими свойствами, подобными свойствам сливочного масла.
Несколько важных примеров промышленных гетерогенных каталитических реакций приведены в таблице \(\PageIndex{1}\). Хотя механизмы этих реакций значительно сложнее, чем описанная здесь простая реакция гидрирования, все они включают адсорбцию реагентов на твердой каталитической поверхности, химическую реакцию адсорбированных частиц (иногда через ряд промежуточных частиц) и, наконец, десорбцию. продуктов с поверхности.
Хотя механизмы этих реакций значительно сложнее, чем описанная здесь простая реакция гидрирования, все они включают адсорбцию реагентов на твердой каталитической поверхности, химическую реакцию адсорбированных частиц (иногда через ряд промежуточных частиц) и, наконец, десорбцию. продуктов с поверхности.
| Коммерческий процесс | Катализатор | Начальная реакция | Конечный коммерческий продукт |
|---|---|---|---|
| контактный процесс | В 2 О 5 или Pt | 2SO 2 + O 2 → 2SO 3 | Н 2 SO 4 |
| Процесс Габера | Fe, K 2 O, Al 2 O 3 | N 2 + 3H 2 → 2NH 3 | НХ 3 |
| Процесс Оствальда | Pt и Rh | 4NH 3 + 5O 2 → 4NO + 6H 2 O | HNO 3 |
| реакция конверсии вода-газ | Fe, Cr 2 O 3 или Cu | CO + H 2 O → CO 2 + H 2 | H 2 для NH 3 , CH 3 OH и других видов топлива |
| паровой риформинг | Ni | CH 4 + H 2 O → CO + 3H 2 | Ч 2 |
| синтез метанола | ZnO и Cr 2 O 3 | CO + 2H 2 → CH 3 OH | CH 3 OH |
| Процесс Сохио | фосфомолибдат висмута | \(\ mathrm{CH}_2\textrm{=CHCH}_3+\mathrm{NH_3}+\mathrm{\frac{3}{2}O_2}\стрелка вправо\mathrm{CH_2}\textrm{=CHCN}+\ матрм{3H_2O}\) | \(\underset{\textrm{акрилонитрил}}{\mathrm{CH_2}\textrm{=CHCN}}\) |
| каталитическое гидрирование | Ni, Pd или Pt | RCH=CHR’ + h3 → RCH 2 -CH 2 R’ | частично гидрогенизированные масла для маргарина и т. д. д. |
Гомогенный катализ
В гомогенном катализе катализатор находится в той же фазе, что и реагент(ы). Количество столкновений между реагентами и катализатором максимально, потому что катализатор равномерно распределен по всей реакционной смеси. Многие гомогенные катализаторы в промышленности представляют собой соединения переходных металлов (таблица \(\PageIndex{2}\)), но извлечение этих дорогостоящих катализаторов из раствора представляет собой серьезную проблему. В качестве дополнительного препятствия для их широкого коммерческого использования многие гомогенные катализаторы можно использовать только при относительно низких температурах, и даже в этом случае они имеют тенденцию к медленному разложению в растворе. Несмотря на эти проблемы, в последние годы был разработан ряд коммерчески жизнеспособных процессов. Полиэтилен высокой плотности и полипропилен получают методом гомогенного катализа.
| Коммерческий процесс | Катализатор | Реагенты | Конечный продукт |
|---|---|---|---|
| Юнион Карбайд | [Rh(CO) 2 I 2 ] − | СО + СН 3 ОХ | CH 3 CO 2 H |
| гидропероксидный процесс | Комплексы Mo(VI) | CH 3 CH=CH 2 + R–O–O–H | |
| гидроформилирование | Rh/PR 3 комплексы | RCH=CH 2 + CO + H 2 | РЧ 2 CH 2 CH |
| адипонитриловый процесс | Ni/PR 3 комплексы | 2HCN + CH 2 =CHCH=CH 2 | NCCH 2 CH 2 CH 2 CH 2 CN используется для синтеза нейлона |
| полимеризация олефинов | (RC 5 H 5 ) 2 ZrCl 2 | CH 2 = CH 2 | –(CH 2 CH 2 –) n : полиэтилен высокой плотности |
Ферменты
Ферменты, катализаторы, встречающиеся в естественных условиях в живых организмах, представляют собой почти все белковые молекулы с типичной молекулярной массой 20 000–100 000 а. е.м. Некоторые из них представляют собой гомогенные катализаторы, которые реагируют в водном растворе внутри клеточного компартмента организма. Другие представляют собой гетерогенные катализаторы, встроенные в мембраны, которые отделяют клетки и клеточные компартменты от их окружения. Реагент в реакции, катализируемой ферментом, называется подложка .
е.м. Некоторые из них представляют собой гомогенные катализаторы, которые реагируют в водном растворе внутри клеточного компартмента организма. Другие представляют собой гетерогенные катализаторы, встроенные в мембраны, которые отделяют клетки и клеточные компартменты от их окружения. Реагент в реакции, катализируемой ферментом, называется подложка .
Поскольку ферменты могут многократно увеличивать скорость реакции (до 10 17 раз по сравнению с некатализируемой скоростью) и имеют тенденцию быть очень специфичными, обычно производя только один продукт с количественным выходом, они находятся в центре активных исследований. В то же время получение ферментов обычно дорого, они часто перестают функционировать при температурах выше 37 °С, имеют ограниченную стабильность в растворе и настолько высокую специфичность, что ограничиваются превращением одного конкретного набора реагентов в один конкретный продукт. . Это означает, что для химически сходных реакций должны быть разработаны отдельные процессы с использованием разных ферментов, что требует много времени и средств. До настоящего времени ферменты нашли лишь ограниченное промышленное применение, хотя они используются в качестве ингредиентов в моющих средствах для стирки, чистящих средствах для контактных линз и размягчителях мяса. Ферменты в этих приложениях, как правило, представляют собой протеазы, которые способны расщеплять амидные связи, удерживающие вместе аминокислоты в белках. Размягчители мяса, например, содержат протеазу, называемую папаином, которую выделяют из сока папайи. Он расщепляет некоторые из длинных волокнистых белковых молекул, которые делают недорогие куски говядины жесткими, в результате чего получается более нежный кусок мяса. Некоторые насекомые, такие как жук-бомбардировщик, содержат фермент, способный катализировать разложение перекиси водорода до воды (рис. \(\PageIndex{3}\)).
До настоящего времени ферменты нашли лишь ограниченное промышленное применение, хотя они используются в качестве ингредиентов в моющих средствах для стирки, чистящих средствах для контактных линз и размягчителях мяса. Ферменты в этих приложениях, как правило, представляют собой протеазы, которые способны расщеплять амидные связи, удерживающие вместе аминокислоты в белках. Размягчители мяса, например, содержат протеазу, называемую папаином, которую выделяют из сока папайи. Он расщепляет некоторые из длинных волокнистых белковых молекул, которые делают недорогие куски говядины жесткими, в результате чего получается более нежный кусок мяса. Некоторые насекомые, такие как жук-бомбардировщик, содержат фермент, способный катализировать разложение перекиси водорода до воды (рис. \(\PageIndex{3}\)).
Ингибиторы ферментов вызывают снижение скорости реакции, катализируемой ферментом, путем связывания с определенной частью фермента и, таким образом, замедления или предотвращения реакции. Таким образом, необратимые ингибиторы являются эквивалентом ядов в гетерогенном катализе. Одним из старейших и наиболее широко используемых коммерческих ингибиторов ферментов является аспирин, который избирательно ингибирует один из ферментов, участвующих в синтезе молекул, вызывающих воспаление. Дизайн и синтез родственных молекул, которые являются более эффективными, селективными и менее токсичными, чем аспирин, являются важными задачами биомедицинских исследований.
Таким образом, необратимые ингибиторы являются эквивалентом ядов в гетерогенном катализе. Одним из старейших и наиболее широко используемых коммерческих ингибиторов ферментов является аспирин, который избирательно ингибирует один из ферментов, участвующих в синтезе молекул, вызывающих воспаление. Дизайн и синтез родственных молекул, которые являются более эффективными, селективными и менее токсичными, чем аспирин, являются важными задачами биомедицинских исследований.
Резюме
Катализаторы участвуют в химической реакции и увеличивают ее скорость. Они не входят в итоговое уравнение реакции и не расходуются в ходе реакции. Катализаторы позволяют реакции протекать по пути, который имеет более низкую энергию активации, чем некатализируемая реакция. В гетерогенном катализе катализаторы обеспечивают поверхность, с которой реагенты связываются в процессе адсорбции. В гомогенном катализе катализаторы находятся в одной фазе с реагентами. Ферменты — это биологические катализаторы, которые вызывают значительное увеличение скорости реакции и, как правило, специфичны для определенных реагентов и продуктов. Реагент в реакции, катализируемой ферментом, называется субстратом. Ингибиторы ферментов вызывают снижение скорости реакции, катализируемой ферментом.
Реагент в реакции, катализируемой ферментом, называется субстратом. Ингибиторы ферментов вызывают снижение скорости реакции, катализируемой ферментом.
14.7: Catalysis распространяется под лицензией CC BY-NC-SA 3.0, автором, ремиксом и/или куратором является LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 3,0
- Показать страницу Содержание
- нет на странице
- Теги
- фермент
- гетерогенный катализ
- Гомогенный катализ
- подложка
Катализатор Определение и значение | Dictionary.
 com
com- Верхние определения
- Викторина
- Связанный контент
- Примеры
- British
- Medical
- Scervifics 222229
- Scervifics
- .
[ kat-l-ist ]
/ ˈkæt l ɪst /
Сохранить это слово!
См. синонимы для: катализатор / катализаторы на Thesaurus.com
Показывает уровень оценки в зависимости от сложности слова.
Определение катализатора
сущ.
Химия. вещество, которое вызывает или ускоряет химическую реакцию, не затрагивая при этом самого себя.
то, что вызывает активность между двумя или более людьми или силами без воздействия на себя.

человек или предмет, который ускоряет событие или изменение: его тюремное заключение правительством послужило катализатором, который помог преобразовать социальные волнения в революцию.
человек, чьи разговоры, энтузиазм или энергия заставляют других быть более дружелюбными, восторженными или энергичными.
ВИДЕО ДЛЯ КАТАЛИЗАТОРА
Может ли человек быть катализатором?
Катализатор означает «что-то, что вызывает активность, событие или изменение». И обычно эти события и изменения бывают большими. Но может ли катализатором быть человек?
БОЛЬШЕ ВИДЕО ОТ DICTIONARY.COM
ВИКТОРИНА
Сыграем ли мы «должен» против. «ДОЛЖЕН» ВЫЗОВ?
Следует ли вам пройти этот тест на «должен» или «должен»? Это должно оказаться быстрым вызовом!
Вопрос 1 из 6
Какая форма используется для указания обязательства или обязанности кого-либо?
Происхождение катализатора
Впервые зафиксировано в 1900-05 гг.
 ; cataly(sis) + (-i)st
; cataly(sis) + (-i)stДРУГИЕ СЛОВА ИЗ Catalonian
self-cat·a·lyst, сущ. катализ, катализ, катализатор, каталитический, каталитический нейтрализатор, установка каталитического крекинга, каталитический крекинг, катализироватьDictionary.com Полный текст На основе Random House Unabridged Dictionary, © Random House, Inc. 2022
Слова, относящиеся к слову катализатор
импульс, стимул, мотивация, стимулятор, адъювант, агитатор, фермент, побуждение, импульс, зажигательный, подстрекательство, подстрекательство, реагент, реактивный , шпора, синергист, свеча зажигания
Как использовать катализатор в предложении
Южная Африка обеспечивает 84% металлов платиновой группы, необходимых для топливных элементов и автомобильных катализаторов.
Европа полагается на иностранное сырье для обеспечения своего зеленого и цифрового будущего. Теперь он хочет добывать их дома|Дэвид Мейер|3 сентября 2020 г.|Fortune
То время, которое я провел в Гане, а также в Западной Африке и странах Африки к югу от Сахары, стало моим катализатором для запуска Tala, и я регулярно призываю членов моей команды взять на себя «разобраться!»
Совет, который помог 40-летним моложе 40 в этом году найти свой собственный путь|kdunn6|3 сентября 2020 г.
 |Fortune
|FortuneСмерть Флойда стала катализатором предыдущих протестов в этом году, а стрельба по Блейку вновь разожгла демонстрации.
Жестокие протесты против жестокости полиции в 60-х и 90-х изменили общественное мнение|Немец Лопес|28 августа 2020 г.|Vox
Так что, больше всего на свете, одобрение стало для нас катализатором, чтобы мы действительно сказали, давайте что-нибудь сделаем , нам не нужно сидеть и ждать, что мы будем делать, одобрять или не одобрять.
Новый проект Log Cabin стремится повторить успех видео Гренелла|Крис Джонсон|26 августа 2020 г.|Washington Blade
Бритни Сайкс — защитный катализатор Спаркс, и ее эффективность значительно улучшилась с двух.
Матча всех звезд WNBA в этом году не будет, но мы все равно выбрали составы|Ховард Мегдал|26 августа 2020 г.|FiveThirtyEight
Но медь выполняет еще одну важную функцию: работает как катализатор в процессе дистилляции.
Когда дело доходит до хорошего виски, размер вашего по-прежнему имеет значение||9 декабря 2014 г.
 |DAILY BEAST
|DAILY BEASTБранч — это катализатор, бранч — это соблюдение различных правил для выходных.
Не пренебрегайте красотой бранча: защищая нашу любимую еду|Тим Тиман|15 октября 2014 г.|DAILY BEAST
Мы гордимся тем, что наш фильм может стать катализатором даже небольших изменений в жизни этих мальчиков. лечатся в Китае.
Китай не хочет, чтобы вы смотрели фильм об интернет-зависимости «Веб-наркоман»|Шош Шлам и Хилла Медалия|9 августа 2014 г.|DAILY BEAST
Другие сервисы, не связанные с дизайном, такие как Adobe Business Catalyst, который проводит кампании по сбору средств по электронной почте и электронную коммерцию, также перестали работать.
«Creative Cloud» от Adobe уходит в автономный режим и забирает с собой миллион дизайнеров|Кайл Чайка|16 мая 2014 г.|DAILY BEAST
И этот вопрос является катализатором всей двусмысленности на протяжении всего фильма.
Как режиссер фильма «Превосходство» Уолли Пфистер стал секретным оружием Кристофера Нолана|Эндрю Романо|17 апреля 2014 г.
 |DAILY BEAST
|DAILY BEASTВозможно, это простое действие послужило катализатором, который дал Берлу решение проблемы.
Забытая планета|Мюррей Ленстер
Таким образом, мы можем сравнить катализатор с тем, что в обществе известно как «хороший миксер».
Творческая химия|Эдвин Э. Слоссон
Тактичная хозяйка, руководитель салона, является социальным катализатором.
Creative Chemistry|Edwin E. Slosson
При контакте перекиси водорода с катализатором, таким как перманганат калия, она распадается на кислород и воду.
Операция: Космос|Уильям Фицджеральд Дженкинс
Катализатор, который был необходим для окончательной реакции, должен был принести ему Полтер.
Beyond the Vanishing Point|Raymond King Cummings
Определение катализатора в Британском словаре
катализатор
/ (ˈkætəlɪst) /
химическая реакция, которая сама по себе увеличивает страдание химическое изменениеСравнить ингибитор (по умолч.
 2)
2)человек или вещь, вызывающая изменение
Collins English Dictionary — Complete & Unabridged 2012 Digital Edition © William Collins Sons & Co. Ltd., 1979, 1986 © HarperCollins Publishers 1998, 2000, 2003, 2005, 2006, 2007, 2009, 2012
Медицинские определения катализатора
Катализатор
[ кэтл-ист ]
n.
Вещество, обычно используемое в небольших количествах по отношению к реагентам, которое изменяет и увеличивает скорость реакции, не расходуясь в процессе.
Другие слова от слова катализатор
каталический (катал-ит’ик) прил.Медицинский словарь Стедмана The American Heritage® Copyright © 2002, 2001, 1995, компания Houghton Mifflin. Опубликовано компанией Houghton Mifflin.
Научное определение катализатора
катализатор
[ кэтл-ист ]
Вещество, которое запускает или ускоряет химическую реакцию, не претерпевая при этом необратимых изменений. Например, ферменты слюны являются катализаторами пищеварения.

Другие слова из слова «катализатор»
каталитический прилагательное (kăt′l-ĭt′ĭk)Научный словарь American Heritage® Авторские права © 2011. Опубликовано издательством Houghton Mifflin Harcourt Publishing Company. Все права защищены.
Культуральные определения катализатора
катализатор
[ (кат-э-список) ]
В химии — вещество, которое вызывает химическую реакцию, но само в ней не участвует.
примечания для катализатора
Термин «катализатор» часто используется для обозначения главного агента любых изменений: «Она была катализатором реорганизации».
Новый словарь культурной грамотности, третье издание Авторское право © 2005 г., издательство Houghton Mifflin Harcourt Publishing Company. Опубликовано издательством Houghton Mifflin Harcourt Publishing Company. Все права защищены.
Катализатор против фермента — разница и сравнение
Ферменты и катализаторы влияют на скорость реакции.
 Фактически все известные ферменты являются катализаторами, но не все катализаторы являются ферментами. 90 927 различий между катализаторами и ферментами заключается в том, что ферменты в основном имеют органическую природу и являются биокатализаторами, в то время как неферментативные катализаторы могут быть неорганическими соединениями. Ни катализаторы, ни ферменты не расходуются в реакциях, которые они катализируют.
Фактически все известные ферменты являются катализаторами, но не все катализаторы являются ферментами. 90 927 различий между катализаторами и ферментами заключается в том, что ферменты в основном имеют органическую природу и являются биокатализаторами, в то время как неферментативные катализаторы могут быть неорганическими соединениями. Ни катализаторы, ни ферменты не расходуются в реакциях, которые они катализируют.Для простоты катализатор в этой статье относится к неферментативным катализаторам, которые легко отличить от ферментов.
Сравнительная таблица
Сравнительная таблица катализатора и фермента Катализатор Фермент Функция Катализаторы — это вещества, которые увеличивают или уменьшают скорость химической реакции, но остаются неизменными. Ферменты — это белки, которые увеличивают скорость химических реакций, превращающих субстрат в продукт. 
Молекулярная масса Низкомолекулярные соединения. Высокомолекулярные глобулярные белки. Типы Катализаторы бывают двух типов – положительные и отрицательные. Существует два типа ферментов — ферменты активации и ферменты ингибирования. Природа Катализаторы представляют собой простые неорганические молекулы. Ферменты представляют собой сложные белки. Альтернативные термины Неорганический катализатор. Органический катализатор или биокатализатор. Скорость реакции Обычно медленнее В несколько раз быстрее Специфичность Они неспецифичны и поэтому в конечном итоге дают остатки с ошибками Ферменты обладают высокой специфичностью, образуя большое количество полезных остатков Условия Высокая температура, давление Мягкие условия, физиологические значения pH и температуры С-С и С-Н связи отсутствуют подарок Пример оксид ванадия амилаза, липаза Энергия активации Понижает Опускает Краткая история катализаторов, ферментов и катализа.

Катализ. хлеба и т. д. В 1812 году русский химик Готлиб Сигизмунд Константин Кирхгоф изучал расщепление крахмала на сахар или глюкозу в кипящей воде в присутствии нескольких капель концентрированной серной кислоты. Серная кислота после эксперимента не изменилась и ее можно было восстановить. В 1835 году шведский химик Йонс Якоб Берцелиус предложил название «9».0927 катализ» от греческого термина «ката» означает вниз и «лайин» означает расслабить.
После того, как были поняты реакции катализа, ученые открыли множество реакций, скорость которых изменялась в присутствии катализаторов . Луи Пастер обнаружил, что существует некий фактор, катализирующий его эксперименты по ферментации сахара и действующий только в живых клетках. Позднее немецкий физиолог Вильгельм Кюне в 1878 году назвал этот фактор «ферментом». Фермент происходит от греческого слова, означающего «в закваске». В 1897 Эдуард Бюхнер назвал фермент, ферментирующий сахарозу, ферментазой.
 Его эксперименты также доказали, что ферменты могут функционировать вне живой клетки. В конце концов были открыты структура и функции различных ферментов, катализирующих важные функции.
Его эксперименты также доказали, что ферменты могут функционировать вне живой клетки. В конце концов были открыты структура и функции различных ферментов, катализирующих важные функции.Структура катализаторов и ферментов
Катализатор — это любое вещество, которое может вызывать значительные изменения скорости химической реакции. Таким образом, это может быть чистый элемент, такой как никель или платина, чистое соединение, такое как диоксид кремния, диоксид марганца, растворенные ионы, такие как ионы меди, или даже смесь, такая как железо-молибден. Наиболее часто используемыми катализаторами являются протонные кислоты в реакции гидролиза. Окислительно-восстановительные реакции катализируются переходными металлами, а платина используется для реакций с участием водорода. Некоторые катализаторы встречаются как предкатализаторы и превращаются в катализаторы в ходе реакции.
 Типичным примером является катализатор Уилкинсона — RhCl (PPh 3 ) 3 , который теряет один трифенилфосфиновый лиганд при катализе реакции.
Типичным примером является катализатор Уилкинсона — RhCl (PPh 3 ) 3 , который теряет один трифенилфосфиновый лиганд при катализе реакции.Ферменты представляют собой глобулярные белки и могут состоять из 62 аминокислот (4-оксалокротонат) до 2500 аминокислот (синтаза жирных кислот). Существуют также ферменты на основе РНК, называемые рибозимами . Ферменты специфичны к субстрату и обычно больше, чем их соответствующие субстраты. В ферментативной реакции участвует лишь небольшая часть фермента. Активный центр — это место, где субстраты связываются с ферментом для облегчения реакции. Другие факторы, такие как кофакторы, прямые продукты и т. д., также имеют специфические сайты связывания на ферменте. Ферменты состоят из длинных цепочек аминокислот, которые накладываются друг на друга, образуя глобулярную структуру. Аминокислотная последовательность придает ферментам субстратную специфичность. Тепло и химические вещества могут денатурировать фермент.

Различия в механизме реакций
Оба катализатора и ферменты снижают энергию активации реакции, тем самым увеличивая ее скорость.
Катализатор может быть положительным (повышает скорость реакции) или отрицательным (уменьшает скорость реакции) по своей природе. Они реагируют с реагентами в ходе химической реакции с образованием промежуточных продуктов, которые в конечном итоге высвобождают продукт и регенерируют катализатор. Рассмотрим реакцию, в которой
C — Катализатор
A и B — реагенты, а
P — Продукт.Типичной каталитической химической реакцией будет:
A + C → AC
B + AC → ABC
ABC → PC
PC → P + CThe catalyst регенерируется на последнем этапе, хотя на промежуточных этапах он интегрировался с реагентами.

Ферментативные реакции протекают по-разному:
- Снижение энергии активации и переход в стабильное переходное состояние обычно достигается за счет искажения формы подложки.
- Снижение энергии переходного состояния без деформации подложки.
- Временное образование комплекса фермент-субстрат и тем самым предоставление альтернативного пути для протекания реакции.
- Снижение энтропии реакции.
- Повышение температуры.
Механизм ферментативного действия соответствует модели индуцированной подгонки, предложенной Даниэлем Кошландом в 1958 году. Согласно этой модели, субстрат встраивается в фермент, и могут быть небольшие изменения в форме фермента и субстрата по мере того, как субстрат связывается с самим собой. активный центр фермента с образованием комплекса фермент-субстрат.
Примеры каталитических и ферментативных реакций
Каталитический нейтрализатор , используемый в автомобилях, представляет собой устройство, удаляющее загрязняющие газы из выхлопных систем автомобилей.
 В качестве катализаторов здесь используются платина и родий, которые расщепляют опасные газы до безвредных. Например, окись азота превращается в азот и кислород в присутствии небольшого количества платины и родия.
В качестве катализаторов здесь используются платина и родий, которые расщепляют опасные газы до безвредных. Например, окись азота превращается в азот и кислород в присутствии небольшого количества платины и родия.Фермент амилаза способствует превращению сложного крахмала в более легко усваиваемую сахарозу.
Промышленное применение
Катализаторы используются в производстве энергии; производство сыпучих химикатов; тонкая химия; в производстве маргарина и в окружающей среде, где они играют решающую роль свободных радикалов хлора в разрушении озона.
Ферменты используются в пищевой промышленности; детское питание; пивоварение; фруктовые соки; молочное производство; крахмальная, бумажная и биотопливная промышленность; макияж, чистка контактных линз; резина, фотография и молекулярная биология.
Ссылки
- Википедия: Фермент
- Википедия: Катализ
- Информация о ферментах — Научное разъяснение
- Подписаться
- Поделиться
- Ссылка
- Авторы
Поделитесь этим сравнением:
Если вы дочитали до этого места, подписывайтесь на нас:
«Катализатор против фермента».
 Diffen.com. Diffen LLC, nd Веб. 28 сентября 2022 г. < >
Diffen.com. Diffen LLC, nd Веб. 28 сентября 2022 г. < >Центральная роль ферментов как биологических катализаторов — клетка
Основная задача белков — действовать как ферменты — катализаторы, увеличивающие скорость практически всех химических реакций внутри клеток. Хотя РНК способны катализировать некоторые реакции, большинство биологических реакций катализируются белками. В отсутствие ферментативного катализа большинство биохимических реакций протекают настолько медленно, что не могли бы протекать в мягких условиях температуры и давления, совместимых с жизнью. Ферменты ускоряют скорость таких реакций более чем в миллион раз, поэтому реакции, которые без катализа заняли бы годы, могут протекать за доли секунд, если их катализирует соответствующий фермент. Клетки содержат тысячи различных ферментов, и их активность определяет, какие из многих возможных химических реакций действительно происходят внутри клетки.
Каталитическая активность ферментов
Как и все другие катализаторы, ферменты характеризуются двумя фундаментальными свойствами.
 Во-первых, они увеличивают скорость химических реакций, но сами не поглощаются и не изменяются в результате реакции. Во-вторых, они увеличивают скорость реакции, не нарушая химического равновесия между реагентами и продуктами.
Во-первых, они увеличивают скорость химических реакций, но сами не поглощаются и не изменяются в результате реакции. Во-вторых, они увеличивают скорость реакции, не нарушая химического равновесия между реагентами и продуктами.Эти принципы ферментативного катализа проиллюстрированы в следующем примере, в котором молекула, на которую действует фермент (называемая субстратом [ S ]) в результате реакции превращается в продукт ( P ). В отсутствие фермента реакция может быть записана следующим образом:
Химическое равновесие между S и P определяется законами термодинамики (как обсуждается далее в следующем разделе этой главы) и представлено отношением скоростей прямой и обратной реакции ( S → P и P → S соответственно). В присутствии соответствующего фермента превращение S по P ускоряется, но равновесие между S и P не меняется. Следовательно, фермент должен одинаково ускорять и прямую, и обратную реакции.
 Реакция может быть записана следующим образом:
Реакция может быть записана следующим образом:Обратите внимание, что фермент ( E ) не изменяется в результате реакции, поэтому химическое равновесие остается неизменным, определяемым исключительно термодинамическими свойствами S и P .
Влияние фермента на такую реакцию лучше всего иллюстрируется изменениями энергии, которые должны происходить при превращении S до P (). Равновесие реакции определяется конечными энергетическими состояниями S и P , на которые не влияет ферментативный катализ. Однако для того, чтобы реакция шла, субстрат должен быть сначала переведен в более высокое энергетическое состояние, называемое переходным состоянием . Энергия, необходимая для достижения переходного состояния (энергия активации), представляет собой барьер для протекания реакции, ограничивая скорость реакции. Ферменты (и другие катализаторы) действуют, уменьшая энергию активации, тем самым увеличивая скорость реакции.
 Повышенная скорость одинакова как в прямом, так и в обратном направлении, поскольку оба должны пройти через одно и то же переходное состояние.
Повышенная скорость одинакова как в прямом, так и в обратном направлении, поскольку оба должны пройти через одно и то же переходное состояние.Рисунок 2.22
Энергетические диаграммы для катализируемых и некаталитических реакций. Проиллюстрированная реакция представляет собой простое превращение субстрата S в продукт P. Поскольку конечное энергетическое состояние P ниже, чем у S , реакция протекает слева направо. Для (подробнее…)
Каталитическая активность ферментов включает связывание их субстратов с образованием комплекса фермент-субстрат ( ES ). Субстрат связывается с определенной областью фермента, называемой активным центром. Связанный с активным центром субстрат превращается в продукт реакции, который затем высвобождается из фермента. Таким образом, катализируемая ферментом реакция может быть записана следующим образом:
Обратите внимание, что E не меняется в обеих частях уравнения, поэтому равновесие не изменяется.
 Однако фермент обеспечивает поверхность, на которой реакции превращения S в P могут происходить более легко. Это результат взаимодействий между ферментом и субстратом, которые снижают энергию активации и способствуют образованию переходного состояния.
Однако фермент обеспечивает поверхность, на которой реакции превращения S в P могут происходить более легко. Это результат взаимодействий между ферментом и субстратом, которые снижают энергию активации и способствуют образованию переходного состояния.Механизмы ферментативного катализа
Связывание субстрата с активным центром фермента представляет собой очень специфическое взаимодействие. Активные центры представляют собой щели или бороздки на поверхности фермента, обычно состоящие из аминокислот из разных частей полипептидной цепи, объединенных в третичную структуру свернутого белка. Субстраты первоначально связываются с активным центром посредством нековалентных взаимодействий, включая водородные связи, ионные связи и гидрофобные взаимодействия. Как только субстрат связывается с активным центром фермента, несколько механизмов могут ускорить его превращение в продукт реакции.
Хотя в простом примере, рассмотренном в предыдущем разделе, участвовала только одна молекула субстрата, большинство биохимических реакций включают взаимодействие между двумя или более различными субстратами.
 Например, образование пептидной связи предполагает соединение двух аминокислот. Для таких реакций связывание двух или более субстратов с активным центром в правильном положении и ориентации ускоряет реакцию (1). Фермент обеспечивает матрицу, на которой реагенты собираются вместе и должным образом ориентируются, чтобы способствовать образованию переходного состояния, в котором они взаимодействуют.
Например, образование пептидной связи предполагает соединение двух аминокислот. Для таких реакций связывание двух или более субстратов с активным центром в правильном положении и ориентации ускоряет реакцию (1). Фермент обеспечивает матрицу, на которой реагенты собираются вместе и должным образом ориентируются, чтобы способствовать образованию переходного состояния, в котором они взаимодействуют.Рисунок 2.23
Ферментативный катализ реакции между двумя субстратами. Фермент обеспечивает матрицу, на которой два субстрата соединяются вместе в правильном положении и ориентации для взаимодействия друг с другом.
Ферменты ускоряют реакции также путем изменения конформации их субстратов, приближая их к конформации переходного состояния. Простейшей моделью взаимодействия фермент-субстрат является модель типа «замок-ключ» , в которой субстрат точно помещается в активный центр (). Однако во многих случаях конфигурация как фермента, так и субстрата модифицируется за счет связывания субстрата — процесс, называемый индуцированная посадка .
 В таких случаях конформация субстрата изменяется так, что она больше напоминает переходное состояние. Напряжение, создаваемое таким искажением подложки, может дополнительно способствовать ее переходу в переходное состояние за счет ослабления критических связей. Более того, переходное состояние стабилизируется его прочным связыванием с ферментом, что снижает необходимую энергию активации.
В таких случаях конформация субстрата изменяется так, что она больше напоминает переходное состояние. Напряжение, создаваемое таким искажением подложки, может дополнительно способствовать ее переходу в переходное состояние за счет ослабления критических связей. Более того, переходное состояние стабилизируется его прочным связыванием с ферментом, что снижает необходимую энергию активации.Рисунок 2.24
Модели фермент-субстратного взаимодействия. (A) В модели «замок-ключ» субстрат точно соответствует активному центру фермента. (B) В модели индуцированного соответствия связывание субстрата искажает конформации как субстрата, так и фермента. Это искажение (далее…)
В дополнение к объединению нескольких субстратов и искажению конформации субстратов для приближения к переходному состоянию многие ферменты непосредственно участвуют в каталитическом процессе. В таких случаях специфические боковые цепи аминокислот в активном центре могут реагировать с субстратом и образовывать связи с промежуточными продуктами реакции.
 Кислотные и основные аминокислоты часто участвуют в этих каталитических механизмах, как показано в последующем обсуждении химотрипсина как примера ферментативного катализа.
Кислотные и основные аминокислоты часто участвуют в этих каталитических механизмах, как показано в последующем обсуждении химотрипсина как примера ферментативного катализа.Химотрипсин является членом семейства ферментов (сериновых протеаз), которые расщепляют белки, катализируя гидролиз пептидных связей. Реакция может быть записана следующим образом:
Различные представители семейства сериновых протеаз (включая химотрипсин, трипсин, эластазу и тромбин) обладают различной субстратной специфичностью; они преимущественно расщепляют пептидные связи, расположенные рядом с разными аминокислотами. Например, в то время как химотрипсин расщепляет связи рядом с гидрофобными аминокислотами, такими как триптофан и фенилаланин, трипсин расщепляет связи рядом с основными аминокислотами, такими как лизин и аргинин. Однако все сериновые протеазы сходны по структуре и используют один и тот же механизм катализа. Активные центры этих ферментов содержат три критически важные аминокислоты — серин, гистидин и аспартат, — которые управляют гидролизом пептидной связи.
 Действительно, эти ферменты называются сериновыми протеазами из-за центральной роли остатка серина.
Действительно, эти ферменты называются сериновыми протеазами из-за центральной роли остатка серина.Субстраты связываются с сериновыми протеазами путем встраивания аминокислоты рядом с сайтом расщепления в карман в активном центре фермента (). Природа этого кармана определяет субстратную специфичность различных членов семейства сериновых протеаз. Например, связывающий карман химотрипсина содержит гидрофобные аминокислоты, которые взаимодействуют с гидрофобными боковыми цепями его предпочтительных субстратов. Напротив, связывающий карман трипсина содержит отрицательно заряженную кислую аминокислоту (аспартат), которая способна образовывать ионную связь с остатками лизина или аргинина своих субстратов.
Рисунок 2.25
Связывание субстрата сериновыми протеазами. Аминокислота, примыкающая к расщепляемой пептидной связи, вставляется в карман в активном центре фермента. У химотрипсина карман связывает гидрофобные аминокислоты; связывающий карман трипсина содержит (подробнее.
 ..)
..)Связывание субстрата позиционирует расщепляемую пептидную связь рядом с активным центром серина (). Затем протон этого серина переносится в активный центр гистидина. Конформация активного центра способствует переносу протона, поскольку гистидин взаимодействует с отрицательно заряженным аспартатным остатком. Серин реагирует с субстратом, образуя тетраэдрическое переходное состояние. Затем пептидная связь расщепляется, и С-концевая часть субстрата высвобождается из фермента. Однако N-концевой пептид остается связанным с серином. Эта ситуация разрешается, когда молекула воды (второй субстрат) входит в активный центр и обращает предшествующие реакции. Протон молекулы воды переносится на гистидин, а его гидроксильная группа – на пептид, образуя второе тетраэдрическое переходное состояние. Затем протон переносится с гистидина обратно на серин, а пептид высвобождается из фермента, завершая реакцию.
Рисунок 2.26
Каталитический механизм химотрипсина. Три аминокислоты в активном центре (Ser-195, His-57 и Asp-102) играют решающую роль в катализе.

Этот пример иллюстрирует некоторые особенности ферментативного катализа; специфичность фермент-субстратных взаимодействий, расположение различных молекул субстрата в активном центре и участие остатков активного центра в формировании и стабилизации переходного состояния. Хотя тысячи ферментов в клетках катализируют множество различных типов химических реакций, в их работе применяются одни и те же основные принципы.
Коэнзимы
Помимо связывания своих субстратов, активные центры многих ферментов связывают другие малые молекулы, участвующие в катализе. Простетические группы представляют собой небольшие молекулы, связанные с белками, в которых они играют важную функциональную роль. Например, кислород, переносимый миоглобином и гемоглобином, связан с гемом, простетической группой этих белков. Во многих случаях ионы металлов (например, цинка или железа) связаны с ферментами и играют центральную роль в каталитическом процессе. Кроме того, различные низкомолекулярные органические молекулы участвуют в специфических типах ферментативных реакций.
 Эти молекулы называются коферментами, потому что они работают вместе с ферментами, увеличивая скорость реакции. В отличие от субстратов коферменты не изменяются необратимо в результате реакций, в которых они участвуют. Скорее, они перерабатываются и могут участвовать во множестве ферментативных реакций.
Эти молекулы называются коферментами, потому что они работают вместе с ферментами, увеличивая скорость реакции. В отличие от субстратов коферменты не изменяются необратимо в результате реакций, в которых они участвуют. Скорее, они перерабатываются и могут участвовать во множестве ферментативных реакций.Коэнзимы служат переносчиками нескольких типов химических групп. Ярким примером кофермента является никотинамидадениндинуклеотид ( НАД + ), который функционирует как переносчик электронов в окислительно-восстановительных реакциях (). НАД + может принимать ион водорода (Н + ) и два электрона (е — ) с одного субстрата, образуя НАДН. Затем NADH может отдавать эти электроны второму субстрату, повторно образуя NAD + . Таким образом, НАД + переносит электроны с первого субстрата (который окисляется) на второй (который восстанавливается).
Рис. 2.27
Роль НАД + в окислительно-восстановительных реакциях.
 (A) Никотинамидадениндинуклеотид (НАД + ) действует как переносчик электронов в окислительно-восстановительных реакциях, принимая электроны (е — ) с образованием НАДН. (B) Например, NAD + может принимать электроны от одного субстрата (подробнее…)
(A) Никотинамидадениндинуклеотид (НАД + ) действует как переносчик электронов в окислительно-восстановительных реакциях, принимая электроны (е — ) с образованием НАДН. (B) Например, NAD + может принимать электроны от одного субстрата (подробнее…)Несколько других коферментов также действуют как переносчики электронов, а третьи участвуют в переносе множества дополнительных химических групп (например, , карбоксильные группы и ацильные группы; ). Одни и те же коферменты действуют вместе с множеством различных ферментов, катализируя перенос определенных химических групп между широким спектром субстратов. Многие коферменты тесно связаны с витаминами, которые частично или полностью составляют структуру кофермента. Витамины не требуются бактериям, таким как E. coli , но являются необходимыми компонентами рациона человека и других высших животных, утративших способность синтезировать эти соединения.
Таблица 2.1
Примеры коферментов и витаминов.

Регулирование активности ферментов
Важной особенностью большинства ферментов является то, что их активность не постоянна, а может модулироваться. То есть активность ферментов можно регулировать так, чтобы они функционировали надлежащим образом для удовлетворения различных физиологических потребностей, которые могут возникнуть в течение жизни клетки.
Одним из распространенных типов регуляции ферментов является ингибирование по принципу обратной связи, при котором продукт метаболического пути ингибирует активность фермента, участвующего в его синтезе. Например, аминокислота изолейцин синтезируется серией реакций, начиная с аминокислоты треонина (). Первый этап пути катализируется ферментом треониндезаминазой, которая ингибируется изолейцином, конечным продуктом пути. Таким образом, достаточное количество изолейцина в клетке ингибирует треониндезаминазу, блокируя дальнейший синтез изолейцина. Если концентрация изолейцина снижается, ингибирование по принципу обратной связи снимается, треониндезаминаза больше не ингибируется и синтезируется дополнительный изолейцин.
 Регулируя таким образом активность треониндезаминазы, клетка синтезирует необходимое количество изолейцина, но избегает затрат энергии на синтез большего количества изолейцина, чем необходимо.
Регулируя таким образом активность треониндезаминазы, клетка синтезирует необходимое количество изолейцина, но избегает затрат энергии на синтез большего количества изолейцина, чем необходимо.Рисунок 2.28
Подавление обратной связи. Первый этап превращения треонина в изолейцин катализируется ферментом треониндезаминазой. Активность этого фермента ингибируется изолейцином, конечным продуктом пути.
Ингибирование по принципу обратной связи является одним из примеров аллостерической регуляции, при которой активность фермента контролируется путем связывания небольших молекул с регуляторными участками фермента (). Термин «аллостерическая регуляция» происходит от того факта, что регуляторные молекулы связываются не с каталитическим участком, а с отдельным участком на белке (9).0935 алло = «другое» и steric = «сайт»). Связывание регуляторной молекулы изменяет конформацию белка, что, в свою очередь, изменяет форму активного центра и каталитическую активность фермента.
 В случае треониндезаминазы связывание регуляторной молекулы (изолейцина) ингибирует ферментативную активность. В других случаях регуляторные молекулы служат активаторами, стимулируя, а не ингибируя ферменты-мишени.
В случае треониндезаминазы связывание регуляторной молекулы (изолейцина) ингибирует ферментативную активность. В других случаях регуляторные молекулы служат активаторами, стимулируя, а не ингибируя ферменты-мишени.Рисунок 2.29
Аллостерическая регуляция. В этом примере активность фермента ингибируется связыванием регуляторной молекулы с аллостерическим сайтом. В отсутствие ингибитора субстрат связывается с активным центром фермента, и реакция протекает. Переплет (далее…)
Активность ферментов можно также регулировать путем их взаимодействия с другими белками и ковалентными модификациями, такими как добавление фосфатных групп к остаткам серина, треонина или тирозина. Фосфорилирование является особенно распространенным механизмом регуляции активности ферментов; добавление фосфатных групп либо стимулирует, либо ингибирует активность многих различных ферментов (). Например, мышечные клетки реагируют на эпинефрин (адреналин), расщепляя гликоген на глюкозу, тем самым обеспечивая источник энергии для повышения мышечной активности.
 Расщепление гликогена катализируется ферментом гликогенфосфорилазой, который активируется путем фосфорилирования в ответ на связывание адреналина с рецептором на поверхности мышечной клетки. Фосфорилирование белков играет центральную роль в контроле не только метаболических реакций, но и многих других клеточных функций, включая рост и дифференцировку клеток.
Расщепление гликогена катализируется ферментом гликогенфосфорилазой, который активируется путем фосфорилирования в ответ на связывание адреналина с рецептором на поверхности мышечной клетки. Фосфорилирование белков играет центральную роль в контроле не только метаболических реакций, но и многих других клеточных функций, включая рост и дифференцировку клеток.Рисунок 2.30
Фосфорилирование белков. Некоторые ферменты регулируются добавлением фосфатных групп к ОН-группам боковых цепей остатков серина (как показано здесь), треонина или тирозина. Например, фермент гликогенфосфорилаза, катализирующий превращение (подробнее…)
Что такое рыночные катализаторы? — Dividend.com
Дивидендный университет
Боб Сиура
В конце концов, рынки не делают больших движений без причины.
Инвесторы часто ищут катализаторы, которые могут подтолкнуть рынок к следующему важному движению вверх или вниз. При обзоре повышения или понижения рейтинга аналитиков или при чтении статей в Интернете с описанием фондового рынка часто используется термин «катализатор», но новички могут не знать, что означает катализатор и как он используется.
 Катализатор — это драматическое событие, которое может сдвинуть рынки с места. Само собой разумеется, что рыночное событие должно быть заметным, поскольку фондовый рынок состоит из тысяч публично торгуемых компаний стоимостью в триллионы долларов. Когда рынки растут или падают на большие проценты, для этих движений есть причина, и эта причина называется катализатором.
Катализатор — это драматическое событие, которое может сдвинуть рынки с места. Само собой разумеется, что рыночное событие должно быть заметным, поскольку фондовый рынок состоит из тысяч публично торгуемых компаний стоимостью в триллионы долларов. Когда рынки растут или падают на большие проценты, для этих движений есть причина, и эта причина называется катализатором.Но действительно есть много событий, которые могут двигать рынки в любом направлении, в краткосрочной или долгосрочной перспективе. Инвесторы должны ознакомиться со своим пониманием рыночных катализаторов и того, как они могут влиять на фондовые рынки.
Краткосрочные катализаторы
Катализаторы могут служить очень важной цели, которая состоит в том, чтобы исправить значительную недооценку или переоценку запасов. Если цена акций компании значительно снизилась, открытие нового продукта или проведение слияния могут послужить катализатором для приведения оценки в соответствие с более подходящими мультипликаторами.
 Эти катализаторы могут действовать как в краткосрочной, так и в долгосрочной перспективе.
Эти катализаторы могут действовать как в краткосрочной, так и в долгосрочной перспективе.Например, краткосрочным катализатором могут быть ежемесячные отчеты о работе. Каждый месяц Бюро статистики труда публикует отчет, в котором подробно указывается, сколько рабочих мест было создано в предыдущем месяце, а также новый уровень безработицы в США. Каждый ежемесячный отчет может оказать ощутимое влияние на рынок, поскольку инвесторы делают выводы о состоянии базовой экономики США на основе сигналов, посылаемых рынком труда. Однако этот эффект обычно непродолжителен, так как до отчета за следующий месяц останется всего 30 дней, что может послать целую новую порцию сигналов.
Пример
Примером рыночного катализатора, который оказал лишь краткосрочное влияние на фондовый рынок, был отчет о занятости за май 2016 года, который показал, что было создано 38 000 новых рабочих мест, что значительно меньше 162 000, ожидаемых экономистами. Эта новость привела к падению промышленного индекса Доу-Джонса почти на 150 пунктов на открытии в день публикации разочаровывающего отчета о занятости, но это оказалось лишь краткосрочным.
 Отчеты о будущих рабочих местах в последующие месяцы сильно превзошли ожидания, и с тех пор рынки восстановились, приблизившись к историческим максимумам.
Отчеты о будущих рабочих местах в последующие месяцы сильно превзошли ожидания, и с тех пор рынки восстановились, приблизившись к историческим максимумам.Долгосрочные катализаторы
С другой стороны, катализаторы могут иметь долгосрочный характер. Примером этого являются процентные ставки. Федеральная резервная система США собирается несколько раз в год для обсуждения состояния экономики США и принятия решений относительно того, следует ли изменить процентные ставки или оставить их на прежнем уровне. В декабре 2015 года Федеральная резервная система повысила процентные ставки, измеряемые ставкой по федеральным фондам, с нуля до 0,25%. Это было первое повышение процентной ставки почти за десятилетие, и в результате оно оказало значительное влияние на рынки, которое все еще ощущается. То, что происходит с процентными ставками, может повлиять на ряд секторов рынка в долгосрочной перспективе, включая коммунальные услуги и инвестиционные фонды недвижимости (REIT).
 На долгосрочную структуру капитала этих компаний могут повлиять изменения процентных ставок.
На долгосрочную структуру капитала этих компаний могут повлиять изменения процентных ставок.Пример
Еще одним примером движущего рынком катализатора с долгосрочными последствиями является недавнее голосование по Brexit. 23 июня Великобритания проголосовала за выход из Евросоюза. Это было заметным событием, которое привело к значительному падению мировых рынков. В то время как мировые индексы восстановились, многие известные дивидендные акции не восстановились. Например, гигант коммунальных услуг PPL Corp. (PPL) торговался по 39,44 доллара за акцию в день голосования по Brexit. PPL сильно зависит от Brexit, потому что он получает значительную часть своих доходов из Европы, где, по мнению большинства экономистов, наблюдается снижение экономического роста из-за Brexit. Акции PPL упали на 12% после голосования по Brexit.
Заботятся ли стоимостные инвесторы о рыночных катализаторах?
Среди различных групп инвесторов не все могут придавать первостепенное значение пониманию рыночных катализаторов.
 Например, стоимостные инвесторы обычно сосредотачиваются на внутренней стоимости компании по отношению к тому, где в настоящее время торгуются акции. Это стиль инвестирования, которого придерживается легендарный инвестор Уоррен Баффет. Ценные инвесторы заинтересованы в том, чтобы найти акции, которые стоят больше, чем их текущая рыночная цена, и не так сосредоточены на рыночных катализаторах.
Например, стоимостные инвесторы обычно сосредотачиваются на внутренней стоимости компании по отношению к тому, где в настоящее время торгуются акции. Это стиль инвестирования, которого придерживается легендарный инвестор Уоррен Баффет. Ценные инвесторы заинтересованы в том, чтобы найти акции, которые стоят больше, чем их текущая рыночная цена, и не так сосредоточены на рыночных катализаторах.Заботятся ли дивидендные инвесторы о рыночных катализаторах?
Однако дивидендные инвесторы могут увидеть преимущества в анализе рыночных катализаторов. Дивидендная доходность является одним из наиболее ценных показателей для дивидендных инвесторов. Он выражает годовой дивиденд компании в процентах от цены акций. Поскольку дивидендная доходность является функцией цены акции, рост цены акции снижает дивидендную доходность, и наоборот. В результате дивидендные инвесторы должны обращать внимание на потенциальные рыночные катализаторы в будущем, поскольку большие колебания цен на акции вызовут колебания дивидендной доходности, что повлияет на решение дивидендного инвестора.

