Принцип работы свинцово-кислотного аккумулятора.
Принцип работы свинцового аккумулятора
Источником электроэнергии на автомобиле при неработающем или работающем с малой частотой вращения коленчатого вала двигателе является аккумуляторная батарея. В настоящее время на автомобилях наиболее широко применяются свинцовые аккумуляторные батареи, состоящие из нескольких последовательно соединенных аккумуляторов. Применение кислотных аккумуляторов объясняется тем, что они обладают небольшим внутренним сопротивлением и способны в течение короткого промежутка времени (несколько секунд) отдавать ток силой в несколько сотен ампер, что необходимо для питания стартера при пуске двигателя.
Свинцовый аккумулятор электрической энергии был изобретен в 1859 году французским физиком Гастоном Планте. В последующие годы конструкция аккумулятора, особенно – химический состав его электродов (пластин) постоянно совершенствовалась. В настоящее время свинцовые аккумуляторы и аккумуляторные батареи широко применяются в разных областях техники в качестве накопителей электроэнергии (стартерные батареи, аварийные и резервные источники энергии и т. п.).
В настоящее время свинцовые аккумуляторы и аккумуляторные батареи широко применяются в разных областях техники в качестве накопителей электроэнергии (стартерные батареи, аварийные и резервные источники энергии и т. п.).
Конструктивно аккумулятор представляет собой емкость, наполненную электролитом, в которой размещены свинцовые электроды. В качестве электролита используется раствор серной кислоты и дистиллированной воды. Электроды выполнены в виде пластин, одна из которых изготовлена из губчатого свинца Pb, а вторая – из диоксида свинца PbO2. При взаимодействии электродов с электролитом между ними возникает разность потенциалов.
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в водном растворе серной кислоты.
При подключении к электродам аккумулятора внешней нагрузки начинается электрохимическая реакция взаимодействия оксида свинца и серной кислоты, при этом металлический свинец окисляется до сульфата свинца.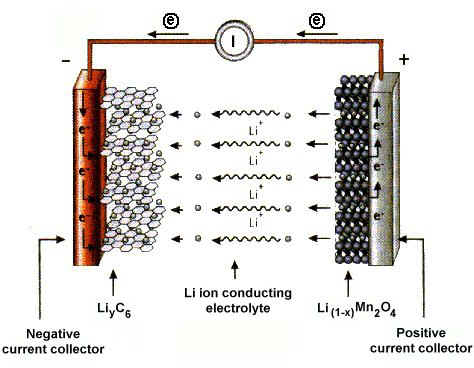
Во время разряда происходит восстановление диоксида свинца на положительном электроде (аноде) и окисление свинца на отрицательном электроде (катоде). При пропускании через электроды аккумулятора зарядного тока в нем протекают обратные реакции. При перезаряде аккумулятора, после исчерпания сульфата свинца начинается электролиз воды, при этом на аноде выделяется кислород, а на катоде — водород.
Электрохимические реакции (слева направо — при разряде, справа налево — при заряде):
Реакции на аноде:
PbO2 + SO42- + 4H+ + 2e— ↔ PbSO4 + 2H2O;
Реакции на катоде:
Pb + SO42- — 2e— ↔ PbSO4.
Физические процессы, происходящие в аккумуляторе, объясняются свойством электролитического растворения металлов, которое заключается в переходе положительно заряженных ионов металла в раствор. Легкоокисляющиеся металлы (например, свинец) обладают этим свойством в большей степени, чем инертные металлы.
При погружении свинцового электрода в раствор электролита от него начнут отделяться положительно заряженные ионы свинца и переходить в раствор, при этом сам электрод будет заряжаться отрицательно.
По мере протекания процесса растет разность потенциалов раствора и электрода, и переход положительных ионов в раствор будет замедляться.
При какой-то определенной разности потенциалов электрода и раствора наступит равновесие между силой электролитической упругости растворения свинца, с одной стороны, и силами электростатического поля и осмотического давления — с другой.
В результате переход ионов свинца в электролит прекратится.
При погружении электрода, изготовленного из двуокиси свинца, в раствор серной кислоты наблюдается такой же процесс, но результат получается иной. Двуокись свинца в ограниченном количестве переходит в раствор, где при соединении с водой ионизируется на четырехвалентные ионы свинца Рв4+ и одновалентные ионы гидроксила ОН.
Четырехвалентные ионы свинца, осаждаясь на электроде, создают положительный потенциал относительно раствора. Серная кислота образует в воде практически только на ионы НO+ и HSO4.
Таким образом, при разряде аккумулятора расходуется серная кислота, образуется вода, а на обоих электродах — сульфат свинца. При заряде процессы протекают в обратном направлении.
При подключении потребителей в аккумуляторе возникает разрядный ток. При этом ионы сернокислотного остатка SO4 соединяются со свинцом электродов и образуют на них сернокислый свинец
В результате электроды покрываются сернокислым свинцом, а серная кислота разбавляется водой, т. е. при разряде аккумулятора плотность электролита уменьшается. Поэтому по плотности электролита можно судить о степени заряженности аккумуляторной батареи.
При прохождении электрического (зарядного) тока через аккумуляторную батарею протекают обратные электрохимические процессы. Ионы водорода, образующиеся в результате распада воды, взаимодействуют с сернокислым свинцом электродов.
Водород, соединяясь с сернистым осадком, образует серную кислоту, а на электродах восстанавливается губчатый свинец. Выделяющийся из воды кислород, соединяется со свинцом положительной пластины, образуя перекись свинца.
По завершению процессов восстановления свинца на электродах заряд аккумулятора прекращается. При дальнейшем прохождении электрического тока через электролит начинается процесс электролиза (разложения) воды, при этом аккумулятор «закипает», и выделяющиеся пузырьки образуют смесь водорода и кислорода. Смесь этих газов является взрывоопасной, поэтому следует избегать перезаряда до появления электролизных явлений по разложению воды.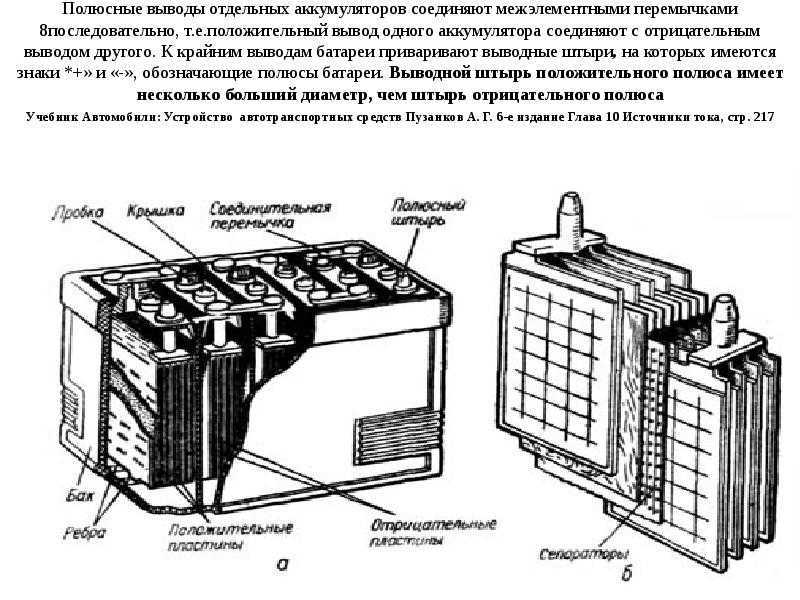
Кроме того, длительный перезаряд приводит к потере электролитом воды (испарению), в результате чего его плотность повышается и для корректировки требуется доливка дистиллированной воды.
При доливке воды необходимо помнить, что вода, попадающая в концентрированную серную кислоту, закипает и сильно разбрызгивает кислотные капли, что при попадании на открытое тело или одежду может привести к ожогам кожи, слизистых оболочек, прожигу одежды и другим неприятным последствиям.
При постоянном напряжении источника зарядного тока по мере увеличения степени заряженности аккумулятора повышается его ЭДС и, следовательно, уменьшается сила зарядного тока. Когда напряжение на клеммах источника тока будет равно ЭДС полностью заряженного аккумулятора плюс ЭДС поляризации, зарядный ток прекратится.
Среднее значение напряжения аккумулятора – 2 В. Поскольку электрооборудование современных автомобилей рассчитано для работы при напряжении в бортовой сети 12 или 24 В, аккумуляторы соединяют в батареи (по 6 или 12 шт. ).
).
Важным параметром аккумулятора является его емкость, т. е. количество электрической энергии, которую способен отдать аккумулятор. Емкость – это произведение силы разрядного тока на продолжительность разрядки до предельно допустимого разряженного состояния. Измеряется емкость аккумулятора в ампер-часах ( А×ч). Емкость аккумулятора зависит, в первую очередь, от активной площади его электродов.
Поэтому повышения емкости можно достичь увеличением поверхности электродов, что достигается использованием нескольких параллельно соединенных между собой пластин, а также применением пористого материала для их изготовления, что позволяет использовать в качестве активной массы не только поверхность, но и внутренний объем пластин.
Емкость аккумулятора не постоянна, она зависит от силы разрядного тока, температуры электролита и состояния активной поверхности пластин. При увеличении разрядного тока и понижении температуры электролита емкость аккумулятора уменьшается, что объясняется неполным протеканием электрохимических реакций разрядки в этих условиях, вследствие сокращения времени разрядки и повышения вязкости электролита при низких температурах.
***
Устройство аккумуляторной батареи и ее маркировка
Главная страница
- Страничка абитуриента
Дистанционное образование
- Группа ТО-81
- Группа М-81
- Группа ТО-71
Специальности
- Ветеринария
- Механизация сельского хозяйства
- Коммерция
- Техническое обслуживание и ремонт автотранспорта
Учебные дисциплины
- Инженерная графика
- МДК.01.01. «Устройство автомобилей»
- Карта раздела
- Общее устройство автомобиля
- Автомобильный двигатель
- Трансмиссия автомобиля
- Рулевое управление
- Тормозная система
- Подвеска
- Колеса
- Кузов
- Электрооборудование автомобиля
- Основы теории автомобиля
- Основы технической диагностики
- Основы гидравлики и теплотехники
- Метрология и стандартизация
- Сельскохозяйственные машины
- Основы агрономии
- Перевозка опасных грузов
- Материаловедение
- Менеджмент
- Техническая механика
- Советы дипломнику
Олимпиады и тесты
- «Инженерная графика»
- «Техническая механика»
- «Двигатель и его системы»
- «Шасси автомобиля»
- «Электрооборудование автомобиля»
Теория работы свинцово-кислотного аккумулятора 🔋
В свинцово-кислотном аккумуляторе основные продукты реакции, происходящие между положительным и отрицательным электродами аккумулятора в водном растворе серной кислоты, подчиняются так называемой теории двойной сульфатации в соответствии с уравнением:
⇐ заряд Pb + PbO2 + 2H2SO4 ⇐ ⇒ 2PbSO4 + 2H2 O (1) разряд ⇒
Этому соотношению подчиняется взаимодействие активных веществ в аккумуляторе во время разряда, заряда, подзаряда, а также во время бездействия (холостого хода).
Основные соотношения между реагентами при бездействии (при разомкнутой внешней цепи аккумулятора) определяются следующими реакциями:
— на отрицательном электроде:
2H+ + 2e- ⇒ H2↑ анодная полуреакция
Pb + SO42- ⇒ PbSO4 + 2e- катодная полуреакция
Pb + H2 SO4 ⇒ PbSO4 + H2↑ общая реакция (2)
— на положительном электроде:
PbO2 + 4H+ + SO42- + 2e- ⇒ PbSO4 + 2H2 O катодная полуреакция
H2 O ⇒ 1/2 O2 ↑ + 2H+ + 2e- анодная полуреакция
PbO2 + H2 SO4 + H2O ⇒ PbSO4 + 2H2 O + 1/2 O2↑ общая реакция (3)
Приведенные уравнения реакций на отрицательном и положительном электродах показывают, что даже при разомкнутой внешней цепи аккумулятора в нем происходит образование сульфата свинца на обоих электродах, снижение плотности электролита, а также разложение воды с выделением газообразных водорода и кислорода, что приводит, таким образом, к снижению емкости аккумулятора, т. е. к саморазряду. Объем продуктов этих реакций зависит от концентрации серной кислоты (плотности электролита), температуры, состава сплава решеток и активной массы электродов, возраста аккумулятора и других причин.
е. к саморазряду. Объем продуктов этих реакций зависит от концентрации серной кислоты (плотности электролита), температуры, состава сплава решеток и активной массы электродов, возраста аккумулятора и других причин.
При подключении к аккумулятору нагрузки токообразующий процесс подчиняется уравнению (1) для фазы разряда. На отрицательном электроде (на границе раздела свинец — сульфат свинца) происходит образование электронов, поступающих во внешнюю цепь:
Pb ⇒ Pb2+ + 2e-
На положительном электроде на границе раздела окись свинца -сульфат свинца происходит поглощение электронов, поступающих через замкнутую внешнюю цепь, и образование воды:
PbO2 + 4H+ + 2e- ⇒ Pb2+ + 2H2 O
Анионы свинца , связываясь с кислотным остатком, образуют на обоих электродах сульфат свинца, покрывающий поверхность активных масс пластин. По мере разряда концентрация серной кислоты в электролите убывает.
По мере разряда концентрация серной кислоты в электролите убывает.
₽20 590
В корзину
₽16 190
В корзину
₽15 990
В корзину
При подключении аккумулятору зарядного устройства токообразующий процесс проходит согласно уравнению (1) для фазы заряда.
На отрицательном электроде анионы свинца, образованные из сульфата свинца при растворении в электролите, связываются с электронами, поступающими из внешней цепи, образуя чистый (губчатый) свинец:
Pb2+ + 2e- ⇒ Pb
На положительном электроде процесс протекает согласно реакции (4) с образованием на электроде окиси свинца и отдачи во внешнюю цепь электронов:
Pb2+ + 2H2 O ⇒ PbO2 + 4H+ + 2e- (4)
По мере заряда увеличивается напряжение поляризации аккумулятора, и, когда оно превысит величину перенапряжения по кислороду, на положительном электроде начинает выделяться кислород:
2OH— ⇒ 1/2 O2↑ + H2 O + 2e-
Когда напряжение поляризации превысит величину перенапряжения по водороду, на положительном электроде начинается образование водорода:
2H+ + 2e- ⇒ H2↑
Таким образом, при заряде наряду с образованием на электродах исходных продуктов (свинца и окиси свинца) происходит повышение плотности электролита за счет восстановления серной кислоты, а на последней стадии заряда при повышенном напряжении часть подводимого электричества идет на разложение воды:
H2 O ⇒ H2↑ + 1/2 O2↑
Из других побочных реакций на положительном электроде при заряде следует обратить внимание на образование озона и на окисление (коррозию) решетки, что оказывает решающее влияние на сокращение срока службы аккумулятора.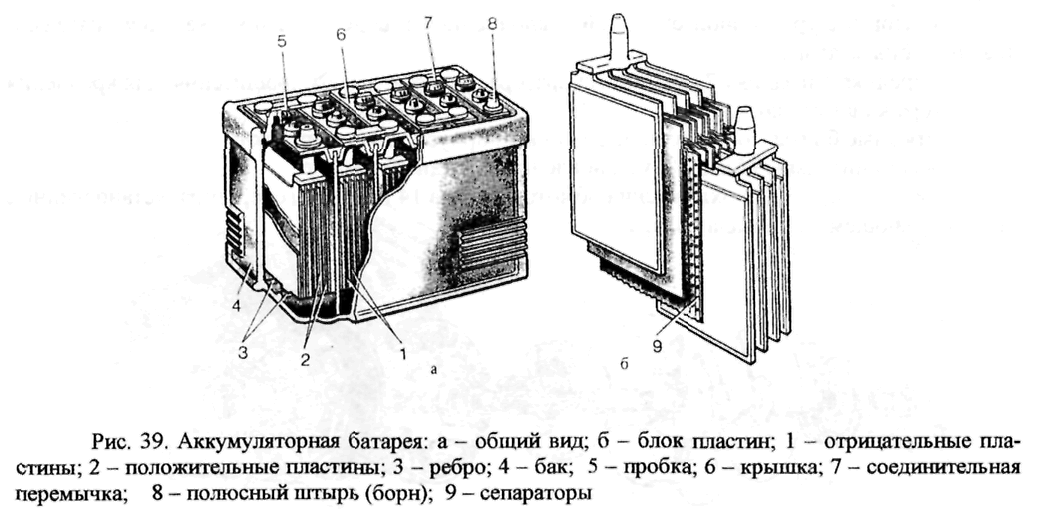
С уважением,
коллектив Бэттери Сервис
Устройство и параметры свинцово-кислотных аккумуляторов — принцип работы
Основная доля на рынке по-прежнему остается у свинцово-кислотных аккумуляторов. Это обусловлено простотой конструкции и невысокой ценой. Применяемых в них принцип используется многие десятки лет, но со временем он претерпевает разные изменения по увеличению емкости, росту энергетических характеристик и долговечности. Так, например, введение в свинцовый сплав легирующих добавок привело к росту многих практических показателей. Рассмотрим подробнее свинцовый аккумулятор и разберемся с особенностями его работы на химическом и физическом уровнях.
Конструкция АКБ
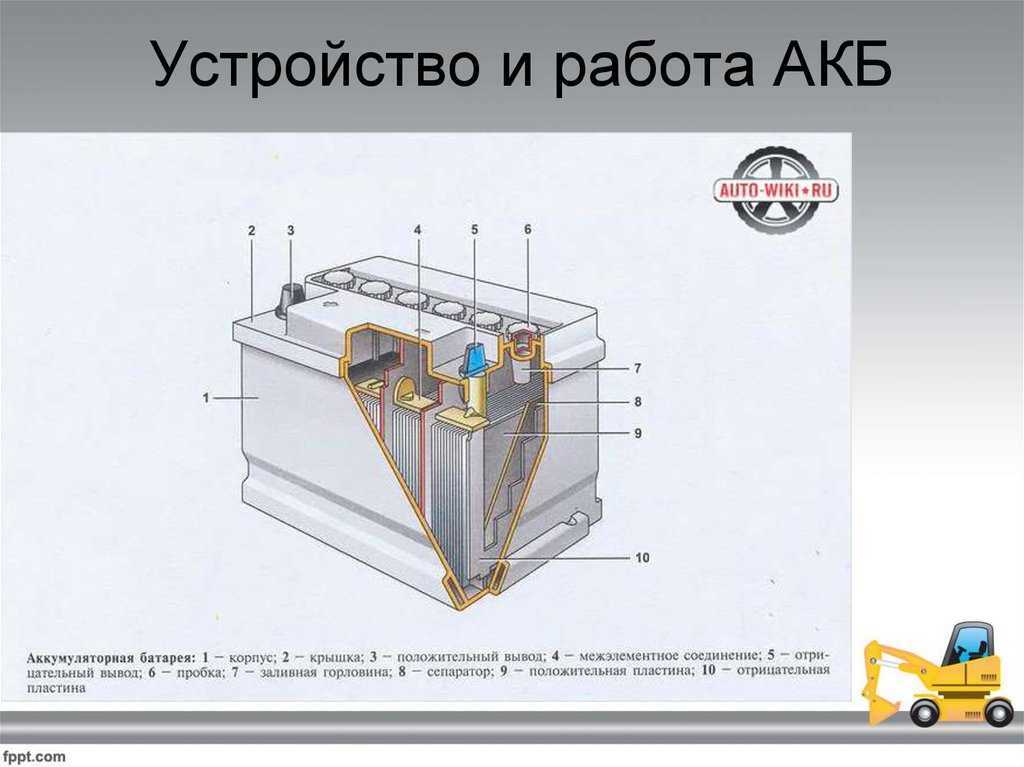
Устройство свинцово-кислотного аккумулятора не является загадкой. Условно в его конструкции имеется всего три компонента. Это корпус, энергетические ячейки и электролит, но, казалось бы, такое простое устройство постоянно изменяется, водятся какие-то добавки и дополнительные элементы, способствующие росту характеристик. Рассмотрим более подробно, из чего состоит аккумулятор:
Рассмотрим более подробно, из чего состоит аккумулятор:
- Снаружи имеется защитная герметичная оболочка, изготовленная из прочного кислотостойкого пластика. Внутри она разделена на отсеки, в каждой из которых находится электродная пара. Для повышения прочности корпус оснащен внутренними ребрами жесткости. Он должен быть герметичным, так как внутренняя среда способна сильно навредить окружающей. В самых бюджетных модификациях аккумуляторов типа WET также присутствуют пробки для доливки жидкости.
- В каждой ячейке находятся электродные решетки. Они представляют собой пары разнополюсных пластин, которые чередуются. Положительные и отрицательные закреплены к токовым шинам. Электроды — в виде решеток с окном определенного размера и формы. В ранних моделях батарей их изготавливали методом литья под высоким давлением. В современных для введения легирующих добавок их производят методом штампования и ковки. Введение сурьмы и кальция увеличили стойкости к глубоким разрядам, отдачи высоких токов и продлению срока службы.

- В электродных решетках содержится активная паста. На положительных — оксид свинца, на отрицательных — губчатая свинцовая масса. Активная паста накапливает заряд и обеспечивает свободное перемещение электронов между пластинами. Один из электродов изолировано сепаратором, необходимый для исключения возникновения короткого замыкания между банками, когда начнет обсыпаться активная паста.
- В конструкции свинцового аккумулятора имеется 6 энергетических ячеек, которые соединены последовательно. Это сделано для того, чтобы получилось требуемое напряжение 12 В, потому что одна ячейка выдает всего 2 В. Токосъемные электроды вынесены в крышку корпуса батареи. Могут быть в виде конусовидных клемм, лепестков, болтов или углублений под болты. В зависимости от страны производителя и первоначального назначения, АКБ могут быть оборудованы клеммами сверху или на боковой стороне.
Особенности корпуса
Корпус, как и конфигурация клемм, бывает нескольких типов в зависимости от того, для какой машины страны был изготовлен источник постоянного тока. Можно разделить:
Можно разделить:
- на американские с резьбовыми клеммами;
- европейские с технологическим выступом для фиксации на штатном месте в нижней и верхней части;
- азиатские без выступов и клеммы выступают за пределы крышки, что указывает на особенности подключения батареи.
В моделях EFB-типа, это усовершенствованные классические свинцово-кислотные аккумуляторы, применена технология рециркуляции испарений электролита. Сам при этом источник тока считается необслуживаемым, то есть в него не нужно добавлять жидкость. Обычно электролит испаряется во время заряда батареи постоянным током или при потреблении больших токов. Это приводит к нагреву, и кислота начинает испаряться. Поднимаемый пар оседает на внутренней стороне крышки и охлаждается там, обратно сворачиваясь в жидкость и возвращаясь обратно в корпус.
На случай, если внутреннее давление критически возрастет, автоматически откроется спускной клапана. Он есть не на всех моделях батарей, но на всех современных источниках. Его наличие позволяет исключить возникновение аварии в случае перегрева или перегрузки.
Его наличие позволяет исключить возникновение аварии в случае перегрева или перегрузки.
Легирование пластин
В общем, конструкция всех модификаций свинцово-кислотных автомобильных аккумуляторов одинаковая. Это касается как стартерных, так и тяговых с большими рабочими токами, которые могут генерироваться в течение длительного времени. Несовершенство первой свинцово-кислотной аккумуляторной батареи было связано со множеством проблем:
- коррозия электродов;
- высокая чувствительность к глубоким разрядам;
- саморазряд;
- утечка электролита и его проникновение опасных испарений в окружающую атмосферу;
- малый срок службы и др.
Все это искоренить, конечно, не получается по многочисленным причинам, но несколько продлить срок эксплуатации АКБ, увеличить отдаваемый ею ток реально. Для этого разработчики стали экспериментировать с составом активной пасты, конструкцией электродов и сплавом, из которого они изготовлены.
В результате проб и ошибок было определено, что в сплав следует добавлять сурьму и кальций. Такой источник получил название гибридный. Сурьма снизила чувствительность к глубоким разрядам, а кальций продлили срок службы, так как он препятствует разрушению свинца. А для получения больших токов в производстве аккумуляторов применяют чистый свинцовый сплав. Чем меньше в нем примесей, тем больше энергии, но в чистом виде он разрушается быстрее.
Применяют следующие типы легирования:
- сурьма-свинец;
- сурьма-кальций;
- кальций-кальций;
- серебро-кальций.
Электродные решетки изготавливают цельнолитыми, то есть, льют в форму под высоким давлением и штампованными. В первом случае из-за высоких температур возможно легирование только добавление сурьмы. Она придает пластинам повышенную прочность и при ее введении электролит начинает закипать уже при 12 В. Для продления срока службы и сохранения высоких токов отдачи в свинцовый сплав стали добавлять кальций.
Такие решетки производятся преимущественно методом штампования. Второй электрод остается сурьмянистым. Комбинация металлов увеличивает срок службы и отдаваемее токи. Так, например, обычной свинцово-кислотный аккумулятор с сурьмянистым легированием работает не более 3 лет. Аккумуляторы с кальцием и сурьмой служат вдвое дольше, поэтому и дороже.
Электролит
В свинцово-кислотных аккумуляторах производители применяют 3 типа электролита в зависимости от его состояния:
- Жидкий — привычный всем раствор серной кислоты. Батареи токсичны при зарядке и опасны при аварии, так как кислота попадет в окружающую атмосферу.
- В капиллярном виде в абсорбере. Он представляет собой пористый материал со множеством пустот, которые заполняются кислотой. Так как материал пропитан, то даже при повороте источника постоянного тока вверх ногами батарея не перестанет работать.
- Гелеобразный — тип электролита в виде оксида кремния. Это густая малоподвижная масса, которая надежно обволакивает пластины со всех сторон, обеспечивая максимальный контакт и токоотдачу.
 Именно поэтому эти батареи обладают самыми высокими пусковыми токами и огромным сроком службы. Производитель заявляет о 12 годах работы.
Именно поэтому эти батареи обладают самыми высокими пусковыми токами и огромным сроком службы. Производитель заявляет о 12 годах работы.
Принцип работы
Работа автомобильного свинцово-кислотного аккумулятора основан на двойном преобразовании. В процессе зарядки электрическая энергия в виде тока и напряжения преобразуется в химическую. Во время штатной работы процесс оборачивается, и химическая реакция выделяет ток на зажимах при замыкании цепи. Во время заряда происходит процесс восстановления пластин АКБ и заполнения пустых ест в активной пасте положительно заряженными на плюсовом контакте и отрицательно заряженными частицами на минусовом.
Когда пользователь смыкает цепь, начинается преобразование химической энергии в электрическую, то есть, положительные частицы переходят на отрицательную обкладку с выделением определенного количества энергии через нагрузку. Величина этой энергии и ток зависят от сопротивления в нагрузке.
Пластины
Казалось бы, такая часть АКБ, как электродная пластина, может разнится от одной линейки батареи к другой. Существует две основных технологии производства пластин, но также есть и разные архитектурные решения, которые неизбежно влияют на работу батареи в целом. Простая прямоугольная решетка уже давно не используется. Применяют лучевые конструкции, так как при такой конфигурации токи лучше распределяются по пластине, обеспечивая ее равномерную выработку. В производстве применяются следующие технологии:
Существует две основных технологии производства пластин, но также есть и разные архитектурные решения, которые неизбежно влияют на работу батареи в целом. Простая прямоугольная решетка уже давно не используется. Применяют лучевые конструкции, так как при такой конфигурации токи лучше распределяются по пластине, обеспечивая ее равномерную выработку. В производстве применяются следующие технологии:
- Expandet metal — штамповка с просечкой и вытягиванием;
- Power Frame — в конструкции таких пластин присутствует опорная рамка, внутри которой находятся тонкие жилки.
- Power Pass — в такой архитектуре вертикально расположенные жилки направлены к ушкам пластин.
- Chess Plate — применена шахматная архитектура устройства пластин.
Что такое сульфация?
Важно знать о том, что свинцово-кислотные аккумуляторы со временем изнашиваются. В них появляется выработка, а на пластинах возникают различные наросты. Одним из подобных состояний является сульфация пластин. Он возникает в результате окисления активной пасты в результате длительного нахождения в разряженном состоянии. Белый налет становится настоящим диэлектриком, через который электроны неспособны просочиться. Данное состояние присуще батареям, которые регулярно разряжаются до 80% от начального состояния и долго находятся в таком виде. Существует технология удаления этого налета. Она заключается в зарядке импульсными зарядными и разрядными токами.
Он возникает в результате окисления активной пасты в результате длительного нахождения в разряженном состоянии. Белый налет становится настоящим диэлектриком, через который электроны неспособны просочиться. Данное состояние присуще батареям, которые регулярно разряжаются до 80% от начального состояния и долго находятся в таком виде. Существует технология удаления этого налета. Она заключается в зарядке импульсными зарядными и разрядными токами.
Какой аккумулятор устанавливается на Mazda 6 GG >
Устройство свинцово-кислотного аккумулятора и принцип его работы
Аккумуляторные батареи являются неотъемлемым атрибутом любого современного транспортного средства. Они вырабатывают энергию, необходимую для пуска двигателя внутреннего сгорания, а в гибридных электрокарах выступают ещё и движущей силой. Несмотря на постоянно продолжающиеся разработки, свинцово-кислотные батареи остаются одними из самых распространённых на рынке.
Устройство свинцово-кислотного аккумулятора
Конструкция батареи свинцово-кислотного типа кардинально отличается от других устройств, предназначенных для выработки пускового тока и питания электроприборов.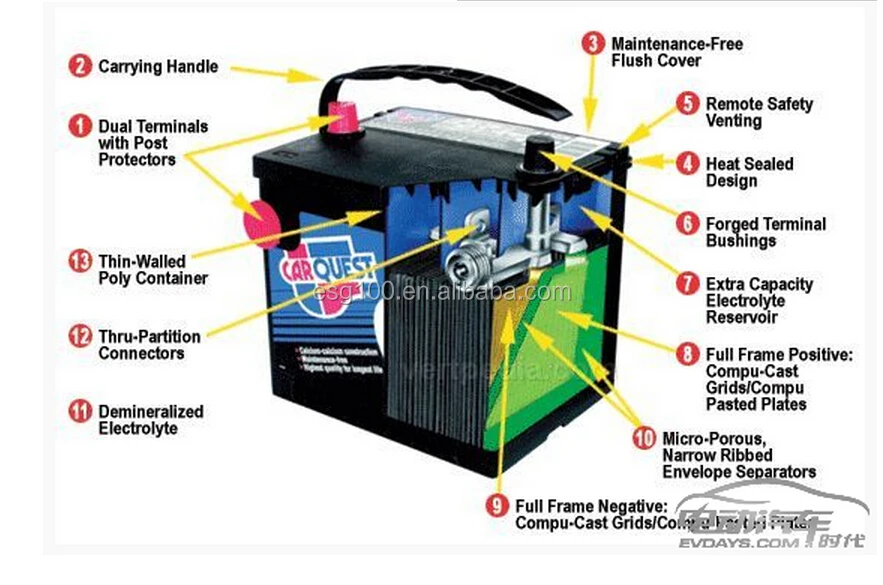 Хотя в самой сути лежат химические процессы и электролиз. Диоксид свинца и чистый свинец вступают во взаимодействие с раствором серной кислоты.
Хотя в самой сути лежат химические процессы и электролиз. Диоксид свинца и чистый свинец вступают во взаимодействие с раствором серной кислоты.
Устройство АКБ такого типа можно описать химическими процессами: в ходе нагрузки происходит образование сульфата свинца. В это время этот металл окисляется на аноде, а на катоде восстанавливается его диоксид. В процессе заряда протекают противоположные реакции. На пластинах располагается сульфат свинца: он распадается, а на аноде снова восстанавливается чистый свинец. Благодаря этим несложным химическим процессам есть возможность многократно использовать батарею, то разряжая, то заряжая её повторно.
Но в составе каждого автомобильного аккумулятора присутствует такой рабочий элемент, как электролит — это жидкость, пропускающая электрический ток. Если зарядка длится слишком долго, то сульфата свинца становится всё меньше, и начинается процесс электролиза. Обилие пузырьков приводит к закипанию дистиллированной воды внутри батареи. Допускать такое явление не рекомендуется, потому что возрастает угроза взрыва.
Производители закладывают такую опцию, как постепенное снижение величины заряда на клеммах по мере возрастания напряжения. Также существует угроза потери дистиллята, но её восполняют периодической доливкой. Одним из самых важных критериев аккумуляторных батарей выступает их ёмкость. Аккумулятор устроен таким образом, чтобы отдавать электрическую энергию, и в этом его самое главное предназначение. Чем больше ёмкость, тем большим количеством энергии он делится с потребителями тока.
Измеряется ёмкость в ампер-часах и зависит от активной площади электродов каждой батареи. Чтобы добиться увеличения этого критерия, можно использовать несколько соединённых между собой пластин, выполняющих роль электродов. Их могут изготавливать из пористых материалов, что тоже приносит положительный эффект. Проводить ток в этом случае может не только поверхность, но и внутренняя структура. Ёмкость не является постоянным фактором, она зависит от других обстоятельств: силы разрядного тока, состояния, в котором находятся пластины, температуры рабочей жидкости. Если температура понижается, ёмкость автоматически тоже уменьшится, поскольку вязкость электролита будет снижена, и электрохимические реакции протекают в таких условиях труднее.
Если температура понижается, ёмкость автоматически тоже уменьшится, поскольку вязкость электролита будет снижена, и электрохимические реакции протекают в таких условиях труднее.
Принцип работы автомобильного аккумулятора
Популярность кислотных аккумуляторов основывается на особенностях их работы и эксплуатационных характеристиках. Небольшое внутреннее сопротивление позволяет им выдавать ток на несколько сотен ампер, а именно это требуется стартеру для того, чтобы запустить двигатель внутреннего сгорания. Постоянное совершенствование автомобильного аккумулятора, который был изобретён ещё в 19-м веке, привело к тому, что в настоящее время он широко применяется в различных областях машиностроения.
В основе конструкции такой батареи лежит комплект свинцовых электродов. Все они расположены в одном и том же рабочем корпусе, залитом электролитом. Основу электролита составляет раствор на основе серной кислоты и дистиллированной воды. Для устройства пластин используется губчатый свинец, а также диоксид этого металла. Между пластинами возникает электрический разряд при взаимодействии электродов и жидкости-электролита.
Между пластинами возникает электрический разряд при взаимодействии электродов и жидкости-электролита.
Свинец с диоксидом свинца находятся в водяном растворе серной кислоты и вступают в реакцию друг с другом — на этом основывается принцип работы всех батарей этого типа. Сначала чистый свинец окисляется до сульфата этого металла. В процессе работы АКБ происходит её разряд — в химической реакции это находит своё отражение следующим образом: на аноде диоксид свинца восстанавливается, а на катоде происходит окисление свинца. Как только через электроды начинает проходить ток, химические реакции будут обратно противоположными.
Типы и особенности свинцово кислотных акб
Свинцово-кислотная технология позволила воплотить в жизнь различные виды автомобильных аккумуляторных батарей, которые обладают своими особенностями и преимуществами. Среди наиболее распространённых можно выделить следующие:
- Жидкостные. Они нуждаются в обслуживании, но являются самыми экономичными.
 Электролит находится в жидкой форме, поэтому контактировать с ним без специальной защиты опасно для здоровья. Рассчитаны на 250–500 циклов заряда.
Электролит находится в жидкой форме, поэтому контактировать с ним без специальной защиты опасно для здоровья. Рассчитаны на 250–500 циклов заряда. - EFB. Имеют лучшие рабочие характеристики по сравнению с жидкостным типом. Количество циклов заряда и разряда может достигать 1000. Также требуют периодического обслуживания.
- Гелевые. Не нуждаются в обслуживании. Кроме увеличенного рабочего ресурса, отличаются меньшим испарением электролита, который находится в гелеобразном состоянии. Хорошо выдерживают внешние удары и вибрации.
- AGM. Одна из самых прогрессивных технологий, предполагающая установку стекловолоконных разделителей, которые накапливают электричество. Они вырабатывают более сильный ток, а заряжаются в 5 раз быстрее.
Преимущества и недостатки свинцово кислотных аккумуляторов
Свинцово-кислотные батареи получили широкое распространение благодаря свой конструкции и эксплуатационным параметрам. Они сравнительно дешевле по отношению к изделиям на основе других химических элементов и отлично подвергаются утилизации. Именно способность к восстановлению позволила аккумуляторам этого типа вытеснить аналоги, ведь уровень повторного применения свинца в ряде государств превышает 98%.
Именно способность к восстановлению позволила аккумуляторам этого типа вытеснить аналоги, ведь уровень повторного применения свинца в ряде государств превышает 98%.
Для того чтобы правильно оценить плюсы и минусы свинцово-кислотного аккумулятора, необходимо учитывать их характеристики, которые важны в процессе эксплуатации. В числе главных преимуществ свинцово-кислотных устройств для производства тока стоит выделить следующие характеристики:
- длительная сохранность заряда по сравнению с оборудованием, принцип работы которого основан на других химических элементах;
- сравнительно простая технология производства позволяет удешевить итоговую стоимость для потребителя;
- эксперты отмечают простоту и неприхотливость в пользовании устройствами этой конструкции;
- отсутствие необходимости в доливке рабочей жидкости;
- высокий пусковой ток, который необходим для ряда транспортных средств.
Наряду с широким перечнем достоинств, аккумуляторы свинцово-кислотного типа обладают и недостатками, которые необходимо учитывать перед их приобретением. Основные недостатки такого оборудования:
Основные недостатки такого оборудования:
- экологические риски, которые АКБ могут причинить окружающей среде, и необходимость обязательной повторной утилизации;
- возможный перегрев батареи в случае неправильного процесса заряда;
- рассчитаны на определённое количество циклов заряда и разряда.
- для хранения батареи должны быть всегда заряженными;
- невысокая энергетическая плотность приводит к проблемам в эксплуатации на стационарных объектах;
- повышенная кислотность электролита негативно сказывается на окружающей среде;
- рассчитаны на определённое количество циклов заряда и разряда;
- перегрев и перезаряд АКБ отрицательно сказываются на её рабочих характеристиках.
Области применения свинцово кислотных аккумуляторов
Применяют батареи, созданные по данной технологии, уже почти 200 лет. Многим потребителям они предпочтительны благодаря невысокой стоимости изготовления, а ещё долговечности. Такое оборудование способно производить высокий пусковой ток, необходимый ряду транспортных средств и оборудования. Основное применение свинцово-кислотных АКБ — это автомобили и механизмы, но есть и другие сферы:
Многим потребителям они предпочтительны благодаря невысокой стоимости изготовления, а ещё долговечности. Такое оборудование способно производить высокий пусковой ток, необходимый ряду транспортных средств и оборудования. Основное применение свинцово-кислотных АКБ — это автомобили и механизмы, но есть и другие сферы:
- системы охраны и сигнализаций;
- оборудование для аварийного энергоснабжения и освещения;
- контрольно-измерительные приборы;
- ИБП для компьютерной техники;
- инвалидные кресла;
- детские электромобили и пр.
Источники питания этого типа продолжают оставаться востребованными благодаря высокой ёмкости, небольшому саморазряду и низкому внутреннему сопротивлению.
Свинцово-кислотный аккумулятор | это… Что такое Свинцово-кислотный аккумулятор?
Автомобильный свинцово-кислотный аккумулятор
См. также: Автомобильный аккумулятор
Свинцово-кислотный аккумулятор — наиболее распространенный на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: аккумуляторные батареи в автомобильном транспорте, аварийные источники электроэнергии.
Основные области применения: аккумуляторные батареи в автомобильном транспорте, аварийные источники электроэнергии.
Содержание
|
История
Свинцовый аккумулятор разработал в 1859—1860 годах Гастон Планте, сотрудник лаборатории Александра Беккереля. В 1878 году Камилл Фор усовершенствовал его конструкцию, покрыв пластины аккумулятора свинцовым суриком.
Принцип действия
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислотной среде.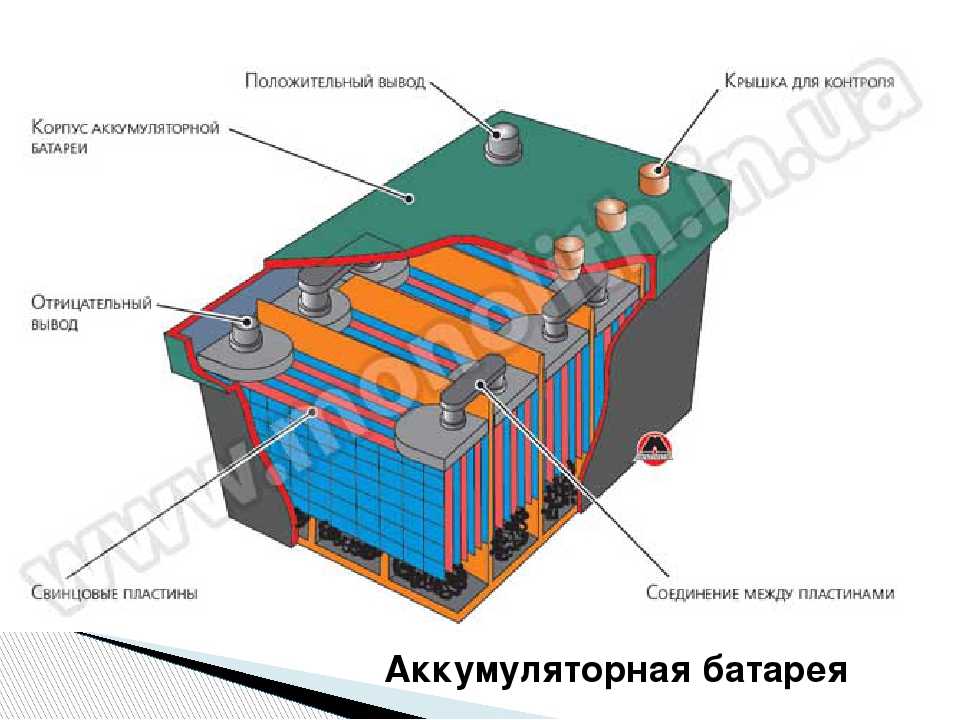
Энергия возникает в результате взаимодействия оксида свинца и серной кислоты до сульфата (классическая версия). Проведенные в СССР исследования показали, что внутри свинцового аккумулятора протекает как минимум ~60 реакций, порядка 20 из которых протекают без участия кислоты электролита (нехимические)[1]
Во время разряда происходит восстановление диоксида свинца на катоде[2][1] и окисление свинца на аноде. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном.
Химическая реакция (слева направо — разряд, справа налево — заряд):
- Анод:
- Катод:
В итоге получается, что при разряде аккумулятора расходуется серная кислота из электролита (и плотность электролита падает, а при заряде, серная кислота выделяется в раствор электролита из сульфатов, плотность электролита растёт). В конце заряда, при некоторых критических значениях концентрации сульфата свинца у электродов, начинает преобладать процесс электролиза воды. При этом на катоде выделяется водород, на аноде — кислород. При заряде не стоит допускать электролиза воды, в противном случае необходимо её долить для восполнения потерянного в ходе электролиза количества.
В конце заряда, при некоторых критических значениях концентрации сульфата свинца у электродов, начинает преобладать процесс электролиза воды. При этом на катоде выделяется водород, на аноде — кислород. При заряде не стоит допускать электролиза воды, в противном случае необходимо её долить для восполнения потерянного в ходе электролиза количества.
Устройство
Элемент свинцово-кислотного аккумулятора состоит из электродов (положительных и отрицательных) и разделительных изоляторов (сепараторов), которые погружены в электролит. Электроды представляют собой свинцовые решётки. У положительных активным веществом является перекись свинца (PbO2), у отрицательных активным веществом является губчатый свинец.
На самом деле электроды выполнены не из чистого свинца, а из сплава с добавлением сурьмы в количестве 1-2 % для повышения прочности и примесей. Иногда в качестве легирующего компонента используются соли кальция, в обеих пластинах, или только в положительных. Применение солей кальция вносит не только положительные но и много отрицательных моментов в эксплуатацию свинцового аккумулятора, например, у такого аккумулятора при глубоких разрядах существенно и необратимо снижается емкость.
Электроды погружены в электролит, состоящий из разбавленной дистиллированной водой серной кислоты (H2SO4). Наибольшая проводимость этого раствора наблюдается при комнатной температуре (что означает наименьшее внутреннее сопротивление и наименьшие внутренние потери) и при его плотности 1,23 г/см³
Однако на практике, часто в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29 −1,31 г/см³.
Существуют экспериментальные разработки аккумуляторов где свинцовые решетки заменяют вспененным карбоном, покрытым тонкой свинцовой пленкой. Используя меньшее количество свинца и распределив его по большой площади, батарею удалось сделать не только компактной и легкой, но и значительно более эффективной — помимо большего КПД, она заряжается значительно быстрее традиционных аккумуляторов.[3]
В батареях для бытовых ИБП жидкий электролит сгущают водным щелочным раствором силикатов натрия (Na2Si2O4)жидкое стекло до пастообразного состояния.
Физические характеристики
Аккумулятор электромобиля
- Теоретическая энергоёмкость (Вт·ч/кг): около 133.
- Удельная энергоёмкость (Вт·ч/кг): 30-60.
- Теоретическая удельная энергоплотность (Вт·ч/дм³): 1250.[4]
- ЭДС заряжённого аккумулятора = 2,11 — 2,17 В, рабочее напряжение = 2 В (3 или 6 секций в итоге дают стандартные 6 В или 12 В (12 В)).[1]
- Напряжение полностью разряженного аккумулятора = 1,75 — 1,8 В (из расчета на 1 секцию). Ниже разряжать их нельзя.[1]
- Рабочая температура: от −40 °C до +40 °C.
- КПД: порядка 80-90 %
Эксплуатационные характеристики
- Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде[5] малым током (1/20 номинальной емкости, выраженной в А*ч).
- Стартерный ток (для автомобильных аккумуляторов).
 Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев замеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики[6] замера отличаются, главным образом, допускаемым конечным напряжением.
Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев замеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики[6] замера отличаются, главным образом, допускаемым конечным напряжением. - Резервная емкость (для автомобильных аккумуляторов). Характеризует время, в течение которого аккумулятор может отдавать ток 25А до конечного напряжения 10,5В согласно ГОСТ Р 53165-2008[7].
Эксплуатация
Ареометр может быть использован для проверки удельного веса электролита каждой секции
При эксплуатации «обслуживаемых» аккумуляторов (с открываемыми крышками над банками) на автомобиле при движении по неровностям неизбежно происходит просачивание проводящего электролита на корпус аккумулятора. Во избежание сильного саморазряда необходимо периодически нейтрализовывать электролит протиранием корпуса, например слабым раствором пищевой соды или разведенным в воде до состояния консистенции жидкой сметаны хозяйственным мылом. Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита, что увеличивает его плотность, увеличивая напряжение на аккумуляторе, и может оголить свинцовые пластины. Поэтому необходимо следить за уровнем электролита и своевременно доливать дистиллированную воду.
Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита, что увеличивает его плотность, увеличивая напряжение на аккумуляторе, и может оголить свинцовые пластины. Поэтому необходимо следить за уровнем электролита и своевременно доливать дистиллированную воду.
Такие нехитрые операции вместе с проверкой автомобиля на утечку тока и периодической подзарядкой аккумулятора могут на несколько лет продлить срок эксплуатации батареи.
Свинцово-кислотный аккумулятор при низких температурах
По мере снижения окружающей температуры, параметры аккумулятора ухудшаются, однако в отличие от прочих типов аккумуляторов, свинцово-кислотные снижают их относительно медленно, что не в последнюю очередь обусловило их широкое применение на транспорте. Считается что свинцово-кислотный аккумулятор теряет ~1% ёмкости на каждый градус от +20°C. Т.е. в -30°C свинцово-кислотный аккумулятор будет иметь 50% ёмкости.
Снижение ёмкости и токоотдачи при низких температурах обусловлено, в первую очередь, ростом вязкости электролита, который уже не может в полном объёме поступать к электродам, и вступает в реакцию лишь в непосредственной близости от них, быстро истощаясь.
Не полностью заряженный аккумулятор в мороз может раздуться из-за замерзания электролита низкой плотности (близкой к 1.10)
Хранение
Свинцово-кислотные аккумуляторы необходимо хранить только в заряжённом состоянии. При температуре ниже −20 °C заряд аккумуляторов должен проводиться постоянным напряжением 2,45 В/секцию 1 раз в год в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/секцию в течение 6-12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи и накипи на поверхности аккумулятора создаёт проводник для тока от одного контакта к другому и приводит к саморазряду аккумулятора,после чего начинается преждевременная сульфатизация пластин и поэтому поверхность аккумулятора необходимо поддерживать в чистоте. Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные циклы, то есть разряд-заряд токами номинальной величины.
Износ свинцово-кислотных аккумуляторов
При использовании технической серной кислоты и не дистиллированной воды, ускоряются саморазряд, сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи.[8]
В результате каждой реакции образуется нерастворимое вещество — сернокислый свинец PbSO4, осаждающийся на пластинах, который образует диэлектрический слой между токоотводами и активной массой. Это один из факторов, влияющий на срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
- сульфатация пластин[1], заключающаяся в образовании крупных кристаллитов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
- коррозия электродов, то есть электрохимические процессы окисления и растворения в электролите, что вызывает осыпание материала электродов;
- слабая механическая прочность или плохое сцепление активной массы с токоотводами, что приводит к опаданию активной массы;[9][1]
- оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности.
 [1]
[1]
Хотя батарею, вышедшую из строя по причине физического разрушения пластин, самому починить нельзя, некоторые источники описывают химические растворы и прочие способы способные «десульфатировать» пластины. Простой но вредный для жизни аккумулятора способ предполагает использование раствора сульфата магния.[1] Раствор заливается в секции после чего батарею разряжают и заряжают несколько раз. Сульфат свинца и прочие остатки химической реакции осыпаются при этом на дно батареи, что может привести к замыканию секции поэтому обработанные секции желательно промыть и заполнить новым электролитом номинальной плотности. Это позволяет несколько продлить срок использования устройства. Если батарея имеет одну или несколько секций которые не работают (то есть не дают 2.17 вольта — например если корпус имеет трещины) возможно соединить две (или больше) батареи последовательно: к плюсовому контакту первой батареи подключаем плюсовой провод потребителя, к минусовому контакту второй батареи — минусовой провод потребителя, а две оставшихся контакта батареи соединяются кабелем. Такая батарея имеет суммарное напряжение работающих секций и поэтому количество работающих секций должно быть не более шести — то есть необходимо слить электролит из излишних секций. Такой вариант подходит для транспортных средств с большим моторным отсеком.
Такая батарея имеет суммарное напряжение работающих секций и поэтому количество работающих секций должно быть не более шести — то есть необходимо слить электролит из излишних секций. Такой вариант подходит для транспортных средств с большим моторным отсеком.
Вторичная переработка
Кодовый символ указывающий, что свинцовые батареи могут быть вторично переработаны
См. также: Вторичная переработка отходов
Вторичная переработка для этого вида аккумуляторов играет важную роль, так как свинец, содержащийся в аккумуляторах является тяжелым металлом и наносит серьёзный вред при попадании в окружающую среду. Свинец и его соли должны быть переработаны на специальных предприятиях для возможности его вторичного использования.
Выброшенные аккумуляторы часто используются как источник свинца для кустарной переплавки, например, в рыболовные грузила, дробь или гири. Для этого из аккумулятора сливается электролит, остатки нейтрализуются промыванием каким-либо безвредным основанием (например, гидрокарбонатом натрия), после чего корпус батареи разбивается и извлекается металлический свинец.
См. также
- Автомобильный аккумулятор
- AGM
Примечания
- ↑ 1 2 3 4 5 6 7 8 Свинцовые аккумуляторы. Эксплуатация: Правда и вымыслы.
- ↑ Н. Ламтев. Самодельные аккумуляторы. Москва: Государственное издательство по вопросам радио, 1936 год.
- ↑ http://auto.lenta.ru/news/2006/12/19/battery/ Американцы облегчили и уменьшили аккумуляторы
- ↑ Расчет идеального свинцового аккумулятора.
- ↑ ГОСТ 26881-86 Методика проверки свинцовых АКБ
- ↑ Краткий аналитический обзор существующих способов оценки емкости ХИТ и приборов, реализующих эти способы
- ↑ ГОСТ Р 53165-2008: Батареи аккумуляторные свинцовые стартерные для автотракторной техники. Общие технические условия
- ↑ Вредные добавки к электролиту свинцовых аккумуляторов
- ↑ О противоречиях в теории работы свинцового кислотного аккумулятора к.
 т. н., проф. Кочуров А. А. Рязанский военный автомобильный институт
т. н., проф. Кочуров А. А. Рязанский военный автомобильный институт
Ссылки
- ГОСТ 15596-82 Источники тока химические. Термины и определения
- ГОСТ Р 53165-2008 Батареи аккумуляторные свинцовые стартерные для автотракторной техники. Общие технические условия. Взамен ГОСТ 959—2002 и ГОСТ 29111-91
- О противоречиях в теории работы свинцового кислотного аккумулятора к. т. н., проф. Кочуров А. А. Рязанский военный автомобильный институт
- Видео, демонстрирующее принцип работы аккумулятора на YouTube
- Форум «Электротранспорт.ру»
- Обслуживание и Восстановление свинцовых АКБ системы AGM»
Герметизированные свинцово-кислотные аккумуляторы. Принцип работы, характеристики, особенности использования
- 1 Ключевые электрохимические процессы в свинцово-кислотном аккумуляторе
- 2 Особенности герметизированного свинцово-кислотного аккумулятора
- 3 Конструкция герметизированных свинцово-кислотных аккумуляторов
- 4 Электрические и эксплуатационные характеристики герметизированных свинцово-кислотных аккумуляторов
- 5 Изменения характеристик свинцово-кислотных аккумуляторов при эксплуатации
- 6 Факторы, влияющие на срок службы свинцово-кислотных аккумуляторов
Первый работоспособный свинцово-кислотный аккумулятор был изобретен в 1859 г. французским ученым Гастоном Планте. Конструкция аккумулятора представляла собой электроды из листового свинца, разделенные сепараторами из полотна, которые были свернуты в спираль и помещены в сосуд с 10 % раствором серной кислоты. Недостатком первых свинцово-кислотных аккумуляторов была их невысокая емкость. Поначалу для ее увеличения проводили большое число циклов заряда-разряда. Для достижения существенных результатов требовалось до двух лет таких тренировок. Причина недостатка была явной — конструкция пластин. Поэтому дальнейшее совершенствование конструкции свинцово-кислотных аккумуляторов было сосредоточено на совершенствование конструкции используемых в них пластин и сепараторов.
французским ученым Гастоном Планте. Конструкция аккумулятора представляла собой электроды из листового свинца, разделенные сепараторами из полотна, которые были свернуты в спираль и помещены в сосуд с 10 % раствором серной кислоты. Недостатком первых свинцово-кислотных аккумуляторов была их невысокая емкость. Поначалу для ее увеличения проводили большое число циклов заряда-разряда. Для достижения существенных результатов требовалось до двух лет таких тренировок. Причина недостатка была явной — конструкция пластин. Поэтому дальнейшее совершенствование конструкции свинцово-кислотных аккумуляторов было сосредоточено на совершенствование конструкции используемых в них пластин и сепараторов.
В 1880 г. К. Фор предложил методику изготовления намазных электродов путем нанесения на пластины окислов свинца. Такая конструкция электродов позволила значительно повысить емкость аккумуляторов. А в 1881 г. Э. Фолькмар предложил применять в качестве электродов намазную решетку. В том же году ученому Селлону был выдан патент на технологию изготовления решеток из сплава свинца и сурьмы.
Первоначально практическое использование свинцово-кислотных аккумуляторов было затруднено из-за отсутствия зарядных устройств — для заряда применяли первичные элементы конструкции Бунзена. То есть химический источник тока заряжался от другого химического источника — батареи гальванических элементов. Положение кардинально поменялось с появлением недорогих генераторов постоянного тока.
Именно свинцово-кислотные батареи первыми в мире из аккумуляторных батарей нашли коммерческое применение. К 1890 году во многих промышленно развитых странах был освоен их серийный выпуск. В 1900 году немецкая фирма Varta произвела первые стартерные аккумуляторы для автомобилей.
В 70-х годах XX века были созданы необслуживаемые свинцово-кислотные аккумуляторные батареи, способные работать в любом положении. Жидкий электролит в них сменили гелиевым или адсорбированным (впитанным) сепараторами электролитом, батареи герметизировали, а для отвода газов, выделяющихся при заряде или разряде, установили клапаны. Строго говоря, абсолютная герметизация свинцово-кислотных аккумуляторов не может быть достигнута, так как нельзя обеспечить полную рекомбинацию кислорода и водорода, которые выделяются в них при заряде и хранении. Но специальными мерами выделение газов и потери воды в процессе эксплуатации удается свести к минимуму.
Строго говоря, абсолютная герметизация свинцово-кислотных аккумуляторов не может быть достигнута, так как нельзя обеспечить полную рекомбинацию кислорода и водорода, которые выделяются в них при заряде и хранении. Но специальными мерами выделение газов и потери воды в процессе эксплуатации удается свести к минимуму.
Были разработаны новые конструкции пластин на базе медно-кальциевых сплавов, покрытых оксидом свинца, а также на основе титановых, алюминиевых и медных решеток.
Свинцовые аккумуляторы являются наиболее распространенными среди всех существующих в настоящее время химических источников тока. Их масштабное производство определяется как относительно низкой ценой, обусловленной сравнительной не дефицитностью исходных материалов, так и разработкой разных вариантов этих аккумуляторов, отвечающих требованиям широкого круга потребителей.
Ключевые электрохимические процессы в свинцово-кислотном аккумуляторе
Активные вещества аккумулятора сосредоточены в электролите и положительных и отрицательных электродах, а совокупность этих веществ называется электрохимической системой. В свинцово-кислотных аккумуляторных батареях электролитом является раствор серной кислоты (H2SO4), активным веществом положительных пластин — двуокись свинца (PbO2), отрицательных пластин — свинец (Pb).
В свинцово-кислотных аккумуляторных батареях электролитом является раствор серной кислоты (H2SO4), активным веществом положительных пластин — двуокись свинца (PbO2), отрицательных пластин — свинец (Pb).
Основные процессы, проходящие на электродах, описывают реакции:
На отрицательном электроде:
Pb + HSO4— → PbSO4 + H+ + 2e— (разряд)
PbSO4 + H+ + 2e— → Pb + HSO4— (заряд)
На положительном электроде:
PbO2 + HSO4— + 3H+ + 2e— → PbSO4 + 2H2O (разряд)
PbSO4 + 2H2O → PbO2 + HSO4— + 3H+ + 2e— (заряд)
Суммарная реакция в свинцовом аккумуляторе имеет вид:
PbO2 + Pb + 2H2SO4 → 2PbSO4 + 2H2O (разряд)
2PbSO4 + 2H2O → PbO2 + Pb + 2H2SO4 (заряд)
Таким образом, при разряде свинцового аккумулятора на обоих электродах формируется малорастворимый сульфат свинца (двойная сульфатация) и происходит сильное разбавление серной кислоты.
Напряжение разомкнутой цепи заряженного аккумулятора равно 2,05-2,15 В, в зависимости от концентрации серной кислоты. При разряде по мере разбавления электролита напряжение разомкнутой цепи аккумулятора понижается и после полного разряда становится равным 1,95-2,03 В.
При заряде свинцово-кислотного аккумулятора, как и в других аккумуляторах с водным электролитом, имеют место побочные реакции выделения газов. Выделение водорода начинается при полном заряжении отрицательного электрода. Кислород начинает выделяться гораздо раньше: в обычных условиях заряда при 50-80% заряженности (в зависимости от тока заряда), а при температуре 0 °С уже после заряда на 30-40 %. Вследствие этого отдача положительного электрода по емкости составляет 85-90 %. Для получения полной разрядной емкости при заряде аккумулятору должен быть обеспечен перезаряд на 10-20 %. Этот перезаряд сопровождается существенным выделением водорода на отрицательном электроде и кислорода — на положительном.
Выделение водорода имеет место и при хранении заряженного свинцово-кислотного аккумулятора. Саморазряд его определяется преимущественно скоростью растворения свинца согласно реакции:
Саморазряд его определяется преимущественно скоростью растворения свинца согласно реакции:
Pb + H2SO4 → PbSO4 + H2
Скорость этого процесса зависит от температуры, объема электролита и его концентрации, но более всего от чистоты компонентов. В отсутствие примесей реакция протекает медленно из-за большого перенапряжения выделения водорода на свинце. Но на практике, на поверхности свинцового электрода всегда много примесей, среди которых наибольшее влияние оказывает сурьма, количество которой в сплаве для решеток и токоведущих деталей доходит до 6 %.
На положительном электроде может также самопроизвольно проходить реакция восстановления диоксида свинца:
PbO2 + H2SO4 → PbSO4 + 1/2O2 + H2O
в результате которой выделяется кислород, но скорость ее незначительна.
В процессе эксплуатации саморазряд аккумулятора может увеличиваться из-за образования дендритных мостиков из металлического свинца. Потери емкости свежеизготовленного аккумулятора за счет саморазряда как правило не превышают 2-3 % в месяц. Но при эксплуатации они быстро увеличиваются.
Потери емкости свежеизготовленного аккумулятора за счет саморазряда как правило не превышают 2-3 % в месяц. Но при эксплуатации они быстро увеличиваются.
Особенности герметизированного свинцово-кислотного аккумулятора
Главные проблемы при создании герметичного варианта свинцово-кислотного аккумулятора связаны с необходимостью обеспечения условий для уменьшения газовыделения и содействия рекомбинации выделяющегося газа. При создании герметизированного аккумулятора, который в обычных условиях эксплуатации не требовал бы доливки воды в электролит в течение всего срока службы и не выделял бы газов, был предпринят ряд мер:
1. В аккумуляторе применяется иммобилизированный (обездвиженный) электролит, который сохраняет высокую электропроводность серной кислоты. Небольшое его количество позволяет обеспечить лучший транспорт кислорода от положительного электрода к отрицательному и высокий уровень его рекомбинации.
При одном методе иммобилизации электролита для его загущивания применяется силикагель (SiO2), который обладает высокой пластичностью и заполняет и электроды, и сепаратор. Благодаря своей вязкости он хорошо удерживается в порах и способствует эффективному использованию активных веществ электродов. Транспортировка кислорода обеспечивается по трещинам, которые появляются при усадке твердеющего электролита.
Благодаря своей вязкости он хорошо удерживается в порах и способствует эффективному использованию активных веществ электродов. Транспортировка кислорода обеспечивается по трещинам, которые появляются при усадке твердеющего электролита.
При другом методе иммобилизации применяется сепаратор из стекловолокна с высокой объемной пористостью и хорошей смачиваемостью в растворе серной кислоты. Такой сепаратор не только осуществляет функцию разделения электродов, но и благодаря тонкой структуре волокон обеспечивает удержание электролита в порах и высокую скорость переноса кислорода. Применение стекловолокнистого сепаратора и плотная сборка блока электродов способствуют также уменьшению оплывания активной массы положительного электрода и разбухания губчатого свинца на отрицательном.
2. Для снижения вероятности выделения водорода свинцово-сурьмяные сплавы токоведущих решеток заменяются другими, обеспечивающими более высокое перенапряжение выделения водорода. Применяются сплавы свинца с кальцием (до 0,1 % Ca), иногда легированного алюминием, сплавы свинца с оловом (0,5-2,5 % Sn), которые имеют неплохие литейные характеристики, и другие.
3. В отрицательный электрод закладывается ёмкость больше, чем в положительный. В данном случае при полном заряде положительного электрода оставшаяся недозаряженной часть активной массы отрицательного электрода практически исключает вероятность разряда ионов водорода. Кислород, выделяющийся на диоксиде свинца, достигает отрицательного электрода и окисляет губчатый свинец до оксида свинца, который в кислотном электролите переходит в сульфат свинца PbSO4 и воду. Следовательно, условия для герметизации аккумулятора улучшаются: газы не выделяются и вода не испаряется.
Снижению газовыделения способствуют и рекомендуемые для герметизированных аккумуляторов режимы заряда, при которых ток понижается по мере их заряжения.
И все-таки все реализованные варианты безуходного свинцово-кислотного аккумулятора оснащены клапаном, который время от времени открывается для сброса излишнего количества газа, главным образом водорода. Именно поэтому аккумулятор называется не герметичным, а герметизированным.
Успехи исследователей и технологов, достигнутые за прошедшие два десятилетия, тщательный контроль процесса изготовления и сотрудничество с потребителями, которые научились понимать, что безуходность этих батарей не означает полной свободы от контроля за их работой, позволяют в настоящее время выпускать на рынок продукцию, которая в ряде случаев может конкурировать с более дорогими герметичными щелочными аккумуляторами.
Герметизированные свинцово-кислотные аккумуляторные батареи ёмкостью до 10-20 А*ч применяются как источники питания для разнообразной портативной аппаратуры и инструментов в тех случаях, когда масса не является определяющим критерием для выбора источника тока, а также в системах бесперебойного питания, телекоммуникаций, информационных системах, для аварийного оборудования и т.д., где они работают в буферном режиме.
Конструкция герметизированных свинцово-кислотных аккумуляторов
Портативные герметизированные свинцово-кислотные аккумуляторы выпускаются в виде батарей, которые собраны в едином призматическом контейнере из пластмассы или резины (моноблочная конструкция). Положительные и отрицательные электроды аккумуляторов делаются обычно намазкой на решетку сотовой структуры. Контейнер и крышка загерметизированы. Межэлементные соединения утапливаются в углублениях крышки и залиты мастикой. Выводы аккумуляторной батареи (в виде ушка или борна) также загерметизированы. Клапанное приспособление для сброса газа при излишнем давлении состоит из резинового клапана и отражателя, служащего для улавливания капель электролита. Воздух в аккумулятор через него не поступает.
Положительные и отрицательные электроды аккумуляторов делаются обычно намазкой на решетку сотовой структуры. Контейнер и крышка загерметизированы. Межэлементные соединения утапливаются в углублениях крышки и залиты мастикой. Выводы аккумуляторной батареи (в виде ушка или борна) также загерметизированы. Клапанное приспособление для сброса газа при излишнем давлении состоит из резинового клапана и отражателя, служащего для улавливания капель электролита. Воздух в аккумулятор через него не поступает.
На электрических и эксплуатационных характеристиках герметизированных свинцовых аккумуляторных батарей большой емкости значительно сказываются различия в конструкции электродов (поверхностного типа, панцирные или стержневые), а также различия в сплавах, используемых для изготовления токоведущих основ.
При выборе герметизированной свинцовой аккумуляторной батареи большой емкости следует внимательно отнестись к использованному в ней способу иммобилизации электролита, поскольку известно, что в высоких аккумуляторах со стекловолокнистым сепаратором (технология AGM) со временем отмечается расслоение электролита. Такие аккумуляторы стараются проектировать высотой не более 35 см.
Такие аккумуляторы стараются проектировать высотой не более 35 см.
Электрические и эксплуатационные характеристики герметизированных свинцово-кислотных аккумуляторов
Напряжение разомкнутой цепи свинцово-кислотных аккумуляторов линейно возрастает с ростом степени заряженности аккумулятора (рисунок 1). По значению напряжения разомкнутой цепи можно судить о степени разряда свинцового аккумулятора.
Рис.1. Зависимость напряжения разомкнутой цепи свинцово-кислотного аккумулятора от уровня заряженностиНоминальной ёмкостью свинцово-кислотного аккумулятора считается ёмкость, полученная при разряде в течение 20 ч, т.е. током 0,05С. Отдаваемая аккумулятором ёмкость значительно зависит от тока разряда, который может достигать нескольких С. Типичные разрядные характеристики при различных токах нагрузки показаны на рисунке 2. Из рисунка видно, что от тока разряда зависит также и конечное разрядное напряжение свинцового аккумулятора.
Рис.2. Разрядные характеристики герметизированной свинцово-кислотной аккумуляторной батареиГерметизированные свинцовые аккумуляторные батареи работоспособны в интервале температур от -30 до +50 °С, чаще гарантируется работоспособность при температуре не ниже -15 °С.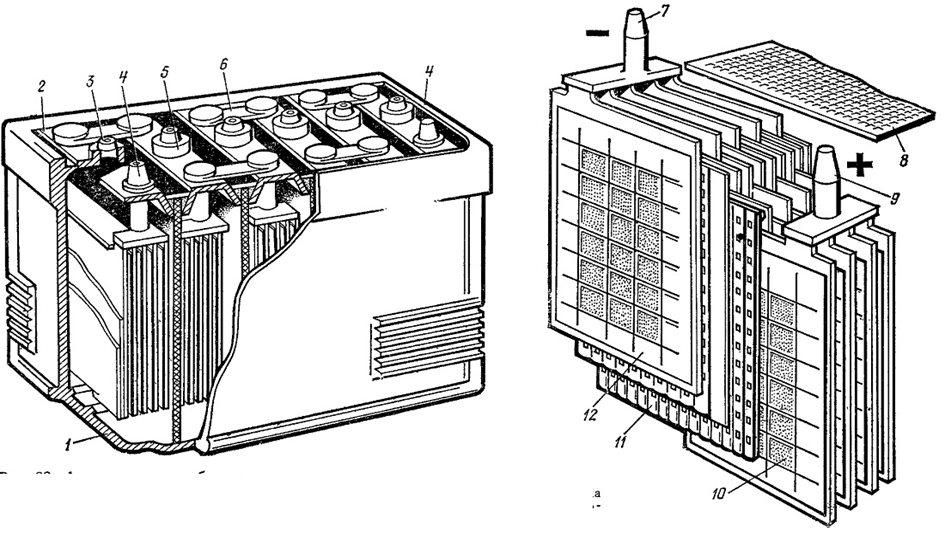 При более низких температурах возможности разряда мешает замерзание электролита. Работоспособность аккумуляторов при низких температурах может быть обеспечена увеличением концентрации электролита, как это и делается в специальных аккумуляторах.
При более низких температурах возможности разряда мешает замерзание электролита. Работоспособность аккумуляторов при низких температурах может быть обеспечена увеличением концентрации электролита, как это и делается в специальных аккумуляторах.
Заряд свинцово-кислотного аккумулятора.
Заряд батарей, как было сказано ранее, должен осуществляться в режиме, при котором ток должен сильно понижаться к концу заряда. Используется несколько стратегий заряда, которые требуют оборудования различной сложности и стоимости. Наиболее простое и дешёвое оборудование осуществляет заряд при постоянном напряжении 2,4-2,45В/ак (потенциостатический режим). Заряд считается законченным если ток заряда остается неизменным в течении 3-х часов.
Но чаще применяют комбинированный режим, при котором начальный ток ограничивают, а по достижении заданного напряжения, заряд проводится при стабилизации напряжения (рисунок 3). Заряд проводится при постоянном токе 0,1С на первом этапе и при постоянном напряжении источника тока на втором. Большинство производителей советуют проводить заряд циклируемых батарей при постоянном напряжении 2,4В на аккумулятор.
Заряд проводится при постоянном токе 0,1С на первом этапе и при постоянном напряжении источника тока на втором. Большинство производителей советуют проводить заряд циклируемых батарей при постоянном напряжении 2,4В на аккумулятор.
Ускорение процесса заряда достигается при повышении тока на первой стадии заряда, но в соответствии с советами производителей не более чем до 0,3С. В конце заряда для большей безопасности может быть применена еще одна ступень заряда: при снижении напряжения источника питания до напряжения подзаряда аккумулятора 2,30-2,35 В.
Заряд аккумуляторных батарей, используемых, для работы в буферном режиме, проводится как правило при более низком напряжении (2,23-2,275 В).
Указанные напряжения заряда не требуют изменения при заряде в некотором интервале температуры (обычно от 5 до 35 °С). За пределами указанного температурного интервала, требуется компенсация влияния температуры: повышение напряжения при пониженных температурах и снижение при более высоких.
Саморазряд свинцово-кислотной аккумуляторной батареи.
Саморазряд в герметизированных свинцово-кислотных аккумуляторах значительно уменьшен по сравнению с вентилируемыми аккумуляторами и составляет 40% в год при 20 °С и 15% при 5 °С. При более высоких температурах хранения саморазряд увеличивается: при 40 °С батареи лишаются 40 % ёмкости за 4-5 месяцев.
При продолжительном хранении в заряженном состоянии батареи рекомендуют периодически подзаряжать. Если они хранились при температуре ниже -20 °С, то подзаряд должен проводиться 1 раз в год в течение 48 ч при постоянном напряжении 2,275 В/ак. При хранении при комнатной температуре — 1 раз в 8 месяцев в течение 6-12 ч при постоянном напряжении 2,4 В/ак. Хранение при температуре выше 30 °С не желателен.
Продолжительное хранение батареи в разряженном состоянии приводит к быстрой потере ее работоспособности.
Изменения характеристик свинцово-кислотных аккумуляторов при эксплуатации
Рис.5. Действие температуры на остаточную емкость герметизированного свинцово-кислотного аккумулятора: 1-40°С, 2-20°С, 3-10°С, 4-0°ССрок службы герметизированных свинцово-кислотных аккумуляторных батарей, как и вентилируемых, в большинстве случаев определяется деградацией положительного электрода, которая определяется коррозией его решетки и изменениями в активной массе.
Скорость коррозии решеток зависит как от состава сплава, конструкции и условий отливки, так и от температуры, при которой работают батареи. Коррозия решетки из сплава без сурьмы или с низким ее содержанием существенно медленнее по сравнению с коррозией традиционных решеток вентилируемых аккумуляторов. В качественно отлитых решетках из сплавов Pb-Ca-Sn скорость коррозии маленькая, но в плохо отлитых — отдельные участки подвергаются глубокой коррозии, что вызывает локальный ее рост и деформацию. Деформация решеток может привести к короткому замыканию разнополярных пластин. Коррозия решеток положительных пластин — самый частый дефект батарей, эксплуатируемых в буферном режиме.
Коррозия решеток положительных пластин — самый частый дефект батарей, эксплуатируемых в буферном режиме.
При эксплуатации в режиме циклирования происходит также разрыхление активных масс положительного электрода, которое приводит к потере контакта между частицами PbO2. Емкость источника тока при этом уменьшается. Процесс разрыхления ускоряется при разряде большими импульсами тока.
В герметизированных аккумуляторах могут протекать и специфические коррозионные процессы на токоведущих деталях отрицательных пластин, которые находятся выше уровня электролита, и на борне. Так как продукты коррозии имеют больший объем, чем свинец, в результате может иметь место выдавливание компаунда, герметизирующего вывод, и повреждение борна, крышки и даже бака. Дефекты такого рода часто отмечались в аккумуляторах разных производителей на ранних этапах разработок и производства. Сейчас большая часть производителей решила эту проблему подбором сплавов для всех компонентов аккумулятора и контролем за металлургическим процессом их изготовления.
В течении эксплуатации герметизированных аккумуляторов из-за неизбежных потерь воды при открывании клапана для сброса излишнего давления газа происходит некоторое осушение сепаратора и повышение внутреннего сопротивления аккумулятора. При эксплуатации в буферном режиме количество отказов, спровоцированных высыханием аккумулятора, становится соизмеримым с отказами из-за коррозии решеток положительных электродов. В аккумуляторах с гелиевым электролитом снижение количества электролита менее критично, чем в аккумуляторах с сепаратором из стекловолокна.
Факторы, влияющие на срок службы свинцово-кислотных аккумуляторов
Рис.6. Зависимость срока службы герметизированной свинцово-кислотной батареи от глубины разрядаСамое большое влияние на срок службы герметизированного свинцово-кислотного аккумулятора оказывают: рабочая температура, глубина разряда и величина перезаряда, а также периодичность срабатывания клапана для сброса газа.
На рисунках 6 и 7 изображено изменение срока службы в зависимости от глубины разряда и температуры окружающей среды.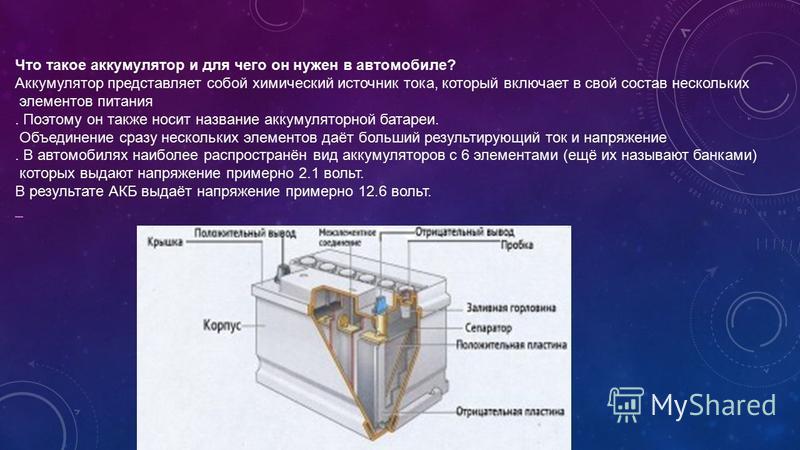 .
.
Герметизированные свинцово-кислотные аккумуляторы очень чувствительны к перезаряду. На рисунке 8 изображено, как быстро уменьшается срок их службы при работе в режиме постоянного подзаряда при повышении напряжения (и тем самым — тока подзаряда) источника питания подключенного к аккумулятору.
Следует помнить, что при заряде герметизированных аккумуляторов их температура может быть значительно выше температуры окружающей среды. Это связано как с разогревом аккумуляторов из-за реакции рекомбинации кислорода, так и с неудовлетворительным отводом тепла от плотноупакованной батареи. Разница температур особенно ощутима при ускоренном режиме заряда. Если нельзя избежать существенного увеличения температуры, то при заряде следует вводить корректировку напряжения источника питания.
Рис.8. Воздействие режима заряда на срок службы герметизированной свинцово-кислотной аккумуляторной батареи при работе в буферном режимеПереразряд также вреден для свинцово-кислотных батарей, как и перезаряд. При многократных переразрядах уменьшается разрядная емкость и понижается срок службы аккумулятора. Такие же изменения могут происходить и при продолжительном хранении батарей в разряженном состоянии.
При многократных переразрядах уменьшается разрядная емкость и понижается срок службы аккумулятора. Такие же изменения могут происходить и при продолжительном хранении батарей в разряженном состоянии.
В связи с расширением сферы применения герметизированных свинцовых аккумуляторов до обитаемых комплексов специального назначения, где должны применяться мощные источники тока с большим напряжением, стало необходимым исследование последствий возникновения аварийных ситуаций в эксплуатации. Такие ситуации могут происходить как при разбалансировании характеристик аккумуляторов, составляющих батарею, так и в результате ошибочного обслуживания батарей или отказе управляющего оборудования. В этом случае при перезаряде или переразряде батарей, приводящем к переполюсованию наиболее слабых аккумуляторов, может произойти разгерметизация аккумуляторов или даже разрушение их баков.
Было показано, что повреждение корпуса приводит к снижению отдаваемой ёмкости, но более серьезных проблем не возникает. Даже при полном разрушении контейнера аккумулятора емкость его стала меньше только на 14 %, так как электролит не вытекает, а задерживается в порах электродов и сепаратора. При вскрытии 5 % площади контейнера, аккумуляторы оставались годными для циклирования при снижении разрядной емкости на 15-20 %.
Даже при полном разрушении контейнера аккумулятора емкость его стала меньше только на 14 %, так как электролит не вытекает, а задерживается в порах электродов и сепаратора. При вскрытии 5 % площади контейнера, аккумуляторы оставались годными для циклирования при снижении разрядной емкости на 15-20 %.
При продолжительном перезаряде (током 0,25 Сн) как свежих аккумуляторов, так и после полтора года эксплуатации в режиме постоянного подзаряда, а также при заряде аккумуляторов при завышенном напряжении (2,6В), чрезвычайного разогрева аккумуляторов не происходило. Температура стабилизируется спустя 4-6 ч на уровне 50-70 °С или затем медленно понижается. Но из-за выброса газов через аварийный клапан происходит осушение аккумуляторов и быстрая их деградация.
Современные герметизированные свинцово-кислотные аккумуляторные батареи обладают достаточно высокими удельными энергетическими характеристиками (до 40 Втч/кг и 100 Втч/л). Они работоспособны в буферном режиме при нормальной температуре в течение продолжительного периода (более 10 лет), а при циклировании обеспечивают несколько сотен циклов до потери 20 % ёмкости.
Источник
Эта статья прочитана 9435 раз(а)!
Эксплуатационный ресурс герметичных АБ
57
Эксплуатационный ресурс герметичных свинцовых аккумуляторных батарей в составе электронного оборудования Мерунко Александр Анатольевич Технический директор ООО «Диск», г.Томск В настоящее время на потребительском рынке вторичных источников тока лидирующее положения (вследствие относительно низкой стоимости) занимают герметичные свинцовые аккумуляторные батареи. Их применяют…
Эксплуатация герметичных аккумуляторов
53
Применение и эксплуатация кислотно-свинцовых герметичных аккумуляторов Автор: Журавлев О. В. В статье рассмотрены вопросы применения и эксплуатации кислотно-свинцовых герметичных аккумуляторных батарей, наиболее широко используемых для резервирования аппаратуры охранно-пожарной сигнализации (ОПС) Появившиеся на российском рынке в начале 90-х годов кислотно-свинцовые герметичные…
Сульфатация аккумуляторов
52
Что такое сульфатация свицово-кислотных аккумуляторов и как с ней бороться? Сульфатация происходит, когда свинцово-кислотный аккумулятор регулярно не заряжается полностью.
 Такой режим типичен как для стартерных батарей в автомобилях, так и в автономных системах электроснабжения, где полный заряд аккумуляторов может отсутствовать…
Такой режим типичен как для стартерных батарей в автомобилях, так и в автономных системах электроснабжения, где полный заряд аккумуляторов может отсутствовать…Аккумуляторы глубокого разряда
50
Аккумуляторы глубокого циклирования Аккумуляторные батареи общего назначения не рассчитаны на тяжелые циклические режимы работы, которые имеют место в автономных системах электроснабжения. При глубине разряда более 15-20% срок их службы существенно сокращается. Поэтому мы рекомендуем в автономных системах электроснабжения использовать специальные…
Замена щелочных АБ на свинцово-кислотные
50
Замена щелочных АБ на свинцово-кислотные Источник: Химические источники тока АККУМУЛЯТОР — химический источник тока, который после разряда обладает возможностью заряда (преобразования электрической энергии в химическую) путем пропускания через него электрического тока обратного направления. Мы рассматриваем две электрохимические системы аккумуляторов, свинцовую…
Новый аккумулятор нужно заряжать ⚡
50
В каких случаях необходимо заряжать новый аккумулятор? Любому автолюбителю известно, что необходимо время от времени обслуживать аккумуляторную батарею, установленную в транспортном средстве, но далеко не всем известно, что необходимо так же обслужить новый аккумулятор перед началом использования.
 Нужно ли заряжать…
Нужно ли заряжать…
Статьи о батареях | Объяснение свинцово-кислотного аккумулятора
База знаний : Учебные пособия : Статьи о аккумуляторах : Объяснение сверхсекретных принципов работы свинцово-кислотного аккумулятора
12-вольтовая аккумуляторная батарея мотоцикла состоит из пластикового корпуса, содержащего шесть элементов. Каждая ячейка состоит из набора положительных и отрицательных пластин, погруженных в разбавленный раствор серной кислоты, известный как электролит, и каждая ячейка имеет напряжение около 2,1 вольта при полной зарядке. Шесть элементов соединены вместе, чтобы получить полностью заряженную батарею с напряжением около 12,6 вольт.
Замечательно, но как при погружении свинцовых пластин в серную кислоту вырабатывается электричество? Батарея использует электрохимическую реакцию для преобразования химической энергии в электрическую. Давайте посмотрим. Каждая ячейка содержит пластины, напоминающие крошечные квадратные теннисные ракетки, сделанные либо из свинцово-сурьмяного, либо из свинцово-кальциевого сплава. Затем к пластинам приклеивается паста из так называемого «активного материала»; губчатый свинец для отрицательных пластин и диоксид свинца для положительных. В этом активном материале происходит химическая реакция с серной кислотой, когда на клеммы аккумулятора подается электрическая нагрузка.
Затем к пластинам приклеивается паста из так называемого «активного материала»; губчатый свинец для отрицательных пластин и диоксид свинца для положительных. В этом активном материале происходит химическая реакция с серной кислотой, когда на клеммы аккумулятора подается электрическая нагрузка.
Как это работает
Позвольте мне сначала представить вам общую картину для тех, кто не очень внимателен к деталям. В основном, когда батарея разряжается, серная кислота в электролите истощается, так что электролит больше напоминает воду. В то же время сульфат из кислоты покрывает пластины и уменьшает площадь поверхности, на которой может происходить химическая реакция. Зарядка обращает процесс вспять, превращая сульфат обратно в кислоту. Это в двух словах, но читайте дальше для лучшего понимания. Если вы уже выбежали из комнаты, крича и дергая себя за волосы, не волнуйтесь.
Электролит (серная кислота и вода) содержит заряженные ионы сульфата и водорода. Ионы сульфата заряжены отрицательно, а ионы водорода — положительно. Вот что происходит, когда вы включаете нагрузку (фары, стартер и т.д.). Ионы сульфата перемещаются к отрицательным пластинам и теряют свой отрицательный заряд. Оставшийся сульфат соединяется с активным материалом на пластинах, образуя сульфат свинца. Это снижает прочность электролита, а сульфат на пластинах действует как электрический изолятор. Избыточные электроны вытекают из отрицательной стороны батареи, проходят через электрическое устройство и возвращаются к положительной стороне батареи. На положительной клемме батареи электроны устремляются обратно и принимаются положительными пластинами. Кислород в активном материале (диоксид свинца) реагирует с ионами водорода с образованием воды, а свинец реагирует с серной кислотой с образованием сульфата свинца.
Вот что происходит, когда вы включаете нагрузку (фары, стартер и т.д.). Ионы сульфата перемещаются к отрицательным пластинам и теряют свой отрицательный заряд. Оставшийся сульфат соединяется с активным материалом на пластинах, образуя сульфат свинца. Это снижает прочность электролита, а сульфат на пластинах действует как электрический изолятор. Избыточные электроны вытекают из отрицательной стороны батареи, проходят через электрическое устройство и возвращаются к положительной стороне батареи. На положительной клемме батареи электроны устремляются обратно и принимаются положительными пластинами. Кислород в активном материале (диоксид свинца) реагирует с ионами водорода с образованием воды, а свинец реагирует с серной кислотой с образованием сульфата свинца.
Ионы, движущиеся в электролите, создают ток, но по мере того, как ячейка разряжается, количество ионов в электролите уменьшается, и площадь активного материала, доступного для их приема, также уменьшается, потому что он покрывается сульфатом. Помните, что химическая реакция происходит в порах активного материала, прикрепленного к пластинам.
Помните, что химическая реакция происходит в порах активного материала, прикрепленного к пластинам.
Многие из вас, возможно, замечали, что батарея, используемая для запуска велосипеда, который просто не заводится, быстро доходит до того, что двигатель даже не заводится. Однако, если эту батарею оставить на некоторое время в покое, она, похоже, вернется к жизни. С другой стороны, если вы оставите переключатель в положении «парк» на ночь (горит только пара маленьких лампочек), то утром аккумулятор будет совершенно бесполезен, и никакой отдых не заставит его восстановиться. Почему это? Поскольку ток возникает в результате химической реакции на поверхности пластин, сильный ток быстро превращает электролит на поверхности пластин в воду. Напряжение и ток будут снижены до уровня, недостаточного для работы стартера. Требуется время, чтобы большее количество кислоты диффундировало через электролит и добралось до поверхности пластин. Этому способствует короткий период отдыха. Кислота не истощается так быстро, когда ток мал (например, для питания лампы заднего фонаря), а скорость диффузии достаточна для поддержания напряжения и тока. Это хорошо, но когда напряжение, в конце концов, падает, больше не остается кислоты, скрывающейся во внешних пределах ячейки, чтобы мигрировать на пластины. Электролит в основном состоит из воды, а пластины покрыты изолирующим слоем сульфата свинца. Теперь требуется зарядка.
Это хорошо, но когда напряжение, в конце концов, падает, больше не остается кислоты, скрывающейся во внешних пределах ячейки, чтобы мигрировать на пластины. Электролит в основном состоит из воды, а пластины покрыты изолирующим слоем сульфата свинца. Теперь требуется зарядка.
Саморазряд
Одной из неприятных особенностей свинцово-кислотных аккумуляторов является то, что они разряжаются сами по себе, даже если не используются. Общее эмпирическое правило – скорость саморазряда составляет один процент в день. Эта скорость увеличивается при высоких температурах и уменьшается при низких температурах. Не забывайте, что ваш Gold Wing с часами, стереосистемой и CB-радио никогда не выключается полностью. Каждое из этих устройств имеет «поддерживающую память» для сохранения ваших предварительных настроек радио и времени, и эти воспоминания потребляют около 20 миллиампер или 0,020 ампер. Это высасывает из вашей батареи около получаса ампер-часа в день при температуре 80 градусов по Фаренгейту. Это потребление в сочетании со скоростью саморазряда приведет к тому, что ваша батарея будет разряжена на 50 процентов за две недели, если велосипед оставить без присмотра и без движения.
Это потребление в сочетании со скоростью саморазряда приведет к тому, что ваша батарея будет разряжена на 50 процентов за две недели, если велосипед оставить без присмотра и без движения.
Когда батарея заряжается
Зарядка — это процесс, который меняет направление электрохимической реакции. Он преобразует электрическую энергию зарядного устройства в химическую энергию. Помните, батарея не хранит электричество; он хранит химическую энергию, необходимую для производства электричества.
Зарядное устройство меняет направление тока при условии, что зарядное устройство имеет большее напряжение, чем аккумулятор. Зарядное устройство создает избыток электронов на отрицательных пластинах, и положительные ионы водорода притягиваются к ним. Водород реагирует с сульфатом свинца с образованием серной кислоты и свинца, и когда большая часть сульфата уходит, водород поднимается с отрицательных пластин. Кислород в воде вступает в реакцию с сульфатом свинца на положительных пластинах, снова превращая их в двуокись свинца, и когда реакция почти завершена, из положительных пластин поднимаются пузырьки кислорода.
Многие люди думают, что внутреннее сопротивление батареи высокое, когда батарея полностью заряжена, но это не так. Если вы подумаете об этом, вы вспомните, что сульфат свинца действует как изолятор. Чем больше сульфата на пластинах, тем выше внутреннее сопротивление батареи. Более высокое сопротивление разряженной батареи позволяет ей принимать более высокую скорость зарядки без выделения газа или перегрева, чем когда батарея почти полностью заряжена. Почти полностью заряженный, остается не так много сульфата, чтобы поддерживать обратную химическую реакцию. Уровень зарядного тока, который может быть применен без перегрева батареи или разрушения электролита на водород и кислород, известен как «естественная скорость поглощения» батареи. Когда ток заряда превышает эту естественную скорость поглощения, происходит перезарядка. Аккумулятор может перегреться, и электролит начнет пузыриться. На самом деле, часть зарядного тока теряется в виде тепла даже при правильном уровне заряда, и эта неэффективность создает необходимость возвращать в аккумулятор больше ампер-часов, чем было извлечено. Подробнее об этом позже.
Подробнее об этом позже.
Как долго будет работать мой аккумулятор?
Существует множество факторов, которые могут привести к выходу из строя батареи или значительному сокращению срока ее службы. Одна из таких вещей позволяет батарее оставаться в частично разряженном состоянии . Мы говорили о сульфатообразовании на поверхности пластин аккумулятора при разряде, сульфат также образуется в результате саморазряда. Сульфат также быстро образуется, если уровень электролита упадет до такой степени, что пластины будут открыты. Если позволить этому сульфату остаться на пластинах, кристаллы будут увеличиваться в размерах и затвердевать до тех пор, пока их станет невозможно удалить путем зарядки. Следовательно, количество доступной площади поверхности для химической реакции будет постоянно уменьшаться. Это состояние известно как «сульфатация», и оно необратимо снижает емкость аккумулятора. Аккумулятор на 20 ампер-часов может начать работать как аккумулятор на 16 ампер-часов (или меньше), быстро теряя напряжение под нагрузкой и не поддерживая достаточное напряжение во время проворачивания коленчатого вала для работы системы зажигания мотоцикла. Это последнее условие проявляется, когда двигатель отказывается запускаться до тех пор, пока вы не уберете палец с кнопки запуска. Когда вы отпускаете стартер, напряжение аккумуляторной батареи мгновенно подскакивает до достаточного уровня. Поскольку двигатель все еще кратковременно вращается, зажигание, включенное теперь, зажжет свечи зажигания. В следующем выпуске мы увидим, почему увеличение внутреннего сопротивления из-за сульфатации приводит к снижению мощности, подаваемой на стартер.
Это последнее условие проявляется, когда двигатель отказывается запускаться до тех пор, пока вы не уберете палец с кнопки запуска. Когда вы отпускаете стартер, напряжение аккумуляторной батареи мгновенно подскакивает до достаточного уровня. Поскольку двигатель все еще кратковременно вращается, зажигание, включенное теперь, зажжет свечи зажигания. В следующем выпуске мы увидим, почему увеличение внутреннего сопротивления из-за сульфатации приводит к снижению мощности, подаваемой на стартер.
Глубокий разряд — еще один убийца батареи. Каждый раз, когда аккумулятор глубоко разряжается, часть активного материала слетает с пластин и падает на дно корпуса аккумулятора. Естественно, при этом остается меньше материала для проведения химической реакции. Если в нижней части корпуса скапливается достаточное количество этого материала, он закорачивает пластины и убивает батарею.
Перезарядка — коварная убийца; его эффекты часто не очевидны для невиновного покупателя десятидолларового зарядного устройства, который оставляет его подключенным к батарее в течение длительного времени. https://www.batterystuff.com/battery-chargers/#mce_temp_url# заряжается с постоянной скоростью независимо от уровня заряда батареи. Если эта скорость больше, чем естественная скорость поглощения батареи при полной зарядке, электролит начнет разрушаться и выкипать. Многие водители всю зиму хранили велосипед на зарядном устройстве, а весной обнаруживали, что батарея практически разряжена. Кроме того, поскольку при зарядке положительные пластины окисляются, продолжительная перезарядка может вызвать коррозию пластин или разъемов до тех пор, пока они не ослабнут и не сломаются.
https://www.batterystuff.com/battery-chargers/#mce_temp_url# заряжается с постоянной скоростью независимо от уровня заряда батареи. Если эта скорость больше, чем естественная скорость поглощения батареи при полной зарядке, электролит начнет разрушаться и выкипать. Многие водители всю зиму хранили велосипед на зарядном устройстве, а весной обнаруживали, что батарея практически разряжена. Кроме того, поскольку при зарядке положительные пластины окисляются, продолжительная перезарядка может вызвать коррозию пластин или разъемов до тех пор, пока они не ослабнут и не сломаются.
Недостаточный заряд — это состояние, характерное для многих мотоциклов. Ваш регулятор напряжения настроен на поддержание напряжения вашей системы на уровне от 14 до 14,4 вольт. Если вы один из тех людей, которые ездят по межштатным автомагистралям с вольтметром, показывающим всего 13,5 вольт, потому что вы сжигаете больше огней, чем рождественская витрина Macy’s, вы должны знать, что этого напряжения достаточно для поддержания заряженной батареи, но недостаточно для полного заряда. перезарядить разряженный.
перезарядить разряженный.
Помните, мы говорили, что выделение газа происходит, когда весь или большая часть сульфата свинца превращается обратно в свинец и диоксид свинца. Напряжение, при котором это обычно происходит, известное как напряжение газообразования, обычно чуть выше 14 вольт. Если напряжение в вашей системе никогда не станет таким высоким, и если вы никогда не компенсируете это, подключив зарядное устройство дома, сульфат начнет накапливаться и затвердевать, как налет во рту. Считайте, что тщательная периодическая зарядка похожа на чистку зубов зубной нитью и зубной нитью. Если вы плохо соблюдаете гигиену полости рта, вы можете пойти к дантисту и попросить его соскрести всю гадость. Когда ваша батарея достигает этой стадии, это шторы!
Какой тип зарядного устройства и почему
Генератор переменного тока и стандартное автомобильное конусное зарядное устройство имеют много общего; они стремятся поддерживать постоянное напряжение. Вот проблема с попыткой быстро зарядить глубоко разряженный аккумулятор любым из них. Помните, мы обсуждали, как сильное потребление тока может заставить батарею выглядеть разряженной. Затем, по мере того как кислота диффундировала через ячейки, концентрация на поверхности пластин увеличивалась, и батарея возвращалась к жизни.
Помните, мы обсуждали, как сильное потребление тока может заставить батарею выглядеть разряженной. Затем, по мере того как кислота диффундировала через ячейки, концентрация на поверхности пластин увеличивалась, и батарея возвращалась к жизни.
Аналогичным образом, напряжение батареи во время заряда увеличивается из-за концентрации кислоты, которая возникает на поверхности пластин. Если скорость заряда значительна, напряжение будет быстро расти. Коническое зарядное устройство или регулятор напряжения автомобиля будут резко снижать скорость зарядки, когда напряжение поднимается выше 13,5 В, но соответствует ли уровень заряда аккумулятора напряжению? Нет! Опять же, кислоте требуется время, чтобы распространиться по клеткам.
Хотя напряжение может быть высоким, электролит во внешних частях элементов все еще слабый, и уровень заряда батареи может быть намного ниже, чем указывало бы напряжение. Только после продолжительной зарядки уменьшенным током будет достигнута полная емкость. По этой причине вы не должны судить о состоянии заряда батареи, измеряя напряжение во время зарядки. Проверяйте его только после того, как батарея постоит не менее часа. Напряжение будет уменьшаться и стабилизироваться по мере того, как кислота будет распространяться по ячейкам.
По этой причине вы не должны судить о состоянии заряда батареи, измеряя напряжение во время зарядки. Проверяйте его только после того, как батарея постоит не менее часа. Напряжение будет уменьшаться и стабилизироваться по мере того, как кислота будет распространяться по ячейкам.
В течение последних нескольких лет несколько компаний разработали зарядные устройства, которые могут быстро зарядить разряженную батарею, а затем удерживать ее при напряжении, которое не приведет ни к выделению газа, ни к саморазряду. Их иногда называют «умными зарядными устройствами» или многоступенчатыми зарядными устройствами. Вот как они работают.
Мы сказали, что батарея может принимать гораздо более высокую скорость зарядки, когда она частично разряжена, чем когда она почти полностью заряжена. Эти многоступенчатые зарядные устройства используют этот факт, начиная заряд постоянным током или в режиме «объемного заряда». Как правило, они обеспечивают ток заряда от 650 миллиампер до 1,5 ампер, в зависимости от марки и модели. Этот объемный заряд поддерживается постоянным (или должен быть) до тех пор, пока напряжение батареи не достигнет 13,5 вольт, что позволяет батарее поглощать большее количество заряда за короткое время и без повреждений. Затем зарядное устройство переключается на постоянное напряжение или «абсорбционный» заряд.
Этот объемный заряд поддерживается постоянным (или должен быть) до тех пор, пока напряжение батареи не достигнет 13,5 вольт, что позволяет батарее поглощать большее количество заряда за короткое время и без повреждений. Затем зарядное устройство переключается на постоянное напряжение или «абсорбционный» заряд.
Идея состоит в том, чтобы позволить батарее поглотить последние 15 процентов своего заряда с естественной скоростью поглощения, чтобы предотвратить чрезмерное выделение газов или нагрев. Наконец, эти зарядные устройства переключаются в «плавающий» режим, в котором напряжение батареи поддерживается на уровне, достаточном, чтобы предотвратить ее разряд, но недостаточном, чтобы вызвать перезарядку. Различные компании в целом расходятся во мнениях относительно того, каким должно быть это плавающее напряжение, но обычно оно составляет от 13,2 до 13,4 вольт. На самом деле, плавающее напряжение должно иметь температурную компенсацию в пределах 13,1 В при 9°С.0 градусов по Фаренгейту до 13,9 вольт при 50 градусах. Большинство очень дорогих высокомощных многоступенчатых зарядных устройств для использования с большими батареями для жилых автофургонов имеют температурную компенсацию, но, насколько мне известно, ни одно из устройств для мотоциклов не компенсируется; они используют компромиссную настройку с плавающей запятой.
Большинство очень дорогих высокомощных многоступенчатых зарядных устройств для использования с большими батареями для жилых автофургонов имеют температурную компенсацию, но, насколько мне известно, ни одно из устройств для мотоциклов не компенсируется; они используют компромиссную настройку с плавающей запятой.
То есть я могу просто установить и забыть, верно? Ну, не совсем так. Во-первых, вам нужно время от времени контролировать уровень жидкости в аккумуляторе (если только у вас не герметичный аккумулятор). Еще одна проблема заключается в том, что заряд батареи. Даже если держать его на уровне 13 вольт, неизменное напряжение позволит аккумулятору со временем начать сульфатироваться. С большинством этих устройств я рекомендую отключать зарядное устройство не реже одного раза в 60 дней во время сезонного хранения. Дайте аккумулятору отдохнуть пару дней, а затем снова подключите зарядное устройство.
Все еще здесь?
Если ты все еще читаешь это, ты настоящий боец.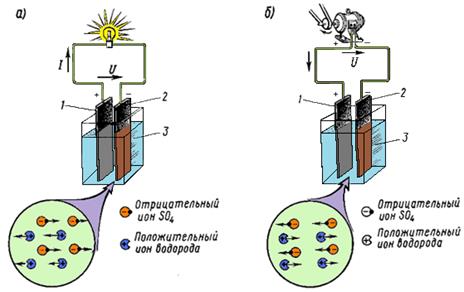 Я понимаю, что эта тема может быть запутанной или даже скучной, но мужайтесь; Я полегчал с тобой. Там гораздо больше осталось невысказанным, чем то, что появляется здесь. Это были «Лучшие хиты Батареи». Я надеюсь, что этого было достаточно, чтобы заинтересовать вас, не отправляя вас в информационную перегрузку, и, может быть, теперь, когда вы знаете, сколько существует способов сократить срок службы батареи, вы понимаете, почему никто не может предсказать, как долго прослужит батарея. Многие гонщики, которые считают, что отлично заботятся о своих батареях, на самом деле убивают их добротой.
Я понимаю, что эта тема может быть запутанной или даже скучной, но мужайтесь; Я полегчал с тобой. Там гораздо больше осталось невысказанным, чем то, что появляется здесь. Это были «Лучшие хиты Батареи». Я надеюсь, что этого было достаточно, чтобы заинтересовать вас, не отправляя вас в информационную перегрузку, и, может быть, теперь, когда вы знаете, сколько существует способов сократить срок службы батареи, вы понимаете, почему никто не может предсказать, как долго прослужит батарея. Многие гонщики, которые считают, что отлично заботятся о своих батареях, на самом деле убивают их добротой.
Выберите зарядное устройство для аккумулятора
Была ли эта информация полезной? Подпишитесь, чтобы получать обновления и предложения.
Адрес электронной почты должен быть в формате [email protected]Мы уважаем ваше право на неприкосновенность частной жизни и никогда никому не передадим информацию о вашей электронной почте.
вы ДОЛЖНЫ включить JavaScript, чтобы иметь возможность комментировать
Свинцово-кислотная технология » Electronics Notes
Что такое свинцово-кислотные аккумуляторы и как работают свинцово-кислотные аккумуляторы — обзор технологии, работы, преимуществ и конструкции свинцово-кислотных аккумуляторов.

Аккумуляторная технология Включает:
Обзор аккумуляторной технологии
Определения и термины батареи
Емкость и срок службы батареи
Батареи / ячейки последовательно и параллельно
Цинк-углерод
Щелочные элементы
Цинковые воздушные ячейки
Литиевая первичная батарея
NiCad
NiMH
литий-ион
Свинцово-кислотный
Свинцово-кислотные аккумуляторы дешевы, удобны и подходят для многих приложений питания от аккумуляторов. Они, вероятно, наиболее известны своим использованием в обычных автомобильных транспортных средствах с двигателем внутреннего сгорания, где они обеспечивают питание для всего, от запуска двигателя до электроники и многого другого.
Свинцово-кислотные аккумуляторы имеют много преимуществ для автомобильного и многих других применений: они имеют большой ток и способность к импульсным перенапряжениям, что идеально подходит для запуска двигателей внутреннего сгорания.
Как технология, свинцово-кислотные аккумуляторы являются хорошо зарекомендовавшей себя технологией, и их можно легко производить с использованием относительно несложного технологического оборудования.
Однако технология свинцово-кислотных аккумуляторов в настоящее время вытесняется технологией ионно-литиевых аккумуляторов. Эти новые ионно-литиевые аккумуляторы для электромобилей способны обеспечить питание автомобиля, а также электронное и электрическое оборудование в автомобиле.
Соответственно, использование технологии свинцово-кислотных аккумуляторов сокращается, поскольку аккумуляторы электромобилей все чаще используются для новых карт и других транспортных средств.
Типичная свинцово-кислотная батарея в автомобилеИстория свинцово-кислотной батареи
Свинцово-кислотная батарея была первой разработанной формой перезаряжаемой батареи. Идея была первоначально предложена французским физиком Гастоном Планте в 1860 году.
Хотя другой французский ученый по имени Готеро обнаружил, что платиновые или серебряные провода, которые использовались для электролиза соленой воды, производили ток в течение короткого промежутка времени, это так и не было превращено в работоспособную батарею.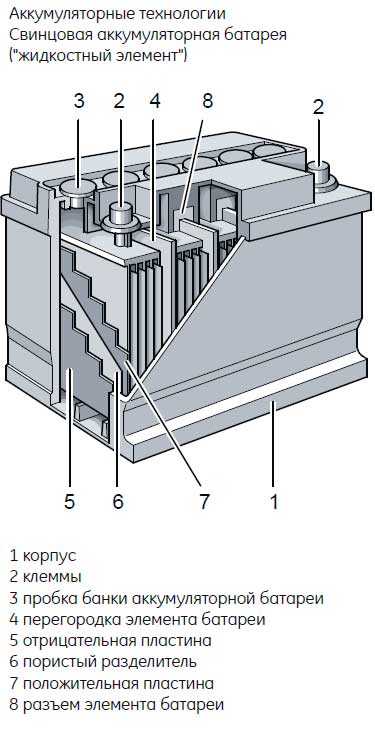
Первые свинцово-кислотные аккумуляторы были изготовлены из свинцовых пластин. Затем батарею нужно было «сформировать», зарядив ее так, чтобы одна из пластин окислилась. Затем батарея увеличивала свою емкость в течение последовательных циклов зарядки-разрядки.
Базовая ячейкаПланта была позже улучшена другим французским инженером по имени Фор. Ему удалось значительно сократить процесс формования, нанеся на пластины несколько полосок оксида свинца. Это значительно ускорило процесс формования, поскольку отрицательная пластина стала только свинцовой, а положительная пластина окислилась до перекиси свинца.
После того, как была создана основная технология свинцово-кислотных аккумуляторов, следующим важным шагом стало решение проблемы потери воды и высыхания электролита.
Аккумуляторы требовали периодической доливки дистиллированной воды для обеспечения их работы. Это было преодолено путем вставки клапана в батарею. Эти свинцово-кислотные батареи с регулируемым клапаном, VRLA, использующие механизм рекомбинации кислорода.
Газы, образующиеся внутри батареи VRLA, были рекомбинированы внутри, и батарея была герметизирована для производства батарей, используемых для стандартных условий эксплуатации.
Основы свинцово-кислотных аккумуляторов: как они работают
При рассмотрении того, как работает свинцово-кислотный аккумулятор, необходимо обратить внимание на основные компоненты. Батарея состоит из сравнительно небольшого количества компонентов — по сути, это четыре основных элемента:
. Схема концепции свинцово-кислотного перезаряжаемого элемента- Положительная пластина: Она покрыта пастой из диоксида свинца.
- Отрицательная пластина: Изготовлена из губчатого свинца.
- Сепаратор: Это изолирующий материал между двумя пластинами, но он позволяет электролиту и ионам проникать в него, обеспечивая проводимость без соприкосновения двух пластин.
- Электролит: Состоит из воды и серной кислоты
Все эти компоненты находятся в пластиковом контейнере, который служит для удержания электролита и аккумулятора вместе.
Хотя пластины или электроды свинцово-кислотной батареи обозначены как свинцовые, сам по себе свинец слишком мягок, чтобы его можно было использовать отдельно. Соответственно, к свинцу добавляют небольшие количества других металлов, чтобы обеспечить необходимую дополнительную прочность. Они также могут улучшить электрические характеристики. Типичные аддитивные металлы включают: сурьму, кальций, олово и селен.
Общая батарея, как правило, состоит из нескольких элементов, соединенных последовательно, чтобы обеспечить требуемое напряжение, поскольку каждый элемент способен обеспечить ЭДС 2,1 вольта.
Зарядка свинцово-кислотных аккумуляторов
Чтобы основной свинцово-кислотный элемент мог вырабатывать напряжение, он должен сначала получить заряд. Напряжение, применяемое для обеспечения этого, должно быть больше 2,1 вольта, чтобы ток мог протекать в ячейку. Если бы он был меньше этого, из него действительно вытекал бы заряд.
Свинцово-кислотные аккумуляторы требуют зарядки постоянным током и постоянным напряжением. Для этого регулируемый ток повышает напряжение на клеммах аккумулятора или элемента до тех пор, пока не будет достигнут верхний предел напряжения заряда. В этот момент ток падает из-за насыщения.
Для этого регулируемый ток повышает напряжение на клеммах аккумулятора или элемента до тех пор, пока не будет достигнут верхний предел напряжения заряда. В этот момент ток падает из-за насыщения.
Время полной зарядки батареи обычно составляет от двенадцати до восемнадцати часов для наиболее распространенных типов батарей, но может достигать 36 или даже 48 часов для больших батарей, которые могут использоваться для временного питания и т. д.
Можно обеспечить быструю зарядку, используя более сложную форму зарядки, что потребует более сложного зарядного устройства, которое в конечном итоге будет стоить дороже. В некоторых ситуациях это может оказаться экономически эффективным подходом. Здесь более высокие токи и многоступенчатая зарядка позволяют аккумулятору не подвергаться чрезмерным нагрузкам при одновременном сокращении времени зарядки. Методами время зарядки можно сократить до восьми-десяти часов, но это не дает полной зарядки.
Хотя зарядка свинцово-кислотных аккумуляторов хорошо работает во многих приложениях, по сравнению с другими более новыми технологиями, такими как технология ионно-литиевых аккумуляторов, они относительно медленные.
После зарядки элемент или батарея смогут заряжать внешние цепи, часто работая в течение нескольких часов в зависимости от разрядки элемента или батареи.
Указания и советы по обслуживанию свинцово-кислотных аккумуляторов
Существует несколько советов и рекомендаций, позволяющих максимально эффективно использовать свинцовый аккумулятор путем его правильной зарядки. Это обеспечит безопасность, наилучшую работу и максимально длительный срок службы батареи.
Зарядка в хорошо проветриваемом помещении: Во время зарядки может образовываться газообразный водород, который, если он находится в небольшом пространстве, может быть взрывоопасным.
Не храните батареи в состоянии низкого заряда: Во избежание процесса, называемого сульфатацией, батареи не следует хранить в состоянии низкого заряда — в идеале их следует всегда заряжать после использования.
Избегайте «сплющивания» аккумулятора: Полная разрядка или сведение аккумулятора может значительно сократить срок его службы.
 Часто обнаруживается, что после полной разрядки автомобильного аккумулятора его емкость значительно снижается, и он, вероятно, снова полностью разрядится. Старые батареи, которые разряжены, следует заменить, чтобы избежать дополнительных проблем.
Часто обнаруживается, что после полной разрядки автомобильного аккумулятора его емкость значительно снижается, и он, вероятно, снова полностью разрядится. Старые батареи, которые разряжены, следует заменить, чтобы избежать дополнительных проблем.Убедитесь, что пластины батареи закрыты: В некоторых батареях необходимо долить электролит, чтобы пластины были закрыты. Это следует делать, используя дистиллированную воду (не обычную воду из-под крана, так как она содержит загрязняющие вещества, которые снижают эффективность электролита). Также никогда не добавляйте новый электролит. Для многих современных типов батарей, требующих минимального обслуживания, дозаправка не требуется, и для этого невозможно получить доступ к аккумуляторным отсекам.
Не переполняйте: При заполнении заполняйте только до указанного уровня. Переполнение может привести к выплескиванию кислоты во время зарядки.
Пузырьки газа на пластинах указывают на то, что аккумулятор практически полностью заряжен: Когда на пластинах так называемых залитых свинцово-кислотных аккумуляторов начинают появляться пузырьки газа, это означает, что аккумулятор полностью заряжен и начинает расщеплять молекулы воды на водород (отрицательная пластина) и кислород (положительная пластина).
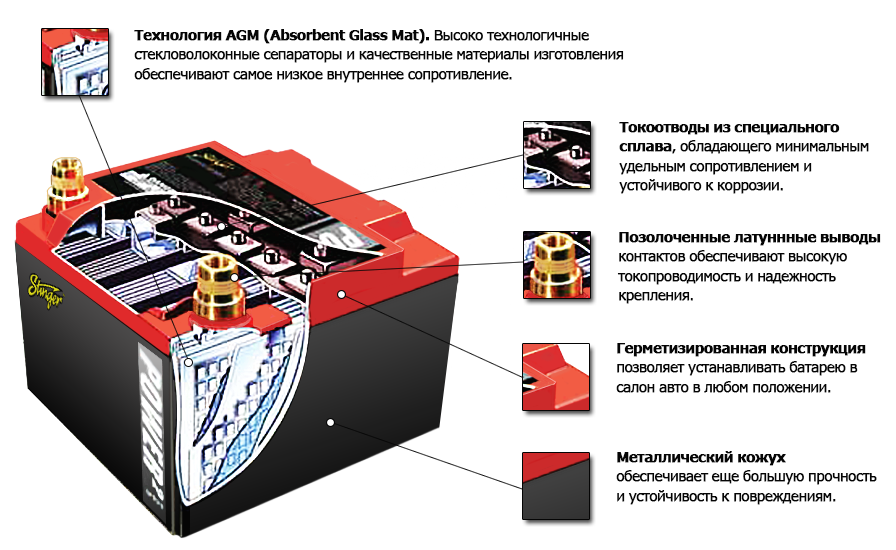
Избегайте зарядки при высоких температурах: Если температура выше 49 или 50°C, избегайте зарядки.
Не допускайте замерзания аккумулятора: Никогда не допускайте замерзания свинцово-кислотного аккумулятора, так как это может привести к непоправимому механическому повреждению. Стоит отметить, что полностью заряженный аккумулятор замерзает при более низкой температуре, чем частично заряженный.
Саморазряд свинцово-кислотного аккумулятора
Характеристики саморазряда свинцово-кислотных аккумуляторов относительно хорошие. При комнатной температуре 20°C скорость саморазряда составляет около 3% в месяц.
Теоретически свинцово-кислотная батарея может храниться до 12 месяцев без подзарядки. Однако при более высоких температурах саморазряд выше. При 30°C увеличивается саморазряд, и через 6 месяцев потребуется перезарядка. Падение заряда батареи ниже 60% в течение некоторого времени приводит к сульфатации.
Сульфатация — это процесс, снижающий емкость свинцово-кислотных аккумуляторов. При обычном использовании образуются маленькие кристаллы сульфата, но это нормально и не опасно. Однако при длительном отсутствии заряда аморфный сульфат свинца превращается в стабильный кристаллический и откладывается на отрицательных пластинах. Это приводит к образованию крупных кристаллов, которые уменьшают количество активного вещества внутри клетки и приводят к снижению ее емкости.
Преимущества и недостатки свинцово-кислотных аккумуляторов
Несмотря на то, что свинцово-кислотные аккумуляторы широко используются, поскольку они имеют ряд явных преимуществ, они также имеют несколько серьезных недостатков. Все это необходимо учитывать при принятии решения о том, использовать эту технологию или нет.
Преимущества свинцово-кислотных аккумуляторов
- Отработанная технология
- Относительно дешевы в производстве и покупке (они обеспечивают самую низкую стоимость единицы емкости аккумуляторных элементов)
- Большой ток
- Может быть изготовлен для различных применений
- Терпимость к злоупотреблениям
- Устойчив к перезарядке
- Доступен широкий диапазон размеров и спецификаций
- Многие производители по всему миру
Свинцово-кислотная батарея Недостатки
- Выход из строя через несколько лет Срок службы обычно 300–500 циклов
- Не всегда можно использовать в различных ориентациях
- Коррозионный электролит (может вызвать ожоги людей и коррозию металлических конструкций)
- Свинец не является экологически чистым
- Кислоту необходимо утилизировать с осторожностью
- Не подходит для быстрой зарядки
- Должен храниться в заряженном состоянии после введения электролита
- Типичная эффективность зарядки всего около 70 %
Как и все аккумуляторные технологии и аккумуляторные системы, свинцово-кислотные аккумуляторы имеют свои преимущества и недостатки. Преимущества и недостатки необходимо учитывать при рассмотрении аккумуляторной технологии для новой разработки. Для существующих систем это необходимо учитывать при обращении с ними, их использовании и обслуживании.
Преимущества и недостатки необходимо учитывать при рассмотрении аккумуляторной технологии для новой разработки. Для существующих систем это необходимо учитывать при обращении с ними, их использовании и обслуживании.
Свинцово-кислотный аккумулятор очень хорошо зарекомендовал себя. Он используется уже более 150 лет и является одной из опор автомобильной промышленности.
Свинцово-кислотная батарея обладает высокой токовой способностью, низкой стоимостью и устойчивостью к небрежному обращению. Это делает свинцово-кислотные аккумуляторы идеальными для многих применений.
Однако с переходом на более экологически безопасные источники энергии электромобили теперь представляются будущим, поскольку производители и законодательство указывают на поэтапный отказ от двигателей внутреннего сгорания. Для электромобилей литий-ионная технология обеспечивает лучшую производительность, они более экологически приемлемы и обладают характеристиками, позволяющими электромобилям добиться успеха. Таким образом, свинцово-кислотные батареи, вероятно, будут использоваться значительно реже.
Таким образом, свинцово-кислотные батареи, вероятно, будут использоваться значительно реже.
Другие электронные компоненты:
Резисторы
конденсаторы
Индукторы
Кристаллы кварца
Диоды
Транзистор
Фототранзистор
полевой транзистор
Типы памяти
Тиристор
Соединители
ВЧ-разъемы
Клапаны/трубки
Батареи
Переключатели
Реле
Технология поверхностного монтажа
Вернуться в меню «Компоненты». . .
Как работает свинцово-кислотный аккумулятор?
Поскольку вы читаете это, у вас, очевидно, есть вопросы о свинцово-кислотных аккумуляторах. Например, как работает свинцово-кислотный аккумулятор? Если на то пошло, что такое свинцово-кислотный аккумулятор?
Достаточно ли эффективны эти батареи для определенных целей или они устарели? Чем они отличаются от других аккумуляторов?
К счастью, у нас есть все ответы, которые вы искали прямо здесь, в этом руководстве. Начнем с того, что мы можем заверить вас, что эти батареи не устарели. На самом деле существует множество приложений, в которых идеально использовать свинцово-кислотные аккумуляторы.
На самом деле существует множество приложений, в которых идеально использовать свинцово-кислотные аккумуляторы.
Мы объясним это более подробно ниже. Мы также предоставляем подробное объяснение того, что такое свинцово-кислотный аккумулятор и как он работает. Читайте дальше, чтобы узнать все, что нужно знать о свинцово-кислотных батареях.
Что такое свинцово-кислотная батарея?
Свинцово-кислотная батарея — это перезаряжаемая батарея, в которой для работы используются свинец и серная кислота. Свинец погружают в серную кислоту, чтобы обеспечить контролируемую химическую реакцию.
Эта химическая реакция заставляет батарею производить электричество. Затем эта реакция меняется на обратную для перезарядки аккумулятора.
Хотите верьте, хотите нет, но этой технологии более 100 лет. Однако с момента его изобретения в 1859 году он был улучшен.и теперь он работает более эффективно.
Как работает свинцово-кислотный аккумулятор?
Проще говоря, электрический заряд батареи генерируется, когда сульфат в серной кислоте связывается со свинцом. Электрический заряд восполняется за счет обращения этой реакции вспять. То есть сульфат снова уходит в серную кислоту и, таким образом, аккумулятор подзаряжается.
Электрический заряд восполняется за счет обращения этой реакции вспять. То есть сульфат снова уходит в серную кислоту и, таким образом, аккумулятор подзаряжается.
Теперь очевидно, что в кислоте есть конечное количество ионов сульфата. И доступная площадь поверхности свинца, к которому он прикрепляется, также ограничена. Итак, по мере истощения сульфата заряд становится слабее.
По этой причине свинцово-кислотные аккумуляторы не подходят для питания устройств в течение длительного периода времени. Вместо этого они лучше всего подходят для приложений, которым нужен короткий мощный всплеск энергии.
Саморазряд свинцово-кислотного аккумулятора
Одним из досадных недостатков свинцово-кислотных аккумуляторов является то, что описанную выше химическую реакцию невозможно полностью остановить. Другими словами, эти батареи будут продолжать разряжаться, даже если они не используются.
Обычно этот саморазряд происходит несколько медленно, около 1% теряется в день. Но некоторые факторы будут увеличивать этот показатель. Например, чем теплее аккумулятор, тем быстрее он саморазряжается.
Но некоторые факторы будут увеличивать этот показатель. Например, чем теплее аккумулятор, тем быстрее он саморазряжается.
Кроме того, некоторые устройства немного расходуют заряд аккумулятора, даже когда они выключены. Хорошим примером этого являются настройки звука в вашем автомобиле. Ваш автомобильный радиоприемник использует энергию аккумулятора, чтобы «запомнить» эти настройки.
В любом случае вам придется время от времени перезаряжать свои свинцово-кислотные аккумуляторы, иначе они разрядятся.
Выход из строя свинцово-кислотного аккумулятора
Итак, что же приводит к выходу из строя свинцово-кислотного аккумулятора? Определенные факторы могут повредить или изменить материалы, необходимые для проведения необходимой химической реакции. Одним из таких факторов является то, что батарея слишком долго остается в частично разряженном состоянии.
Частичный разряд
Когда аккумулятор разряжается, в нем уменьшается количество раствора электролита (серная кислота, смешанная с водой). Это оставляет свинцовые пластины частично открытыми.
Это оставляет свинцовые пластины частично открытыми.
Если они останутся незащищенными, сульфат, уже связанный со свинцом, может затвердеть. Затем он остается постоянно включенным, что снижает способность аккумулятора к перезарядке.
Этот частичный разряд является распространенной проблемой автомобильных аккумуляторов. Видите ли, аккумулятор заряжается, когда вы едете. Но если вы ездите нечасто или совершаете очень короткие поездки, ваша батарея может никогда не зарядиться полностью.
Глубокий разряд
Другой распространенной причиной выхода из строя батареи является глубокий разряд. Это когда ваш свинцово-кислотный аккумулятор разряжен ниже 50%.
Когда это происходит, маленькие кусочки свинцовых пластин могут отколоться и погрузиться в раствор электролита. Тогда остается меньше материала, способного вызвать химическую реакцию. Если отломать слишком много, реакции вообще не будет.
Вот почему автомобильный аккумулятор приходит в негодность, если вы случайно не включили фары на ночь. Даже если вы сможете перезапустить разряженную батарею, ущерб уже нанесен. Аккумулятор окончательно разряжен и подлежит замене.
Даже если вы сможете перезапустить разряженную батарею, ущерб уже нанесен. Аккумулятор окончательно разряжен и подлежит замене.
Перезарядка
Перезарядка происходит, когда вы продолжаете заряжать уже полностью заряженный аккумулятор. Это может привести к разрушению материала электролита. Как только это происходит, не остается сульфата, связывающего свинец.
Вот почему вы не хотите постоянно держать свинцово-кислотную батарею подключенной к зарядному устройству. Лучше включать его только время от времени.
Плюсы и минусы свинцово-кислотных аккумуляторов
Свинцово-кислотные аккумуляторы имеют высокое напряжение для своего размера. Таким образом, они могут питать мощные инструменты и оборудование.
Они могут даже приводить в действие электромобили, такие как тележки для гольфа. Однако в этом случае вам нужно быть осторожным, чтобы заряжать аккумулятор достаточно часто (и не перезаряжать его). Если вы этого не сделаете, транспортное средство умрет, не доехав до места назначения, что также повредит аккумулятор.
Кроме того, свинцово-кислотные аккумуляторы отлично подходят для запуска автомобилей. Они обеспечивают интенсивный выброс энергии для запуска автомобиля, а затем перезаряжаются во время движения автомобиля.
С другой стороны, они не подходят для устройств, которые вы хотите использовать в течение длительного времени, таких как мобильные телефоны. Кроме того, они саморазряжаются, когда не используются, что в конечном итоге убивает батарею.
Другими словами, вы не можете оставить их без дела. Таким образом, они являются плохим вариантом для любого приложения, которое не будет использоваться часто.
Для чего вы будете использовать свинцово-кислотные батареи?
Теперь, когда вы получили ответы на свои вопросы, воспользуйтесь этим руководством, чтобы определить, подходят ли свинцово-кислотные аккумуляторы для ваших нужд. Кроме того, знаете ли вы кого-нибудь еще, кто задается вопросом: «Как работает свинцово-кислотный аккумулятор?» Если да, поделитесь с ними этим руководством.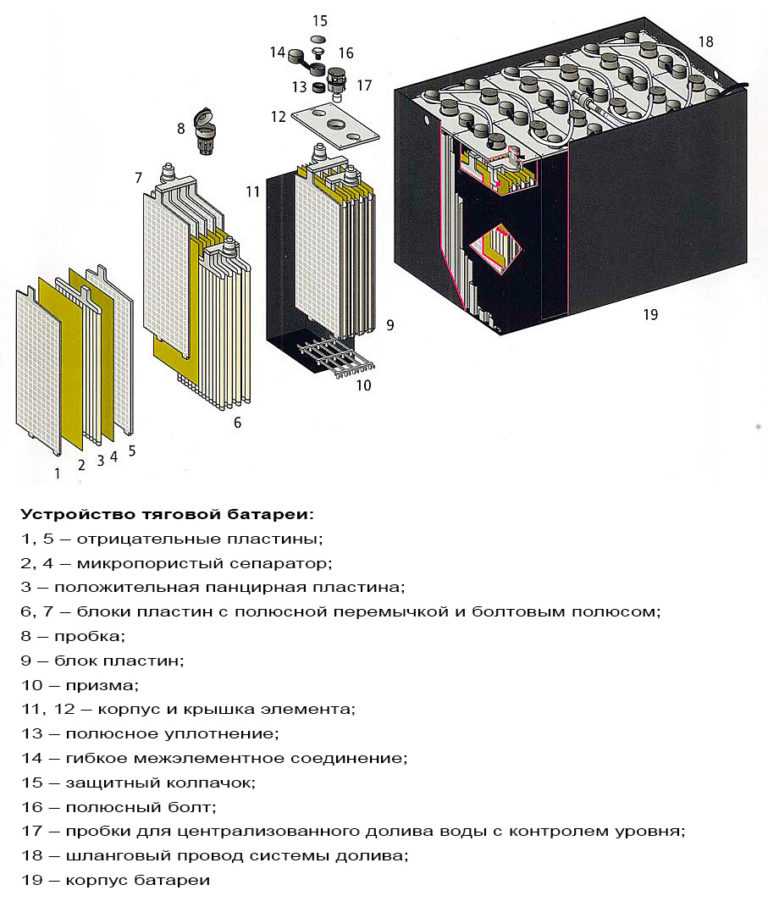
Дополнительные сведения см. в статье Внутри батареи: как это все работает.
Как работает свинцово-кислотный аккумулятор? – Аксессуары для аккумуляторов
Сегодня мы рассмотрим, что такое свинцово-кислотные аккумуляторы и как они могут вписаться в ваши промышленные аккумуляторы. Мы будем смотреть, как они работают и как вы можете эффективно ухаживать за ними.
Многие приложения работают более эффективно со свинцово-кислотными батареями, а с правильной BMS (системой управления батареями) ваши свинцово-кислотные батареи будут работать эффективно и эффективно для вашего бизнеса, экономя ваше время и деньги и позволяя вашим батареям максимизировать производительность.
Что такое свинцово-кислотная батарея? По сути, свинцово-кислотная батарея — это перезаряжаемая батарея, в которой для работы используется как свинец, так и серная кислота. Когда свинец погружают в серную кислоту, возникает контролируемая химическая реакция; химическая реакция заставляет батарею производить электричество. Чтобы перезарядить свинцово-кислотный аккумулятор, эта реакция обратная.
Чтобы перезарядить свинцово-кислотный аккумулятор, эта реакция обратная.
Свинцово-кислотные батареи не являются новой технологией; Изобретенная в 1959 году, свинцово-кислотная батарея с годами значительно улучшилась. Версии свинцово-кислотных аккумуляторов можно проследить гораздо раньше, до 179 г.1, где Луиджи Гальвани создал «корытообразную» батарею, которая позже изобрела гальваническую батарею. Мало того, что свинцово-кислотные батареи очень эффективны, существует также множество инновационных аккумуляторных продуктов, которые помогают эффективно обслуживать и управлять батареями для вашего бизнеса.
Как работает свинцово-кислотный аккумулятор?Проще говоря, электрический заряд свинцово-кислотной батареи генерируется, когда сульфат в серной кислоте связывается со свинцом. Ему дается электронный заряд, который заряжает батарею, и сульфат возвращается в серную кислоту.
В кислоте содержится определенное количество сульфат-ионов, и площадь поверхности свинца, с которой она связывается, также ограничена. По мере истощения сульфата заряд свинцово-кислотного аккумулятора начинает ослабевать. Это означает, что их лучше всего использовать для приложений, которым требуется короткий и мощный всплеск энергии.
По мере истощения сульфата заряд свинцово-кислотного аккумулятора начинает ослабевать. Это означает, что их лучше всего использовать для приложений, которым требуется короткий и мощный всплеск энергии.
Свинцово-кислотные батареи могут и будут саморазряжаться, и эту реакцию невозможно полностью остановить. Они будут продолжать разряжаться, даже если они не используются. Хотя скорость саморазряда очень низкая, около 1% в день, некоторые факторы могут увеличить эту скорость, например, температура батареи.
Поэтому необходима система управления батареями, поскольку она означает, что свинцово-кислотные батареи будут контролироваться, поддерживаться при правильной температуре, чередоваться и поливать. BMS будет знать, какие батареи заряжать и когда. Они даже дадут пользователю знать, какую батарею использовать следующей из аккумуляторной.
Что приводит к выходу из строя свинцово-кислотного аккумулятора? Различные факторы могут повредить и изменить материалы, необходимые для химической реакции.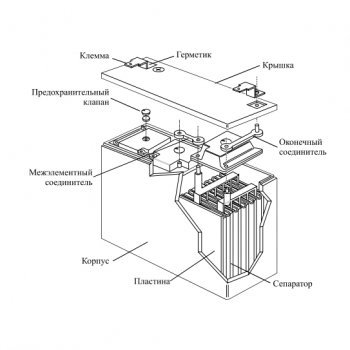 Одной из основных причин выхода из строя батареи является то, что батарея может оставаться в частично разряженном состоянии в течение длительного периода времени. Различают три основных типа выделений:
Одной из основных причин выхода из строя батареи является то, что батарея может оставаться в частично разряженном состоянии в течение длительного периода времени. Различают три основных типа выделений:
Частичный разряд — Когда батарея разряжается, раствор электролита опускается, оставляя свинцовые пластины частично открытыми. Если оставить его открытым на какое-то время, сульфат, который уже связан со свинцом, может начать затвердевать. Если его не лечить, сульфат остается на проводе и не дает аккумулятору правильно заряжаться.
Эта проблема может быть характерна для автомобильных аккумуляторов, поскольку во время движения аккумулятор заряжается сам. Если вы редко водите машину или совершаете несколько коротких поездок, аккумулятор может никогда не зарядиться полностью.
Глубокий разряд . Еще одной серьезной причиной выхода из строя батареи является глубокая разрядка, когда свинцово-кислотная батарея разряжена ниже 50%. Это означает, что мелкие кусочки свинцовых пластин могут отколоться и погрузиться в раствор электролита.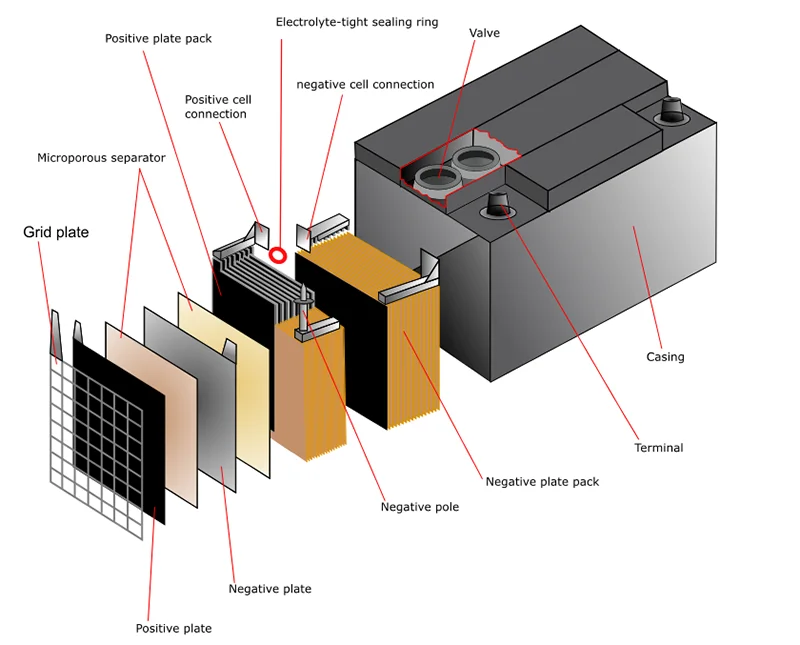 Это означает, что меньше свинцовой поверхности доступно для химической реакции, необходимой для эффективной работы батарей. Если отрывается слишком много свинца, то реакция полностью остановится. Это может означать, что ваши батареи окончательно испорчены и их необходимо заменить.
Это означает, что меньше свинцовой поверхности доступно для химической реакции, необходимой для эффективной работы батарей. Если отрывается слишком много свинца, то реакция полностью остановится. Это может означать, что ваши батареи окончательно испорчены и их необходимо заменить.
Перезарядка — Как следует из названия, это когда свинцово-кислотная батарея продолжает заряжаться, когда она уже полностью заряжена. Перезарядка может разрушить материал электролита, в результате чего не останется сульфата, который мог бы связываться со свинцом. Свинцово-кислотный аккумулятор нельзя подключать к зарядному устройству, если его не нужно заряжать.
Почему выбирают свинцово-кислотные аккумуляторы? Несмотря на меньшие размеры, свинцово-кислотные аккумуляторы имеют очень мощное напряжение и являются отличным вариантом для тяжелонагруженного оборудования и инструментов. Мало того, они также могут питать электромобили, такие как багги для гольфа и поломоечные машины. Они также отлично подходят для автомобилей, так как когда вы запускаете двигатель, они создают интенсивный толчок энергии для запуска автомобиля, и они перезаряжаются, когда вы ведете машину.
Они также отлично подходят для автомобилей, так как когда вы запускаете двигатель, они создают интенсивный толчок энергии для запуска автомобиля, и они перезаряжаются, когда вы ведете машину.
Всеми обсуждаемыми проблемами можно легко управлять с помощью системы управления батареями в аккумуляторных помещениях вашей компании, такой как iBOS. BMS позаботится обо всех аспектах ваших свинцово-кислотных аккумуляторов, чтобы их срок службы был как можно дольше. Они помогают сократить время, затрачиваемое вручную на проверку всех параметров аккумуляторов, таких как температура, полив и зарядка, с помощью дополнительного монитора срока службы аккумулятора, такого как eGO! Ассортимент мониторов времени автономной работы. Он расскажет вам историю жизни батареи, измеряя производительность и предсказывая, когда батарею необходимо заменить, поможет выявить любые проблемы до того, как они приведут к повреждению, и предоставит важные данные о батарее, которые помогут при принятии решений о покупке для вашего бизнеса.
Что делает автомобильный аккумулятор и как он работает?
Традиционные свинцово-кислотные автомобильные аккумуляторы в настоящее время могут быть упущены из виду из-за безумия по поводу литий-ионных аккумуляторов для электромобилей, но эти маленькие ребята представляют собой бесценные чудеса инженерной мысли, которые десятилетиями помогали транспортным средствам питаться.
Без сложных химических реакций внутри 12-вольтовой аккумуляторной батареи вашего автомобиля вы даже не смогли бы завести автомобиль или тем более выключить электрические стеклоподъемники. Читайте дальше, чтобы узнать об оригинальных способах работы вашего автомобильного аккумулятора и о том, как он объединяется с генератором автомобиля, чтобы сделать ваш автомобиль лучшим местом для времяпрепровождения.
Как работает автомобильный аккумулятор 12 В?
Автомобильный аккумулятор работает с химическими реакциями. По сути, он переносит электроны между анодом (отрицательным выводом) туда, где они на самом деле хотят быть: катод (положительный вывод). Например, свинцово-кислотная батарея, используемая в большинстве автомобилей, получила свое название из-за того, что в ней используются пластины из диоксида свинца (и чистого свинца), погруженные в смесь воды и серной кислоты.
Например, свинцово-кислотная батарея, используемая в большинстве автомобилей, получила свое название из-за того, что в ней используются пластины из диоксида свинца (и чистого свинца), погруженные в смесь воды и серной кислоты.
Эти аккумуляторы на самом деле имеют шесть элементов, каждый из которых вырабатывает около 2 В, поэтому автомобильные аккумуляторы обычно называют аккумуляторами на 12 В, хотя они не совсем 12 В. Каждая из этих шести ячеек состоит из пластин из диоксида свинца (положительный катод) и свинцовых пластин (отрицательный анод), которые погружаются в смесь серной кислоты и воды, чтобы вызвать химические реакции, которые в конечном итоге помогут батарее высвобождать электричество.
Имейте в виду, что батарея состоит из шести элементов, и каждый из них имеет различные пластины. Но в основе этого процесса лежит взаимодействие между положительной и отрицательной клеммами. Когда диоксид свинца катода взаимодействует с сульфатом в кислой смеси, ионы кислорода высвобождаются в смесь, где они взаимодействуют с водородом с образованием воды. Между тем, с отрицательной стороны, сульфат реагирует со свинцом в аноде, создавая слой сульфата свинца на аноде и высвобождая электроны.
Между тем, с отрицательной стороны, сульфат реагирует со свинцом в аноде, создавая слой сульфата свинца на аноде и высвобождая электроны.
Эти электроны накапливаются в отрицательной клемме и определенно не хотят там находиться, но они не могут проходить через раствор электролита, поэтому они направляются через отрицательную клемму и через цепь, пока в конечном итоге не достигнут положительной клеммы. Это основной принцип работы автомобильного аккумулятора, так как все остальные вспомогательные устройства в вашем автомобиле подключаются к этой цепи.
Но это работает только при выключенной машине; в противном случае то, что на самом деле питает электронику вашего автомобиля, — это генератор переменного тока. Аккумулятор, по сути, находится в вашем автомобиле для питания стартера, когда автомобиль выключен, но как только стартер оживляет двигатель, генератор вступает во владение. Генератор переменного тока также заряжает батарею за счет реверсирования процессов, которые привели к ее разрядке.
Что делает генератор?
Как было сказано ранее, генератор переменного тока в основном выполняет работу, которую, по мнению людей, постоянно выполняет батарея. Помните, что аккумулятор быстро разряжается, если ему приходится питать все ваши стеклоподъемники, радио и вообще любое другое электронное устройство в вашем автомобиле. Итак, решение этой проблемы весьма изобретательно.
Инженеры установили в ваш автомобиль генератор переменного тока, работающий от двигателя вместо аккумулятора. Он производит достаточно электроэнергии для питания всех электрических битов вашего автомобиля. Самое замечательное в генераторе переменного тока то, что он также заряжает аккумулятор при работающем двигателе автомобиля, потому что аккумулятор действительно сильно разряжается после выполнения своей работы по запуску двигателя.
Единственная проблема генератора переменного тока заключается в том, что он вырабатывает переменный ток, который необходимо преобразовать в постоянный. Чтобы решить эту проблему, переменный ток обрабатывается выпрямителем, что позволяет генератору переменного тока выкачивать требуемый постоянный ток.
Чтобы решить эту проблему, переменный ток обрабатывается выпрямителем, что позволяет генератору переменного тока выкачивать требуемый постоянный ток.
Когда генератор выходит из строя, вы начинаете повсюду замечать признаки этого. Например, электроника вашего автомобиля не будет работать правильно, и ваши фары могут внезапно погаснуть. В этих условиях ваш автомобиль может начать выдавать кучу кодов, и даже если вы подключите его к приложению OBD2, он, вероятно, не определит, что проблема на самом деле в генераторе или аккумуляторе.
Что еще хуже, во многих транспортных средствах используются усовершенствованные модули, которые откалиброваны для работы с очень малыми допусками. Если ваш генератор или аккумулятор вышли из строя, весь автомобиль может начать работать хаотично и выдавать коды, совершенно не связанные с реальной проблемой: неисправность аккумулятора или генератора.
Является ли автомобильный аккумулятор таким же, как аккумулятор электромобиля?
Нет, это не то же самое, что аккумулятор в вашем электромобиле. Свинцово-кислотные аккумуляторы значительно отличаются от литий-ионных аккумуляторов вашего электромобиля. Прежде всего, как вы уже узнали, состав свинцово-кислотных аккумуляторов в основном состоит из свинца и смеси воды и серной кислоты. С другой стороны, литий-ионные батареи состоят из таких материалов, как литий, кобальт и графит.
Свинцово-кислотные аккумуляторы значительно отличаются от литий-ионных аккумуляторов вашего электромобиля. Прежде всего, как вы уже узнали, состав свинцово-кислотных аккумуляторов в основном состоит из свинца и смеси воды и серной кислоты. С другой стороны, литий-ионные батареи состоят из таких материалов, как литий, кобальт и графит.
Кроме того, литий-ионные аккумуляторы имеют более высокую плотность энергии, чем свинцово-кислотные аккумуляторы, что особенно идеально подходит для высокопроизводительных электромобилей и электроники, где крайне важны компактность и вес.
Свинцово-кислотные батареи также имеют меньший жизненный цикл по сравнению с литий-ионными батареями. Это означает, что вы можете заряжать и разряжать литий-ионный аккумулятор во много раз чаще, чем свинцово-кислотный аккумулятор. Это, безусловно, огромный плюс для использования в электромобилях, где батарея является наиболее важным и дорогим компонентом, а некачественный жизненный цикл сделает ее бесполезной. Свинцово-кислотные батареи также требуют регулярного обслуживания, чтобы поддерживать их работу, в то время как литий-ионные батареи относительно не требуют обслуживания в течение всего срока службы.
Свинцово-кислотные батареи также требуют регулярного обслуживания, чтобы поддерживать их работу, в то время как литий-ионные батареи относительно не требуют обслуживания в течение всего срока службы.
Легко понять, почему литий-ионные батареи используются в электромобилях вместо традиционных свинцово-кислотных батарей. Если бы в электромобилях использовались свинцово-кислотные батареи, они были бы безумно тяжелыми и маломощными.
Свинцово-кислотные аккумуляторы все еще имеют свое место
Несмотря на недостатки, связанные со свинцово-кислотными аккумуляторами, они занимают свое место в автомобильной среде. Их относительно низкая стоимость по сравнению с литий-ионными батареями гарантирует, что они будут продолжать использоваться в автомобилях с бензиновым двигателем и других устройствах, где первоначальная стоимость является важным фактором.
Эти аккумуляторы используются в транспортных средствах уже много лет, и хотя литий-ионная технология является блестящей новинкой, свинцово-кислотные аккумуляторы всегда будут занимать свое место в автомобильной истории.
Должны ли вы выбрать свинцово-кислотную батарею для хранения солнечной энергии?
Свинцово-кислотная батарея — это тип перезаряжаемой батареи, в которой электрическая энергия накапливается за счет химических реакций между свинцом, водой и серной кислотой. Технологии, лежащей в основе этих батарей, уже более 160 лет, но причина, по которой они все еще так популярны, заключается в том, что они прочны, надежны и дешевы в производстве и использовании.
Если вы хотите хранить энергию, вырабатываемую солнечной батареей, свинцово-кислотные батареи могут быть хорошим выбором, но новые технологии могут оказаться более удобными и компактными.
Статья ниже посвящена свинцово-кислотным батареям для хранения солнечной энергии, но у нас также есть более общая статья о домашних солнечных батареях.
На этой странице
… Показать больше
Как работает свинцово-кислотный аккумулятор
Хотя химический состав свинцово-кислотных аккумуляторов довольно прост, написание всех химических уравнений может показаться очень сложным, поэтому мы Попытаюсь объяснить это без всего этого.
Простейшая версия свинцово-кислотной батареи состоит из трех компонентов:
- Металлическая пластина из свинца и сурьмы с отрицательным зарядом
- Положительно заряженная металлическая пластина из диоксида свинца
- Смесь серной кислоты и воды
Отрицательная пластина называется анодом, положительная пластина называется катодом, а смесь вода/кислота называется электролитом.
Простая свинцово-кислотная батарея. Источник изображения: LibreTexts.org
Когда пластины подвешены в электролитной смеси и подключены к проводам, батарея готова к выработке электроэнергии!
Когда электроны вытекают из батареи, кислота в электролите начинает прилипать к свинцу на электродах, превращая их внешние поверхности в сульфат свинца и оставляя дополнительные ионы водорода, плавающие в воде.
По мере того, как электроны перемещаются по проводам, на пластинах образуется сульфат свинца, пока батарея разряжается. Источник: Динамическая наука
Источник: Динамическая наука
Зарядка батареи добавляет электроны обратно и разрывает электрохимические связи между свинцом и сульфатом. Сульфат рекомбинирует со свободными ионами водорода в электролите, снова образуя серную кислоту.
Свинцово-кислотная конструкция имеет недостаток. Если батарея разряжена слишком сильно, часть сульфата свинца не может быть расщеплена и воссоединена со свободным водородом, что приводит к постоянному покрытию свинцовых пластин, называемому сульфатированием. Сульфатация значительно сокращает срок службы аккумулятора.
Чтобы свинцово-кислотные аккумуляторы могли работать в течение длительного периода времени, их необходимо регулярно разряжать не более чем на половину их общей емкости.
Автомобильные аккумуляторы и аккумуляторы глубокого цикла
Автомобильные аккумуляторы плохо подходят для хранения энергии в домашних условиях, поскольку они предназначены для выработки коротких импульсов электричества, которые используются для запуска автомобиля. На самом деле, эти типы батарей называются пусковыми, осветительными и запальными (SLI).
На самом деле, эти типы батарей называются пусковыми, осветительными и запальными (SLI).
Аккумуляторы SLI изготовлены из тонких пористых свинцовых пластин, которые предназначены для получения максимально возможного количества электроэнергии из электролита за один раз. Этот всплеск энергии называется током и измеряется в амперах.
Автомобильные аккумуляторы состоят из 6 элементов, соединенных последовательно. Когда батарея полностью заряжена, каждая ячейка вырабатывает около 2 вольт, что приводит к общему напряжению 12 вольт. Вольты, умноженные на ампер, равны мощности в ваттах или общей мощности, доступной за один раз.
Узнать больше : Амперы, вольты и ватты
Аккумуляторы глубокого цикла для хранения солнечной энергии не должны производить кучу мгновенной мощности, чтобы запустить что-либо, поэтому они имеют более толстые свинцовые пластины, которые прослужат долгое время и потребляют энергию от электролита. медленнее и равномернее.
Батареи глубокого цикла для хранения солнечной энергии
Аккумуляторы глубокого цикла, как правило, представляют собой большие прямоугольные коробки, сделанные из пластикового композитного материала, что облегчает их штабелирование рядом друг с другом. Поскольку им не нужно заводить автомобиль, они могут производить меньше мощности по отдельности и могут быть соединены вместе, чтобы создать батареи.
Поскольку им не нужно заводить автомобиль, они могут производить меньше мощности по отдельности и могут быть соединены вместе, чтобы создать батареи.
Многие аккумуляторы глубокого цикла для хранения энергии имеют только один большой элемент и вырабатывают 2 вольта. И чем больше клетка, тем больше энергии она может хранить. Другие конструкции с 2, 3 и 6 элементами встречаются в батареях мощностью 4, 6 и 12 Вт соответственно. Аккумуляторы, предназначенные для хранения солнечной энергии, соединены вместе для получения 12, 24 или 48 вольт.
Например, шесть 2-вольтовых батарей можно соединить последовательно (от отрицательного к положительному по всей линии), чтобы получить 12-вольтовую батарею, или четыре 12-вольтовые батареи можно соединить последовательно, чтобы получить 48-вольтовую батарею. банк аккумуляторов.
Если вы думаете об электричестве, как о воде, то напряжение батареи соответствует давлению в шланге. Более высокое давление означает большую скорость потока. Сила тока, измеряемая в амперах, определяет ширину отверстия шланга. Вместе они определяют мощность или скорость потока.
Сила тока, измеряемая в амперах, определяет ширину отверстия шланга. Вместе они определяют мощность или скорость потока.
Способность накапливать энергию измеряется в ампер-часах за 20 часов, что означает, что она измеряется количеством энергии, которое потребуется для разрядки батареи за 20 часов. Представьте себе шланг, прикрепленный к бочке. Большая батарея похожа на большую бочку, потому что она содержит больше энергии (воды).
Вы можете увидеть 2-вольтовую батарею, рассчитанную на 1100 ампер-часов. Это означает, что батарея может выдавать 55 ампер в течение 20 часов. При напряжении 2 вольта это означает, что батарея будет производить 110 ватт в любой момент времени (2 вольта х 55 ампер = 110 ватт).
Но 2 вольта это не очень высокое напряжение. Это все равно, что держать шланг на одном уровне со стволом. За ним много воды, но она просто вытекает. Идея состоит в том, чтобы создать большее давление, чтобы энергия могла течь с большей скоростью.
Последовательное соединение аккумуляторов для повышения напряжения подобно добавлению давления в воду . Возьмем блок батарей из предыдущего: последовательное соединение шести 2-вольтовых батарей не увеличивает накопленную энергию, а просто увеличивает скорость ее течения за счет давления в «шланге».
Возьмем блок батарей из предыдущего: последовательное соединение шести 2-вольтовых батарей не увеличивает накопленную энергию, а просто увеличивает скорость ее течения за счет давления в «шланге».
В этом случае серия батарей по-прежнему может производить 55 ампер в течение 20 часов, но на этот раз они производят его при 12 вольтах, что в сумме составляет 660 ватт (55 ампер на 12 вольт).
И наоборот, параллельное соединение двух батарей увеличивает силу тока, но не напряжение . Параллельная проводка соединяет отрицательные клеммы обеих батарей и положительные клеммы обеих батарей. Параллельное подключение допустимо, если вы соединяете батареи на 12 вольт вместе, но большинству людей понадобится блок батарей, который может производить 24 или 48 вольт; в этом случае их нужно будет соединить последовательно-параллельно.
Последовательно-параллельное соединение соединяет два или более ряда батарей, соединенных последовательно. Это увеличивает как общую накопленную энергию, так и напряжение, как показано на изображении ниже.
Проектирование блока аккумуляторов
Проектирование блока аккумуляторов для хранения солнечной энергии — это поиск правильного напряжения, правильного тока и правильного количества накопленной энергии.
Большинству домов требуется около 900 киловатт-часов (кВтч) электроэнергии в месяц или 30 кВтч в день. Чтобы удовлетворить эти потребности, вам понадобится аккумуляторная батарея, способная хранить 625 ампер-часов при 48 вольтах.
Важным правилом проектирования аккумуляторной батареи является не допускать силы тока более 100 ампер. Основная идея здесь состоит в том, чтобы построить банк батарей с достаточно высоким напряжением, чтобы ток не превышал 100 ампер .
Напряжение батареи падает по мере разрядки батареи после полной зарядки, поэтому важно учитывать это при планировании банка батарей. Если вы планируете использовать много бытовых приборов только от батареи, рекомендуется выбрать аккумуляторную батарею на 48 вольт, чтобы вы могли потреблять до 4800 Вт за раз.
Когда вы используете бытовую технику, каждая из них требует определенного количества энергии, и большинство из них имеют рабочую мощность и более высокую мощность при запуске. В идеале банк батарей сможет удовлетворить все ваши потребности, когда работает несколько устройств.
Различные типы свинцово-кислотных аккумуляторов глубокого цикла для солнечных батарей
Вот где резина встречается с дорогой. Существует три основных типа свинцово-кислотных аккумуляторов глубокого цикла, каждый из которых имеет свои преимущества и недостатки. К ним относятся:
- Залитые свинцово-кислотные аккумуляторы
- Аккумуляторы с абсорбирующим стекловолокном (AGM)
- Гелевые аккумуляторы
Первый тип недорог и долговечен, но требует регулярного обслуживания, чтобы поддерживать баланс электролита с водой внутри корпуса батареи.
Два других подпадают под более широкую категорию «герметичных свинцово-кислотных аккумуляторов». Несмотря на то, что они не требуют обслуживания за счет герметизации электролита внутри корпуса, они также дороже и могут не прослужить так долго.
Несмотря на то, что они не требуют обслуживания за счет герметизации электролита внутри корпуса, они также дороже и могут не прослужить так долго.
Залитые свинцово-кислотные аккумуляторы
Наименее сложными и наименее дорогими типами аккумуляторов глубокого разряда являются залитые свинцово-кислотные (FLA) аккумуляторы. Эти батареи больше всего похожи на изображение простой свинцово-кислотной батареи, показанной ниже, с цилиндрическими свинцовыми пластинами, погруженными в электролитную ванну с водой и кислотой.
Восемь 6-вольтовых залитых свинцово-кислотных аккумуляторов составляют батарею на 48 В. Источник изображения: Otherpower.com
Батареи FLA могут быть недорогими, но за ними также сложно ухаживать, поскольку электролит внутри корпуса батареи со временем испаряется, что требует регулярного добавления дистиллированной воды. Если вы не будете добавлять воду достаточно часто, срок службы батареи значительно сократится.
Поскольку батареи FLA предназначены для открывания, их необходимо хранить в вертикальном положении и обеспечивать достаточную вентиляцию, чтобы предотвратить скопление газообразного водорода, выделяющегося при разрядке батареи. Это означает, что хранение банка аккумуляторов FLA глубокого цикла, подходящих для домашнего хранения энергии, может занимать много места, как показано на изображении выше .
При правильном уходе и регулярной разрядке не более чем на половину своей емкости батареи FLA могут прослужить от 5 до 8 лет в домашней системе хранения энергии.
Герметичные свинцово-кислотные аккумуляторы
Как следует из названия, герметичные свинцово-кислотные (SLA) аккумуляторы нельзя вскрывать и не требуют доливки воды.
Набор герметичных свинцово-кислотных аккумуляторов для использования в автодомах. Источник изображения: AM Solar
Вместо этого они используют один из двух методов, чтобы удержать почти всю воду, присутствующую в электролите, внутри корпуса батареи: либо путем добавления поглощающих сепараторов из стекловолокна между положительной и отрицательной пластинами, либо путем превращения электролита в гель. Благодаря такой конструкции батареи SLA можно класть на бок и складывать друг на друга для удобства хранения .
Благодаря такой конструкции батареи SLA можно класть на бок и складывать друг на друга для удобства хранения .
Несмотря на эти улучшения, аккумуляторы SLA по-прежнему нуждаются в вентиляции, чтобы предотвратить накопление газообразного водорода. Это вентиляционное отверстие управляется клапаном, поэтому батареи SLA иногда также называют «свинцово-кислотными батареями с клапанным регулированием» или батареями VRLA.
Как упоминалось выше, существует два основных типа аккумуляторов SLA: абсорбирующий стекломат (AGM) и гелевые аккумуляторы.
Аккумуляторы AGM (впитывающий стеклянный мат)
Аккумуляторы AGM были разработаны, когда производители аккумуляторов искали лучший способ держать электролит близко к пластинам для использования в устройствах с высокой вибрацией, таких как тележки для гольфа.
Мат в данном случае изготовлен из тонкой стекловолоконной сетки, похожей на марлевую прокладку, и помещается между отрицательной и положительной пластинами в каждой из ячеек батареи.
Пример внутренних частей типичной батареи AGM. Источник изображения: Bosch
Поскольку аккумулятор AGM улавливает почти весь электролит внутри аккумулятора, его можно разряжать на большую глубину, позволяя сульфату рекомбинировать со свободным водородом.
Высококачественные аккумуляторы AGM могут быть разряжены до 80% своей емкости в течение сотен циклов и обычно служат от 4 до 6 лет в домашней установке для хранения энергии. Разрядка до уровня не более 50% по-прежнему рекомендуется для максимального срока службы батареи.
Однако за эти преимущества приходится платить. Аккумуляторы AGM обычно стоят в 1,5–2 раза дороже за киловатт-час (кВтч) накопленной энергии. Аккумуляторы AGM также занимают немного больше места на кВтч, но, опять же, их можно складывать на бок, чтобы сэкономить место в домашней системе хранения.
Выбирайте AGM-аккумуляторы для хранения солнечной энергии, если вы предпочитаете не соблюдать строгий график тестирования и полива FLA-аккумуляторов, вам нужны универсальные варианты монтажа и долгий срок службы, и вы готовы за это платить .
Гелевые аккумуляторы
Как и аккумуляторы AGM, гелевые аккумуляторы удерживают электролит внутри аккумулятора и предотвращают его испарение или проливание.
В этой конструкции серная кислота взвешена в силикагеле, что делает аккумулятор очень стабильным и имеет низкую скорость саморазряда в течение длительных периодов времени.
Пример гелевой батареи глубокого цикла. Источник изображения: Taico
Гелевые аккумуляторы являются самыми безопасными свинцово-кислотными аккумуляторами, поскольку они выделяют очень мало газообразного водорода из своих вентиляционных клапанов. Они хорошо работают в местах, где высокие температуры вызывают беспокойство, и могут быть разряжены ниже 50% и сохраняют свой срок службы.
Недостатки гелевых аккумуляторов заключаются в том, что они сохраняют меньше энергии в том же объеме, что и другие типы свинцово-кислотных аккумуляторов, а гелевые плохо работают при низких температурах.
Кроме того, гелевые аккумуляторы требуют осторожной зарядки с помощью специальных интеллектуальных зарядных устройств, которые предназначены для ограничения напряжения, используемого для зарядки аккумуляторов, и предотвращения перезарядки. Неиспользование этих зарядных устройств может привести к тому, что аккумулятор разрядится на годы раньше срока.
Выбирайте гелевые аккумуляторы для хранения солнечной энергии, если вы живете в жарком климате и не можете хранить аккумуляторы в прохладном или хорошо проветриваемом месте, а также если вы можете абсолютно на 100 % гарантировать, что они никогда не будут заряжаться при напряжении, превышающем допустимое. конкретный диапазон .
Лучше ли свинцово-кислотные батареи, чем ионно-литиевые?
Короткий ответ на этот вопрос: нет, свинцово-кислотные батареи не лучше литий-ионных.
Однако стоит отметить, что ионно-литиевые батареи представляют собой более новую технологию аккумуляторов, которая имеет определенные преимущества по сравнению со свинцово-кислотными, в том числе:
- Большая плотность энергии (больше энергии в меньшем объеме)
- Повышенная устойчивость к изменениям температуры
- Способность регулярно разряжаться до 80% и сохраняться в течение 10 лет
Например, литий-ионный аккумулятор, такой как Tesla Powerwall, занимает всего около 4,5 кубических футов, висит на стене, хранит 13,5 кВтч полезной энергии и имеет гарантию, которая гласит, что он прослужит не менее 10 лет, оставаясь при этом в рабочем состоянии. способен хранить 70% своей первоначальной емкости. При ежедневном разряде до 80% это около 33 000 кВтч.
способен хранить 70% своей первоначальной емкости. При ежедневном разряде до 80% это около 33 000 кВтч.
Принимая во внимание, что аккумуляторная батарея глубокого цикла, состоящая из залитых свинцово-кислотных аккумуляторов, которые могут разряжаться до 10,4 кВтч в день, будет занимать 8,2 кубических фута на полу, требовать регулярного обслуживания и служить в общей сложности около 7 лет, обеспечивая около 28 000 кВтч. .
Свинцово-кислотные батареи дешевле литий-ионных?
Дешёвых аккумуляторов не бывает, но разница в цене между этими двумя видами аккумуляторов, конечно же, есть.
Покупка описанных выше свинцово-кислотных аккумуляторов вместе со всем оборудованием для тестирования и полива обойдется примерно в 7500 долларов США, включая затраты на установку. Покупка Powerwall по текущим ценам (на начало 2022 г.) обойдется в 12 000 долларов с учетом затрат на установку.
Покупка Powerwall по текущим ценам (на начало 2022 г.) обойдется в 12 000 долларов с учетом затрат на установку.
Затраты на хранение энергии имеют право на получение федерального налогового кредита на экологически чистую энергию. Налоговый кредит составляет до 30% от стоимости установки системы. После налоговой льготы описанная выше система свинцово-кислотных аккумуляторов будет стоить 5250 долларов, а Powerwall — 8400 долларов.
Разделив стоимость на ожидаемый срок службы, свинцово-кислотный аккумулятор стоит 750 долларов в год, а Powerwall будет стоить 840 долларов в год, или на 12% больше.
Обзоры свинцово-кислотных аккумуляторов
Для получения дополнительной информации посетите наши страницы о лучших солнечных батареях и свинцово-кислотных аккумуляторах Trojan.
Ключевые выводы
- Свинцово-кислотные батареи для хранения солнечной энергии называются «батареями глубокого цикла».

