Аккумуляторная батарея для тракторов
Категория:
Тракторы
Публикация:
Аккумуляторная батарея для тракторов
Читать далее:
Генераторы и реле-регуляторы
Аккумуляторная батарея для тракторов
Аккумуляторная батарея представляет собой вспомогательный источник электрической энергии, питающий всех потребителей в то время, когда двигатель трактора не работает. Батарея состоит из отдельных аккумуляторов — приборов, обладающих свойством накапливать химическую энергию, которую по мере необходимости можно превращать в электрическую.
Принцип действия. Если в бак (рис. 48, а), заполненный электролитом (водным раствором серной кислоты), поместить две свинцовые пластины, отлитые в виде решетки и заполненные окисью свинца, то в результате взаимодействия этой окиси с серной кислотой на поверхности пластин образуется слой сульфата свинца, а в сосуде останется электролит низкой плотности.
Рекламные предложения на основе ваших интересов:
Дополнительные материалы по теме:
Рис. 48. Аккумуляторная батарея:
а — схема действия; б — устройство; 1 — бак; 2 — положительная пластина; 3—отрицательная пластина; 4 — ареометр; 5 — источник постоянного тока; 6 — потребитель тока; 7 — клемма; 8 — перемычка; 9 — крышка; 10 — сепараторы; 11 — полублок; I — подготовка к зарядке; II — зарядка; III — разрядка.
Чтобы накопить в аккумуляторе химическую энергию, его нужно зарядить. Для этого одну из пластин, например (см. рис. 48, а, II), соединяют с отрицательным полюсом источника постоянного тока, а другую, с положительным полюсом источника тока. В результате электролиза электрическая энергия превращается в химическую. Плотность электролита при этом увеличивается, что можно определить при помощи ареометра.
Если между пластинами заряженного аккумулятора установить потребитель электрического тока (см.
Устройство. Аккумуляторная батарея состоит из бака (см. рис. 48, б), изготовленного из эбонита или какого-либо другого кислотоупорного материала, с внутренними перегородками, образующими отдельные сосуды для аккумуляторов. В батарею входит три или шесть аккумуляторов.
Для того чтобы в аккумуляторе можно было накопить достаточно большое количество химической энергии, т. е. чтобы аккумулятор имел большую емкость, в каждый сосуд помещают не две пластины, а две группы пластин, спаянных в полублоки. Каждый из полублоков содержит четыре, пять или больше положительных пластин и на одну больше отрицательных пластин (пять, шесть и т. д.).
При сборке аккумуляторов пластины разноименных полублоков изолируют одну от другой сепараторами — пластинами, изготовленными из изоляционного материала, например микропористого эбонита (мипор). Сверху каждый аккумулятор закрыт крышкой. Все аккумуляторы, находящиеся в батарее, соединены между собой последовательно свинцовыми перемычками. Крайние аккумуляторы имеют конические выводные клеммы, к которым и присоединяют провода, идущие в электрическую сеть трактора.
Сверху каждый аккумулятор закрыт крышкой. Все аккумуляторы, находящиеся в батарее, соединены между собой последовательно свинцовыми перемычками. Крайние аккумуляторы имеют конические выводные клеммы, к которым и присоединяют провода, идущие в электрическую сеть трактора.
Аккумуляторные батареи выпускаются сухозаряжен-ными и несухозаряженными. Сухозаряженные батареи можно долго хранить на складе и быстро привести в рабочее состояние. При особой необходимости такую батарею можно устанавливать на трактор без подзарядки через 3 ч после заливки электролита при условии, что плотность электролита за это время понизится не более чем на 0,04 г/см3.
Аккумуляторная батарея с «массой» соединяется при помощи специального устройства — включателя (рис. 49, а, б), к которому подводится от батареи отрицательный полюс. Для включения «массы» нужно нажать на шток 3 включателя. При этом контактный диск замкнет контакты и направит ток на «массу».
Чтобы отключить батарею от «массы», нужно нажать на боковую кнопку включателя, тогда шток освободится и под действием пружины 5 поднимется вверх и отключит батарею от «массы» (см. рис. 49, б).
рис. 49, б).
Обозначение. На каждой аккумуляторной батарее дается обозначение, например 6СТ-132 ЭМС ГОСТ 959 18—79. Первая цифра (3 или 6) обозначает число аккумуляторов в батарее, что позволяет судить о напряжении тока в батарее (6 или 12 В). Буквы СТ указывают, что батарея стартерная, т. е. такая, которая способна отдавать очень большие токи (до 1000… 2000 А). Следующее за буквами число (50, 75, 82, 132, 150, 182 и 215) соответствует номинальной емкости батареи (А-ч) при 20-часовом разрядном токе. Последующие буквы обозначают материал блока (Э — эбонит, Т — термопласт) и материал сепаратора (М — мипласт, Р — мипор, С — стекловолокно). В условное обозначение несухозаряженной батареи добавляется буква Н. И наконец в обозначение батарей, подготовленных для работы в тропическом климате, входит буква Т.
Рис. 49. Схема подключения включателя «массы»:
а — включено; б — выключено; 1 — контакты; 2— диск; 3— шток; 4 — кнопка; 5 — пружина.
У некоторых тракторов при включении аккумуляторной батареи на «массу» загорается контрольная лампа, расположенная на щитке контрольных приборов.
Назначение и устройство аккумуляторной батареи на тепловозе ЧМЭ3. — Студопедия
Поделись
Аккумулятортепловоза ЧМЭ3 — представляет собой стальной никелированный сосуд 2, в который помещены полублоки положительных 3 и отрицательных 13 электродов ламельного типа и залит электролит (Рис.122, а).
Каждый электрод состоит из комплекта плоских коробочек (ламелей) 22, собранных в стальной рамке 21. Ламели изготовлены из жести и заполнены активной массой – веществом, участвующим в химических реакциях при заряде (т.е. процессе превращения электрической энергии в химическую) и разряде аккумулятора (обратном процессе).
Для доступа электролита к активной массе ламели имеют большое количество мелких отверстий. При заряженном аккумуляторе активная масса положительных электродов – гидрат окиси никеля Ni(ОН)3, а отрицательных – губчатый кадмий (Cd) с примесью губчатого железа (Fe). Электролитом служит 20%-ный раствор едкого калия (КОН) в дистиллированной воде. Для увеличения срока службы электролита в него добавляют едкий литий.
Электролитом служит 20%-ный раствор едкого калия (КОН) в дистиллированной воде. Для увеличения срока службы электролита в него добавляют едкий литий.
Электроды одной полярности собирают в общий полублок посредством шпильки 17 (М10), проходящей через отверстия в верхней части рамок и закрепленной двумя гайками 16. Полублоки собраны соответственно из 17-ти положительных и 16-ти отрицательных электродов (пластин), т.е. каждый отрицательный электрод расположен между двумя положительными. Две крайние положительные пластины соприкасаются с корпусом, а все отрицательные пластины отделены от него пластмассовыми боковыми изоляторами 20. Для фиксации расстояния между электродами одного полублока на шпильку надевают стальные дистанционные кольца 18. Разноименные электроды разделены сепараторами 23 в виде эбонитовых стержней (палочек), не допускающих короткого замыкания внутри аккумулятора.
Рис. 122. Аккумуляторная батарея типа NКS150:
а) – аккумулятор и его части;
1 – выступ; 2 – сосуд; 3, 13 – полублоки положительных и отрицательных электродов;
4 – борн; 5 – крышка; 6 – горловина; 7 – колпачок; 8 – пластины; 9, 14, 16 – гайки;
10, 15 – шайбы; 11 – пластмассовое кольцо; 12 – резиновая втулка; 17 – шпилька; 18 – дистанционное кольцо; 19 – перемычка; 20 – боковой изолятор; 21 – рамка; 22 – ламель;
23 – сепаратор;
Сверху к сосуду приварена стальная штампованная крышка 5, через отверстия в которой выведены токопроводящие штыри (борны) 4, надетые на шпильки 17. Для заливки электролита в крышке имеется горловина 6, закрытая стальным колпачком 7, снабженным пластинчатой пружиной. Борны уплотняют в крышке резиновыми втулками 12, на которые сверху надевают пластмассовые кольца
Для заливки электролита в крышке имеется горловина 6, закрытая стальным колпачком 7, снабженным пластинчатой пружиной. Борны уплотняют в крышке резиновыми втулками 12, на которые сверху надевают пластмассовые кольца
Рис. 122. Аккумуляторная батарея типа NКS150:
б) – ящик секций батареи и подвеска аккумулятора;
в) – схема соединения аккумуляторов;
1 – выступ; 2 – сосуд; 24 – скоба; 25 – торцовая стенка; 26 – пластины; 27 – рым-болт;
28, 30 – боковая и нижняя доски; 29 – поперечная перегородка; 31 – пластмассовая втулка.
Ящик (Рис.122, б) собран из двух торцовых стенок 25, четырех боковых досок 28, поперечной перегородки 29 и двух нижних досок 30, усиленных прикрепленными к ним стальными скобами 24. На торцовых стенках укреплены винтами пластины 26 с приваренными к ним выступами. В резьбовые отверстия выступов ввернуты рым-болты 27, служащие для транспортировки секции.
Боковые доски 28 имеют по 10 глухих отверстий, в которые вставлены пластмассовые втулки 31. При сборке секции ящик устанавливают на специальном стенде в наклонном положении, снимают с одной стороны боковые доски и ставят каждый аккумулятор так, чтобы выступы сосуда вошли в пластмассовые втулки 31. После крепления снятых боковых досок и возвращения секции в вертикальное положение все аккумуляторы будут подвешены в ящике, не касаясь его дна.
Все 15 секций батареи установлены в задней части капота на двух сварных стеллажах, расположенных в разных уровнях.
по 40-ой (внизу), с левой стороны – с 41-го по 60-ый (внизу) и с 61-го по 75-ый (вверху). Аккумуляторы соединены между собой медными пластинами 8, покрытыми слоем свинца, а секции – гибкими многожильными перемычками 19. Все межэлементные и межсекционные соединения батареи закреплены на борнах гайками 14, под которые поставлены стальные шайбы 15.
«Плюс» и «минус» батареи (Рис.122, в) соединены кабелями 21 и 23 с плюсовым и минусовым зажимами рубильника ОБА.
— от «плюса» 21-го аккумулятора через провод Р1 напряжение 75В подведено к цепям поездной радиостанции;
— от «плюса» 41-го аккумулятора через провод А58 – напряжение 50В подведено к цепям АЛСН;
— от «плюса» 61-го аккумулятора через провод 45, средний нож рубильника ОБА, провод 29, плавкий предохранитель П300 на 6А, провод 309, замыкающие контакты КУ1 и провод 300 – напряжение 24 В подведено к цепям пожарной сигнализации.
На тепловозах ЧМЭЗ до №923 к проводу 300 подключены также электротермометры и электроманометры, установленные на пульте управления.
Глава 43 Аккумуляторная батарея (АКБ). Назначение, устройство и типы
10.2.1 Назначение аккумуляторной батареиАккумуляторная батарея обеспечивает электрическим током все потребители, пока двигатель не работает или работает на очень малых оборотах, также является резервным источником питания в случае выхода из строя генератора.
Внимание
В случае выхода из строя генератора не стоит затягивать с его ремонтом, необходимо сразу решать возникшую проблему. Длительное использование исключительно АКБ может вывести ее из строя, причем в самый неподходящий момент.
Одним из основных функциональных назначений АКБ является пуск двигателя с помощью стартера.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.
 2.2 Устройство аккумуляторной батареи
2.2 Устройство аккумуляторной батареиВ аккумуляторной батарее происходит преобразование химической энергии в электрическую. Химия в том, что взяли и поместили в раствор серной кислоты две пластины, состоящие из свинца, и на пластинах сделали выводы (рисунок 10.1). Подсоединили к выводам два провода от генератора, начали вращать его, чтобы тот выделял электрический ток и зарядили АКБ (пока аккумулятор заряжается, он является потребителем тока). В данном случае электрическая энергия преобразовалась в химическую – аккумулятор зарядился. Отсоединили от выводов генератор и подсоединили, например, лампочку, и она загорелась! Потому что начался процесс преобразования химической энергии в электрическую. Прелесть данной конструкции в том, что процессы зарядки и разрядки можно производить многократно. И если соблюдать основные, довольно несложные, правила эксплуатации АКБ, она может прослужить долгое время.
Простейший аккумулятор состоит из двух пластин, помещенных в корпус (его еще называют банкой), этот корпус заполнен раствором серной кислоты (который называется электролитом) и закрыт сверху крышкой. В крышке имеются отверстия, через которые выведены по два вывода от каждой из пластин (положительный и отрицательный).
В крышке имеются отверстия, через которые выведены по два вывода от каждой из пластин (положительный и отрицательный).
Рисунок 10.1 Принцип работы аккумуляторной батареи.
Любая АКБ состоит из нескольких (чаще шести) простейших батарей, описанных выше. Почему именно шести? Бортовая сеть автомобиля рассчитана на 12 вольт, а значит и аккумуляторная батарея должна выдавать столько же. Ввиду своих габаритных размеров одна банка (две пластины) обеспечивает напряжение приблизительно в 2 вольта. Для получения 12 вольт положительные и отрицательные пластины соединяют последовательно и делают два общих вывода – положительный и отрицательный (смотрите рисунок 10.2).
Примечание
Аккумуляторная батарея должна иметь такие габаритные размеры, чтобы оптимально вписаться в ограниченное пространство моторного отсека автомобиля.
Рисунок 10.2 Устройство аккумуляторной батареи.
На многих современных автомобилях для предотвращения кражи головного модуля аудиосистемы существует своеобразная защита, которая блокирует аудиомагнитолу после отключения отрицательной клеммы от аккумуляторной батареи. Чтобы магнитола заработала, в нее необходимо ввести определенный код – ключ. Если вы приобретаете новый автомобиль, данный код вам вручат в салоне, если покупаете машину с рук, необходимо уточнить у владельца наличие такого кода.
Чтобы магнитола заработала, в нее необходимо ввести определенный код – ключ. Если вы приобретаете новый автомобиль, данный код вам вручат в салоне, если покупаете машину с рук, необходимо уточнить у владельца наличие такого кода.
Примечание
Стоит помнить, что в некоторых современных автомобилях после отключения АКБ и повторного подключения бортовой компьютер может вывести сообщение об ошибке, которое можно сбросить с помощью специализированного оборудования на СТО.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.2.3 Типы АКБ
По принципу необходимости обслуживания аккумуляторные батареи разделяют на: обслуживаемые и необслуживаемые. Одним из подтипов обслуживаемых стали малообслуживаемые АКБ. На данный момент применение обслуживаемых АКБ сведено к минимуму. Названия типов аккумуляторных батарей говорят сами за себя.
Основа свинцово-кислотных АКБ, о которых идет речь в данной главе, — жидкий электролит. Однако технологии производства батарей шагнули далеко вперед и сейчас довольно часто можно встретить АКБ, выполненные на базе технологии AGM, в которой сам электролит абсорбирован в стеклянных волокнах. Также не стоит забывать и о набирающих популярность гелевых АКБ (GEL), в них электролит загущен с помощью силикагеля до гелеобразного состояния.
Из-за большого многообразия типов АКБ возникло много споров относительно эффективности и стойкости каждого из них. Если по существу, то нет одного, идеального для всех эксплуатационных условий аккумулятора. Ибо, выигрывая в чем-то одном, любой тип АКБ обязательно существенно проигрывает в чем-нибудь другом. Так, например, столь популярные необслуживаемые «кальциевые» аккумуляторы имеют очень низкие показатели саморазряда и не требуют к себе какого-либо внимания, однако они очень сильно «боятся» глубоких разрядов (как пример, при многократных коротких поездках в зимний период). С такими разрядами АКБ такого типа придет в непригодность за очень короткий период эксплуатации. А вот малообслуживаемые АКБ глубоких разрядов не боятся, но взамен требуют регулярной доливки дистиллированной воды (в среднем, раз в полгода).
С такими разрядами АКБ такого типа придет в непригодность за очень короткий период эксплуатации. А вот малообслуживаемые АКБ глубоких разрядов не боятся, но взамен требуют регулярной доливки дистиллированной воды (в среднем, раз в полгода).
Примечание
Во время зарядки АКБ происходит закипание электролита, но закипание не в бытовом понимании этого слова, просто происходит расщепление воды на кислород и водород (появляются пузырьки). Составная часть электролита – вода – выкипает, а плотность электролита, соответственно, растет. Чтобы привести плотность электролита в норму, доливают дистиллированную воду.
Внимание
Одной из существенных опасностей при плановой зарядке АКБ является выделение водорода из электролита. И вроде мало, но и взорваться может. Поэтому при обслуживании и эксплуатации АКБ необходимо соблюдать все меры предосторожности.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.
 2.3.a Полярность АКБ
2.3.a Полярность АКБПолярность указывает на расположение отрицательного и положительного выводов батареи. Полярность бывает прямой и обратной.
Примечание
Чтобы узнать, какая полярность на вашей АКБ, установите ее к себе той стороной, ближе к которой смещены выводы. Посмотрите, какой из выводов обозначен знаком «+», а какой — знаком «-». Если «+» находится слева, значит полярность прямая, если справа – обратная.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.2.3.b Номинальная емкость
Номинальная емкость (обозначается С20) — количество электричества (в А·ч), которое способна отдать АКБ при 20-часовом режиме разряда током, численно равным 0,05 номинальной емкости до напряжения на выводах 10,5 В при температуре электролита 25 °С.
Внимание
Следует всегда помнить о том, что на автомобиль следует устанавливать АКБ той емкости, которая указана заводом-изготовителем транспортного средства.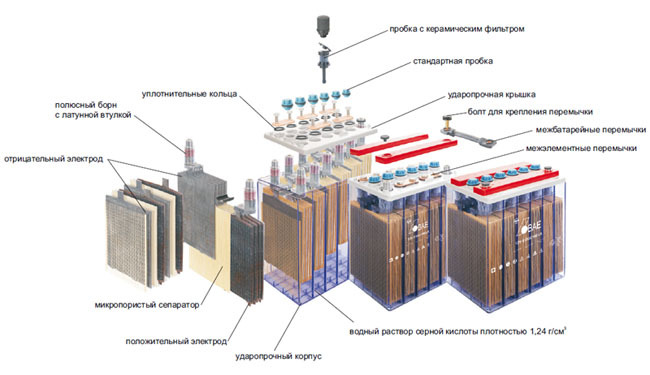 В принципе, ничего страшного не случится, и первое время будет радовать резвый пуск двигателя, но не стоит забывать о том, что возможности генератора не безграничны, а условия эксплуатации автомобиля могут быть очень суровы. Как следствие, батарея большей емкости будет постоянно недополучать энергию для восстановления — не будет заряжаться на 100%, что в скором времени приведет к выходу ее из строя.
В принципе, ничего страшного не случится, и первое время будет радовать резвый пуск двигателя, но не стоит забывать о том, что возможности генератора не безграничны, а условия эксплуатации автомобиля могут быть очень суровы. Как следствие, батарея большей емкости будет постоянно недополучать энергию для восстановления — не будет заряжаться на 100%, что в скором времени приведет к выходу ее из строя.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.2.3.c Резервная емкость
Резервная емкость (обозначается Cр) – время разряда в минутах полностью заряженной батареи током 25 А до напряжения 10,5 В при температуре электролита 25 °С.
Примечание
Резервная емкость в 1,63 раза больше номинальной в числовом выражении (так, для АКБ емкостью 55 А·ч она составляет приблизительно 90 минут). Это время, в течение которого полностью заряженная батарея может обеспечивать электроэнергией минимальное количество потребителей, необходимых для безопасного движения автомобиля в случае отказа генератора.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.2.3.d Ток холодной прокрутки
Ток холодной прокрутки (Iх.п.) – по ГОСТу (ДСТУ) 959-2002 – это ток разряда, который способна отдать батарея при температуре электролита минус 18 °С в течение 10 секунд при напряжении не менее 7,5 В. Чем выше данный параметр, тем лучше двигатель будет пускаться зимой, однако по причине увеличения нагрузки на стартер может снизиться его ресурс.
Примечание
Величина тока холодной прокрутки зависит от методики ее измерения. Примерное соответствие значений тока холодной прокрутки, определенного по разным стандартам, приведено в таблице ниже.
| DIN 43559, ГОСТ 959-91 | 170 | 200 | 225 | 255 | 280 | 310 | 335 | 365 | 395 | 420 |
| EN 60095-1, ГОСТ 959-2002 (Россия) | 280 | 330 | 360 | 420 | 480 | 520 | 540 | 600 | 640 | 680 |
| SAE J537 | 300 | 350 | 400 | 450 | 500 | 550 | 600 | 650 | 700 | 750 |
Комментарии пользователей (0)
Задать вопрос преподавателю
10.
 2.3.e Плотность электролита АКБ
2.3.e Плотность электролита АКБОдним из основных показателей, характеризующих рабочее состояние АКБ, является плотность электролита. Она должна быть всегда в определенном диапазоне. Если АКБ малообслуживаемая, то летом плотность немного понижают, а вот зимой, чтобы исключить вероятность замерзания электролита, повышают.
Примечание
Плотность электролита измеряется специальным прибором – ареометром.
Комментарии пользователей (0)
Задать вопрос преподавателю
10.2.4 При покупке АКБ
Допустим, вы решили заменить источник питания. Придя, например, в магазин автозапчастей, определились с моделью. Теперь внимательнее. Спросите сначала АКБ сухозаряженный (без электролита) или залитый электролитом и заряженный. В первом случае срок хранения на складе не должен превышать трех лет, во втором – полугода.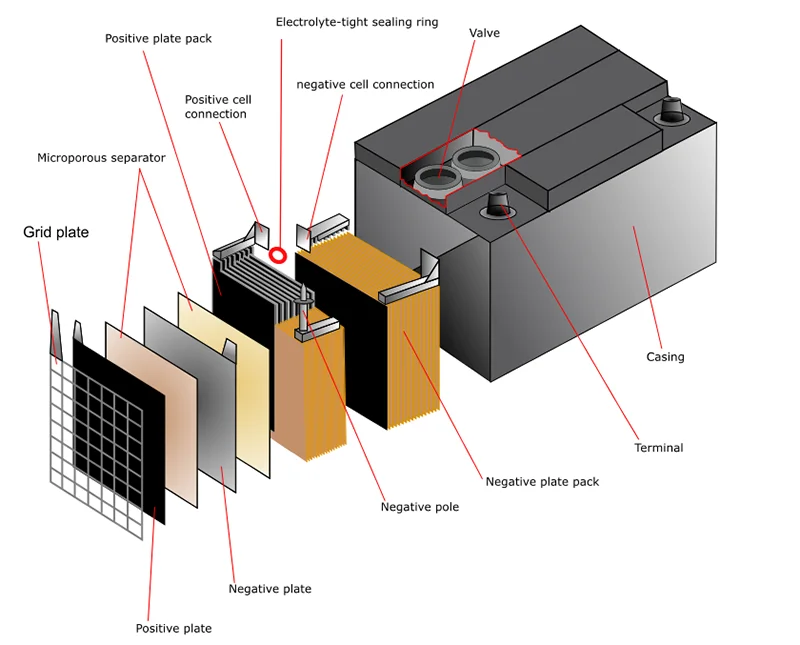
Посмотрите на дату изготовления АКБ и если с даты производства прошло более одного года, выполните, по возможности, следующие проверки:
- осмотрите корпус на наличие повреждений;
Для залитых и заряженных
- уровень электролита должен находиться между метками «min» и «max» (корпус из полупрозрачного пластика) или быть выше примерно на 15 – 20 мм от верхнего торца пластин;
- плотность электролита должна составлять 1,25–1,26 г/см3 при 25±5 °С;
Маркировка АКБ
Рисунок 10.3 Маркировка АКБ по отечественному стандарту.
Рисунок 10.4 Маркировка АКБ по европейскому стандарту EN 60095-1.
Рисунок 10.5 Маркировка АКБ по американскому стандарту SAE J537.
Для всех
- цвет индикатора заряженности (если такой есть в наличии) должен быть зеленым;
- напряжение на выводах без нагрузки должно быть не менее 12,6 В.
Внимание
Так или иначе, но в наличии должна быть инструкция по эксплуатации на русском или украинском языке и гарантийный талон с указанными условиями гарантии.
Не стесняйтесь требовать от продавца выполнения описанных выше проверок, ведь автомобильная АКБ это не батарейка в плеер, и приобретается не на один месяц, причем от качества АКБ зависит работа всех электрических систем автомобиля.
Комментарии пользователей (0)
Задать вопрос преподавателю
История и развитие аккумуляторов
Хосе Аларко и Питер Талбот, Разговор
Батареи прошли долгий путь с момента их появления в 250 г. до н.э. Предоставлено: Flickr/Patty, CC BY-NC-SA.Батарейки настолько распространены сегодня, что почти невидимы для нас. Тем не менее, это замечательное изобретение с долгой и легендарной историей и столь же захватывающим будущим.
Батарея — это устройство, в котором хранится химическая энергия, преобразуемая в электричество. По сути, батареи представляют собой небольшие химические реакторы, в ходе реакции которых образуются энергичные электроны, готовые пройти через внешнее устройство.
По сути, батареи представляют собой небольшие химические реакторы, в ходе реакции которых образуются энергичные электроны, готовые пройти через внешнее устройство.
Батарейки давно с нами. В 1938 году директор Багдадского музея обнаружил в подвале музея то, что сейчас называют «Багдадской батареей». Анализ датировал его примерно 250 г. до н.э. и месопотамского происхождения.
Этот самый ранний пример батареи вызывает споры, но предлагаемые варианты использования включают гальваническое покрытие, обезболивание или религиозное покалывание.
Американский ученый и изобретатель Бенджамин Франклин впервые употребил термин «батарея» в 1749 году, когда проводил эксперименты с электричеством, используя набор связанных конденсаторов.
Первая настоящая батарея была изобретена итальянским физиком Алессандро Вольта в 1800 году. Вольта сложил диски из меди (Cu) и цинка (Zn), разделенные тканью, смоченной в соленой воде.
Провода, подключенные к любому концу стека, производили непрерывный стабильный ток. Каждая ячейка (набор медных и цинковых дисков и рассол) производит 0,76 Вольт (В). Полученное значение, кратное этому значению, определяется количеством ячеек, сложенных вместе.
Каждая ячейка (набор медных и цинковых дисков и рассол) производит 0,76 Вольт (В). Полученное значение, кратное этому значению, определяется количеством ячеек, сложенных вместе.
Один из самых долговечных аккумуляторов, свинцово-кислотный аккумулятор, был изобретен в 1859 году и до сих пор используется для запуска большинства автомобилей с двигателями внутреннего сгорания. Это самый старый пример перезаряжаемой батареи.
Сегодня батареи бывают самых разных размеров: от больших мегаваттных, которые хранят энергию от солнечных ферм или подстанций, чтобы гарантировать стабильное снабжение целых деревень или островов, до крошечных батарей, таких как те, которые используются в электронных часах.
Аккумуляторы основаны на различных химических веществах, которые генерируют базовое напряжение элемента, как правило, в диапазоне от 1,0 до 3,6 В. Последовательное расположение элементов увеличивает напряжение, а их параллельное соединение увеличивает подачу тока. Этот принцип используется для суммирования требуемых напряжений и токов вплоть до мегаваттных размеров.
В настоящее время многие ожидают, что аккумуляторная технология сделает еще один скачок: разрабатываются новые модели с достаточной емкостью для хранения энергии, вырабатываемой бытовыми солнечными или ветровыми системами, а затем для питания дома в более удобное (обычно ночное) время для несколько дней
Как работают батареи?
Когда аккумулятор разряжается, в ходе химической реакции образуются дополнительные электроны. Примером реакции, в результате которой образуются электроны, является окисление железа с образованием ржавчины. Железо реагирует с кислородом и отдает электроны кислороду с образованием оксида железа.
Стандартная конструкция батареи состоит из двух металлов или соединений с разным химическим потенциалом, разделенных пористым изолятором. Химический потенциал — это энергия, запасенная в атомах и связях соединений, которая затем передается движущимся электронам, когда им позволяют двигаться через подключенное внешнее устройство.
Проводящая жидкость, такая как соль и вода, используется для переноса растворимых ионов от одного металла к другому во время реакции и называется электролитом.
Металл или соединение, которое теряет электроны во время разряда, называется анодом, а металл или соединение, которое принимает электроны, называется катодом. Этот поток электронов от анода к катоду через внешнее соединение — это то, что мы используем для работы наших электронных устройств.
Первичные и перезаряжаемые батареи
Если реакцию, вызывающую поток электронов, нельзя обратить вспять, батарея называется первичной. Когда один из реагентов расходуется, батарея разряжается.
Наиболее распространенной первичной батареей является углеродно-цинковая батарея. Было обнаружено, что когда электролит представляет собой щелочь, батареи служат намного дольше. Это щелочные батареи, которые мы покупаем в супермаркете.
Проблема утилизации таких первичных батарей заключалась в том, чтобы найти способ их повторного использования путем перезарядки батарей. Это становится все более важным по мере того, как батареи становятся больше, а их частая замена становится коммерчески невыгодной.
Один из первых аккумуляторов, никель-кадмиевый аккумулятор (NiCd), также использует щелочь в качестве электролита. В 19Было разработано 89 никель-металловодородных аккумуляторов (NiMH), которые имели более длительный срок службы, чем никель-кадмиевые аккумуляторы.
Аккумуляторы этого типа очень чувствительны к перезарядке и перегреву во время зарядки, поэтому скорость заряда контролируется ниже максимальной скорости. Сложные контроллеры могут ускорить заряд, не занимая менее нескольких часов.
В большинстве других более простых зарядных устройств процесс обычно занимает ночь.
Портативные устройства, такие как мобильные телефоны и портативные компьютеры, постоянно нуждаются в максимальной и наиболее компактной хранимой энергии. Хотя это увеличивает риск резкого разряда, этим можно управлять с помощью ограничителей скорости тока в батареях мобильных телефонов из-за общего небольшого размера.
Но по мере того, как предполагается более широкое применение батарей, безопасность большого формата и большого количества элементов становится все более важным фактором.
Первый большой шаг вперед: литий-ионные аккумуляторы
Новые технологии часто требуют более компактных, более емких, безопасных перезаряжаемых аккумуляторов.
В 1980 году американский физик профессор Джон Гуденаф изобрел новый тип литиевой батареи, в которой литий (Li) мог мигрировать через батарею от одного электрода к другому в виде иона Li+.
Литий является одним из самых легких элементов в таблице Менделеева и имеет один из самых высоких электрохимических потенциалов, поэтому эта комбинация создает одни из самых высоких возможных напряжений в самых компактных и легких объемах.
Это основа для литий-ионного аккумулятора. В этой новой батарее литий сочетается с переходным металлом, таким как кобальт, никель, марганец или железо, и кислородом, образуя катод. Во время перезарядки при приложении напряжения положительно заряженный ион лития с катода мигрирует к графитовому аноду и становится металлическим литием.
Поскольку литий обладает сильной электрохимической движущей силой, которая может окисляться, если ему это позволяют, он мигрирует обратно к катоду, снова становясь ионом Li+, и отдает свой электрон обратно иону кобальта. Движение электронов в цепи дает нам ток, который мы можем использовать.
Движение электронов в цепи дает нам ток, который мы можем использовать.
Второй большой скачок вперед: нанотехнологии
В зависимости от переходного металла, используемого в литий-ионном аккумуляторе, элемент может иметь более высокую емкость, но может быть более реактивным и восприимчивым к явлению, известному как тепловой разгон.
В случае с батареями из оксида лития-кобальта (LiCoO 2 ), произведенными Sony в 1990-х годах, это привело к возгоранию многих таких батарей. О возможности изготовления аккумуляторных катодов из наноразмерного материала и, следовательно, о большей реакционной способности не могло быть и речи.
Но в 1990-х годах Гуденаф снова совершил огромный скачок в технологии аккумуляторов, представив стабильный литий-ионный катод на основе литиевого железа и фосфата.
Катод термически стабилен. Это также означает, что наноразмерный фосфат лития-железа (LiFePO 4 ) или феррофосфат лития (LFP) теперь можно безопасно превращать в элементы большого формата, которые можно быстро заряжать и разряжать.
В настоящее время для этих новых элементов существует множество новых применений, от электроинструментов до гибридных и электрических транспортных средств. Пожалуй, самым важным применением станет хранение бытовой электроэнергии для домашних хозяйств.
У первого мобильного телефона была большая батарея и короткое время автономной работы — современные мобильные телефоны и смартфоны требуют меньших батарей, но более продолжительной работы.Электромобили
Лидером в производстве аккумуляторов нового формата для транспортных средств является компания по производству электромобилей Tesla, у которой есть планы по строительству «гига-заводов» для производства этих аккумуляторов.
Размер блока литиевых батарей для Tesla Model S составляет впечатляющие 85 кВтч.
Этого также более чем достаточно для бытовых нужд, поэтому было так много слухов о том, что основатель Tesla Илон Маск готовится раскрыть на этой неделе.
Модульная конструкция аккумуляторной батареи может создавать форматы аккумуляторных батарей, которые в некоторой степени взаимозаменяемы и подходят как для транспортных средств, так и для бытового применения без необходимости перепроектирования или реконструкции.
Возможно, мы станем свидетелями смены поколений в производстве и хранении энергии благодаря постоянно совершенствующимся возможностям скромной батареи.
Узнать больше
Помимо ионно-литиевых батарей — важный шаг к более эффективной батарее
Источник: Разговор
Эта история опубликована с разрешения The Conversation (под Creative Commons-Attribution/Без производных).
Цитата :
История и развитие аккумуляторов (2015, 30 апреля)
получено 5 октября 2022 г. с https://phys.org/news/2015-04-history-batteries.html
с https://phys.org/news/2015-04-history-batteries.html
Этот документ защищен авторским правом. Помимо любой добросовестной сделки с целью частного изучения или исследования, никакие часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в ознакомительных целях.
Заряженный вопрос: как работают аккумуляторы телефонов и почему некоторые взрываются | Смартфоны
Срок службы батареи — это взрывоопасная проблема. Буквально, как Samsung обнаруживает к своему ужасу. Смартфон Galaxy Note 7 компании после выпуска получил высокую оценку за лучшее в своем классе время автономной работы, намного опережая своего основного конкурента, iPhone 6S и 7 Plus. Затем он начал взрываться. Samsung выпустила программу отзыва и замены, и количество замен также начало резко увеличиваться, что вынудило компанию полностью приостановить производство.
Это дело знаменует собой последнее препятствие в долгой борьбе за улучшение батарей, питающих нашу электронику.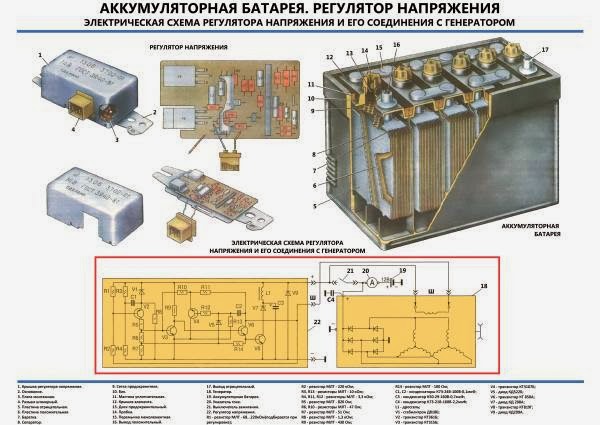 В то время как скорость обработки данных удваивается примерно каждые 18 месяцев, для увеличения емкости батареи требуется почти десятилетие. Этот пробел начинает вызывать проблемы, но, как показала компания Samsung, его нелегко исправить.
В то время как скорость обработки данных удваивается примерно каждые 18 месяцев, для увеличения емкости батареи требуется почти десятилетие. Этот пробел начинает вызывать проблемы, но, как показала компания Samsung, его нелегко исправить.
Смартфон часто работает меньше суток, ноутбук иногда всего несколько часов, а электромобиль с трудом проезжает 350 миль. Так почему же время автономной работы до сих пор является такой проблемой — и когда мы собираемся это исправить?
Что такое батарея?
Внутри этого пластикового и металлического корпуса находится небольшая коробочка с химическими веществами, готовыми к реакции и созданию электричества. Фотография: BitchBuzz/FlickrБатарейки — это небольшие контейнеры с химической энергией. Когда смартфон подключен к сети, электричество используется для сброса химической реакции внутри батареи, перенося электроны с отрицательного анода на катод — положительный конец батареи.
После зарядки батарея может вырабатывать электричество, направляя электроны через цепь, в данном случае через смартфон, к аноду, и будет продолжать это делать до тех пор, пока все электроны, содержащиеся в батарее, не перейдут на анод или встроенную -in выключатель отключает аккумулятор.
Из чего сделан аккумулятор?
Внутри типичной батареи у вас есть анод, катод и электролит — то, через что проходят положительные ионы.
Литий-ионные аккумуляторы, используемые в большинстве смартфонов и электронных устройств, имеют катод из оксида металла, изготовленный из смеси кобальта, никеля, марганца или железа, пористый графитовый анод, удерживающий внутри себя ионы лития, и электролит на основе соли лития.
Положительно заряженные ионы лития проходят через электролит от анода к катоду, направляя электроны через смартфон по мере необходимости обратно к аноду.
Почему этого недостаточно?
Символ низкого заряда батареи на Nokia Lumia 800 в кармане джинсов. Фотография: Мартин Абегглен/FlickrПринцип работы батареи может быть простым, но химия и технология, обеспечивающие ее работу, не являются таковыми. Основным ограничивающим фактором для батарей является их плотность энергии.
Аккумулятор может генерировать столько электричества, сколько его химические компоненты могут хранить энергию.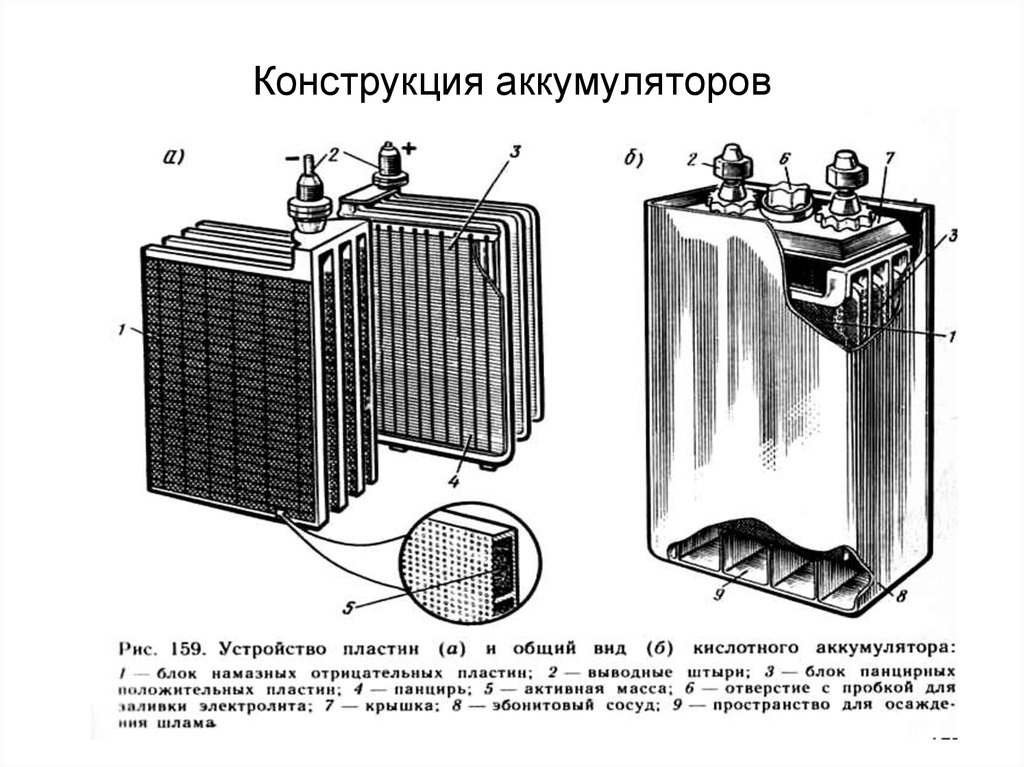 Все, что не является активным материалом внутри батареи, фактически является мертвым грузом, включая корпус, микросхемы контроллера, провода для отвода тока — все они добавляют вес, но не мощность.
Все, что не является активным материалом внутри батареи, фактически является мертвым грузом, включая корпус, микросхемы контроллера, провода для отвода тока — все они добавляют вес, но не мощность.
Типичная литий-ионная батарея в смартфоне имеет плотность энергии около 150 ватт-часов на килограмм (Втч/кг). Хотя плотность энергии литий-ионных аккумуляторов улучшилась с момента их появления в начале 1990-х годов, это сдерживается их конструкцией и химическим составом.
Единственный способ немедленно увеличить срок службы батареи смартфона с помощью современных технологий — это повысить энергоэффективность электронных компонентов смартфона и увеличить размер батареи, но все тоньше и тоньше смартфоны требуют все более тонких аккумуляторов.
Почему срок службы батареи уменьшается?
Полностью заряжен или нет? Со временем аккумулятор не может хранить столько энергии, сколько был новым. Фотография: Bastian Greshake/Flickr Срок службы батареи не остается постоянным на протяжении всего срока службы смартфона — он медленно уменьшается с течением времени по мере разрядки и перезарядки батареи.
Это связано с тем, что химическая реакция, в результате которой вырабатывается электричество, вызывает отложение тонких слоев лития на электродах, что снижает количество доступного для выработки электричества и увеличивает внутреннее сопротивление батареи.
Чем выше сопротивление, тем тяжелее батарея должна работать, чтобы поддерживать полезное напряжение, и поэтому количество энергии, которое она может производить за один заряд, уменьшается. Возможно, вы помните этот фрагмент из школы:
Напряжение = Ток x Сопротивление (V=IR)
Почему некоторые батареи взрываются?
Аккумулятор вырывается из корпуса аккумулятора 17-дюймового MacBook Pro из-за вздутия. Фотография: J Aaron Farr/FlickrБатареи с гораздо более высокой плотностью энергии, чем элементы на основе лития, уже доступны, но они недостаточно безопасны для использования в портативной электронике.
«Чем больше энергии вы вложите в коробку, тем опаснее она будет», — говорит доктор Билли Ву, преподаватель Школы проектирования Дайсона Имперского колледжа Лондона. «Безопасность является абсолютно ключевым фактором, а управление температурным режимом имеет решающее значение. Если батарея нагревается выше 80°C, вы сталкиваетесь с так называемым тепловым разгоном, когда компоненты начинают разлагаться, и тогда она может взорваться».
«Безопасность является абсолютно ключевым фактором, а управление температурным режимом имеет решающее значение. Если батарея нагревается выше 80°C, вы сталкиваетесь с так называемым тепловым разгоном, когда компоненты начинают разлагаться, и тогда она может взорваться».
Конкретная причина проблем Samsung со взрывающимися батареями неизвестна, компания просто ссылается на «проблему с аккумулятором».
Что дальше?
На данный момент мы застряли с перезаряжаемой литий-ионной батареей. Фотография: Razor512/FlickrВ ближайшее время прогресс в области аккумуляторов будет достигнут за счет приближения существующих литий-ионных технологий к их теоретическим пределам, что повысит удельную мощность аккумуляторов.
Типичная литий-ионная батарея, в которой используется оксид лития-марганца, имеет теоретическую плотность мощности 280 Втч/кг, но конечный продукт имеет только 150 Втч/кг, поэтому, безусловно, есть возможности для улучшения.
«Речь идет об оптимизации структуры батареи, — говорит Ву. «Если представить, что внутри вашей батареи есть пористая структура, заполненная активным материалом».
«Если представить, что внутри вашей батареи есть пористая структура, заполненная активным материалом».
«Для более высокой выходной мощности вам нужна более пористая структура, чтобы увеличить площадь поверхности и пропускать больше ионов лития в любой момент времени, но поскольку в ней больше отверстий, она удерживает меньше активного материала, что, в свою очередь, снижает емкость. ”
Новые передовые химические составы аккумуляторов, такие как литий-сера и литий-кремний, также находятся в стадии разработки, и компании Великобритании в настоящее время разрабатывают эту технологию.
Каково будущее технологии аккумуляторов?
Комбинированное фото показывает, как Samsung Note 7 взрывается, когда к его полностью заряженному аккумулятору оказывается давление во время испытаний в аккумуляторной лаборатории Applied Energy Hub в Сингапуре, 6 октября. Фотография: Edgar Su/Reuters Твердотельные батареи — это одно из возможных будущих, когда жидкий электролит в батарее заменен твердым веществом, что обеспечит значительное повышение безопасности.
«Основное преимущество твердотельных аккумуляторов заключается в том, что вы можете вернуться к использованию лития в качестве материала анода, который имеет действительно хорошую мощность и плотность энергии, но небезопасен с жидкими электролитами», — объясняет Ву.
Твердотельные батареи устранят необходимость в пористом угольном аноде и, следовательно, уменьшат вес батареи, который не способствует выработке энергии.
Воздушно-металлические батареи, использующие цинк, литий или алюминий, также находятся на горизонте, но, по словам Ву, до коммерческого применения осталось 20 лет.
Что я могу сделать, чтобы моя батарея работала дольше?
Знакомое зрелище для всех, у кого есть смартфон, планшет или компьютер. Фотография: Сэмюэл Гиббс/The Guardian Есть несколько вещей, которые вы можете сделать, чтобы продлить срок службы батареи. Природа химической реакции внутри батареи означает, что она должна работать интенсивнее на последних 20% разряда и выше 80% заряда.
Поддержание литий-ионного аккумулятора примерно на уровне от 80% до 20% заряда поможет ему дольше сохранять большую часть своей емкости. В настоящее время разрабатываются интеллектуальные системы управления питанием, которые делают именно это при подключении к стене на ночь.
Батареи нельзя оставлять включенными постоянно, что особенно важно для ноутбуков. Они содержатся в лучшем рабочем состоянии, если их время от времени разряжать и перезаряжать. Раз в месяц надо делать.
- Является ли алюминий ответом на все наши молитвы об аккумуляторе?
- Кризис Samsung Galaxy Note 7 усугубляется сообщениями о приостановке производства
Что такое система управления батареями (BMS)? — Как это работает
Как работают системы управления батареями?
Типы систем управления батареями
Важность систем управления батареями
Преимущества систем управления батареями
Системы управления батареями и Synopsys
Надзор, который обеспечивает BMS, обычно включает:
- Мониторинг батареи
- Обеспечение защиты аккумулятора
- Оценка рабочего состояния батареи
- Непрерывная оптимизация производительности батареи
- Отчет о рабочем состоянии на внешние устройства
Здесь термин «батарея» подразумевает всю упаковку; тем не менее, функции контроля и управления специально применяются к отдельным элементам или группам элементов, называемым модулями, в общей сборке аккумуляторной батареи. Литий-ионные перезаряжаемые элементы имеют самую высокую плотность энергии и являются стандартным выбором для батарей для многих потребительских товаров, от ноутбуков до электромобилей. Несмотря на то, что они превосходно работают, они могут быть довольно неумолимыми, если работают за пределами, как правило, узкой безопасной рабочей зоны (SOA), с последствиями, варьирующимися от снижения производительности батареи до откровенно опасных последствий. BMS, безусловно, имеет сложное описание работы, а ее общая сложность и охват контроля могут охватывать многие дисциплины, такие как электрические, цифровые, контрольные, тепловые и гидравлические.
Литий-ионные перезаряжаемые элементы имеют самую высокую плотность энергии и являются стандартным выбором для батарей для многих потребительских товаров, от ноутбуков до электромобилей. Несмотря на то, что они превосходно работают, они могут быть довольно неумолимыми, если работают за пределами, как правило, узкой безопасной рабочей зоны (SOA), с последствиями, варьирующимися от снижения производительности батареи до откровенно опасных последствий. BMS, безусловно, имеет сложное описание работы, а ее общая сложность и охват контроля могут охватывать многие дисциплины, такие как электрические, цифровые, контрольные, тепловые и гидравлические.
Как работают системы управления батареями?
Типы систем управления батареями
Важность систем управления батареями
Функциональная безопасность имеет первостепенное значение для BMS. Во время операций зарядки и разрядки очень важно не допустить, чтобы напряжение, ток и температура любой ячейки или модуля, находящихся под диспетчерским контролем, превышали определенные пределы SOA. Если ограничения превышаются в течение длительного времени, это может привести не только к повреждению потенциально дорогостоящего аккумуляторного блока, но и к опасным условиям теплового разгона. Кроме того, для защиты литий-ионных элементов и функциональной безопасности также строго контролируются нижние пороговые значения напряжения. Если литий-ионная батарея останется в этом низковольтном состоянии, медные дендриты могут в конечном итоге вырасти на аноде, что может привести к увеличению скорости саморазряда и вызвать возможные проблемы с безопасностью. Высокая плотность энергии систем с литий-ионным питанием достигается ценой, которая оставляет мало места для ошибок при управлении батареями. Благодаря BMS и литий-ионным усовершенствованиям, это один из самых успешных и безопасных химических элементов аккумуляторов, доступных на сегодняшний день.
Во время операций зарядки и разрядки очень важно не допустить, чтобы напряжение, ток и температура любой ячейки или модуля, находящихся под диспетчерским контролем, превышали определенные пределы SOA. Если ограничения превышаются в течение длительного времени, это может привести не только к повреждению потенциально дорогостоящего аккумуляторного блока, но и к опасным условиям теплового разгона. Кроме того, для защиты литий-ионных элементов и функциональной безопасности также строго контролируются нижние пороговые значения напряжения. Если литий-ионная батарея останется в этом низковольтном состоянии, медные дендриты могут в конечном итоге вырасти на аноде, что может привести к увеличению скорости саморазряда и вызвать возможные проблемы с безопасностью. Высокая плотность энергии систем с литий-ионным питанием достигается ценой, которая оставляет мало места для ошибок при управлении батареями. Благодаря BMS и литий-ионным усовершенствованиям, это один из самых успешных и безопасных химических элементов аккумуляторов, доступных на сегодняшний день.
Производительность аккумуляторной батареи — следующая по важности характеристика BMS, и она включает управление электрическими и тепловыми параметрами. Чтобы электрически оптимизировать общую емкость батареи, все элементы в блоке должны быть сбалансированы, что означает, что SOC соседних элементов в сборке примерно эквивалентны. Это исключительно важно, поскольку позволяет не только реализовать оптимальную емкость батареи, но и помогает предотвратить общую деградацию и уменьшает потенциальные точки перегрева из-за перезарядки слабых элементов. Литий-ионные батареи следует избегать разряда ниже нижнего предела напряжения, так как это может привести к эффекту памяти и значительной потере емкости. Электрохимические процессы очень чувствительны к температуре, и аккумуляторы не являются исключением. Когда температура окружающей среды падает, емкость и доступная энергия батареи значительно снижаются. Следовательно, BMS может задействовать внешний встроенный нагреватель, который находится, скажем, в системе жидкостного охлаждения аккумуляторной батареи электромобиля, или включать резидентные пластины нагревателя, которые установлены под модулями батареи, встроенной в вертолет или другое устройство. самолет. Кроме того, поскольку зарядка холодных литий-ионных элементов отрицательно сказывается на сроке службы батареи, важно сначала достаточно поднять температуру батареи. Большинство литий-ионных элементов нельзя быстро зарядить, если они ниже 5°C, и вообще не следует заряжать, если они ниже 0°C. Для оптимальной производительности при типичном рабочем использовании система управления температурным режимом BMS часто обеспечивает работу батареи в узком диапазоне рабочих температур Златовласки (например, 30–35 °C). Это гарантирует производительность, продлевает срок службы и способствует созданию здоровой и надежной аккумуляторной батареи.
самолет. Кроме того, поскольку зарядка холодных литий-ионных элементов отрицательно сказывается на сроке службы батареи, важно сначала достаточно поднять температуру батареи. Большинство литий-ионных элементов нельзя быстро зарядить, если они ниже 5°C, и вообще не следует заряжать, если они ниже 0°C. Для оптимальной производительности при типичном рабочем использовании система управления температурным режимом BMS часто обеспечивает работу батареи в узком диапазоне рабочих температур Златовласки (например, 30–35 °C). Это гарантирует производительность, продлевает срок службы и способствует созданию здоровой и надежной аккумуляторной батареи.
Преимущества систем управления батареями
Вся система накопления энергии на батареях, которую часто называют BESS, может состоять из десятков, сотен или даже тысяч литий-ионных элементов, стратегически упакованных вместе, в зависимости от применения. Эти системы могут иметь номинальное напряжение менее 100 В, но могут достигать 800 В с током питания до 300 А и более. Любое неправильное обращение с высоковольтным блоком может привести к опасной для жизни катастрофе. Следовательно, поэтому BMS абсолютно необходимы для обеспечения безопасной работы. Преимущества BMS можно резюмировать следующим образом.
Любое неправильное обращение с высоковольтным блоком может привести к опасной для жизни катастрофе. Следовательно, поэтому BMS абсолютно необходимы для обеспечения безопасной работы. Преимущества BMS можно резюмировать следующим образом.
- Функциональная безопасность. Несомненно, для литий-ионных аккумуляторов большого формата это особенно разумно и важно. Но известно, что даже меньшие форматы, используемые, скажем, в ноутбуках, загораются и наносят огромный ущерб. Личная безопасность пользователей продуктов, включающих системы с литий-ионным питанием, оставляет мало места для ошибок при управлении батареями.
- Срок службы и надежность. Управление защитой аккумуляторной батареи, электрической и тепловой, гарантирует, что все элементы используются в соответствии с заявленными требованиями SOA. Этот деликатный контроль обеспечивает защиту элементов от агрессивного использования и быстрых циклов зарядки и разрядки и неизбежно приводит к стабильной системе, которая потенциально обеспечит многолетнюю надежную работу.

- Производительность и диапазон. Управление емкостью аккумуляторной батареи BMS, при котором балансировка между ячейками используется для выравнивания SOC соседних ячеек в сборке батареи, позволяет реализовать оптимальную емкость батареи. Без этой функции BMS для учета изменений саморазряда, циклов зарядки/разрядки, температурных эффектов и общего старения аккумуляторная батарея может в конечном итоге стать бесполезной.
- Диагностика, сбор данных и внешняя связь. Задачи наблюдения включают в себя непрерывный мониторинг всех элементов батареи, при этом регистрация данных может использоваться сама по себе для диагностики, но часто предназначена для задачи вычисления для оценки SOC всех элементов в сборке. Эта информация используется для алгоритмов балансировки, но в совокупности может передаваться на внешние устройства и дисплеи для отображения доступной энергии резидента, оценки ожидаемого диапазона или диапазона/срока службы на основе текущего использования и предоставления информации о состоянии аккумуляторной батареи.

