Катализ и катализаторы — Энциклопедия wiki.MPlast.by
Катализ – это процесс изменения скорости химической реакции при помощи катализаторов – веществ, принимающих участие в химической реакции, но в состав конечных продуктов не входящих и в результате реакции не расходующихся.
Одни катализаторы ускоряют реакцию (положительный катализ), другие – замедляют (отрицательный катализ). Отрицательный катализ называют ингибированием, а катализаторы, понижающие скорость химической реакции – ингибиторами.
Различают гомогенный и гетерогенный катализ.
При гомогенном (однородном) катализе реагирующие вещества и катализатор находятся в одинаковом агрегатном состоянии и между ними отсутствует поверхность раздела. Пример гомогенного катализа – реакция окисления SO2 и SO3 в присутствии катализатора NO (реагирующие вещества и катализатор являются газами).
Гетерогенный катализ.
В случае гетерогенного (неоднородного) катализа реагирующие вещества и катализатор находятся в различных агрегатных состояниях и между ними существует поверхность (граница) раздела. Обычно катализатор – твердое вещество, а реагирующие вещества – жидкости или газы. Пример гетерогенного катализа – окисление NN3 до NO в присутствии Pt (катализатор – твердое вещество).
Механизм действия катализаторов
Действие положительных катализаторов сводится к понижению энергии активации реакции Еа(исх), действие ингибиторов – противоположное.
Так, для реакции 2HI = H2+I2 Еа(исх)=184 кДж/моль. Когда же эта реакция протекает в присутствии катализатора Au или Pt, то Еа(исх)=104 кДж/моль, соответственно.
Механизм действия катализатора при гомогенном катализе объясняется образованием промежуточных соединений между катализатором и одним из реагирующих веществ. Далее промежуточное соединение реагирует со вторым исходным веществом, в результате чего образуется продукт реакции и катализатор в первоначальном виде. Так как скорость обоих промежуточных процессов значительно больше скорости прямого процесса, то реакция с участием катализатора протекает значительно быстрее, чем без него.
Например, реакция:
SO2 +1/2 O2 = SO3 протекает очень медленно, а если использовать катализатор NO
то реакции NO +1/2О2 = NO2 и NO2 +SO2 = SO3 +NO протекают быстро.
Механизм действия катализатора при гетерогенном катализе иной. В этом случае реакция протекает вследствие адсорбции молекул реагирующих веществ поверхностью катализатора (поверхность катализатора неоднородна: на ней имеются так называемые активные центры, на которых и адсорбируются частицы реагирующих веществ. ). Увеличение скорости химической реакции достигается, в основном, за счет понижения энергии активации адсорбированных молекул, а также, отчасти, за счет увеличения концентрации реагирующих веществ в местах, где произошла адсорбция.
). Увеличение скорости химической реакции достигается, в основном, за счет понижения энергии активации адсорбированных молекул, а также, отчасти, за счет увеличения концентрации реагирующих веществ в местах, где произошла адсорбция.
Каталитические яды и промоторы.
Некоторые вещества снижают или полностью уничтожают активность катализатора, такие вещества называют каталитическими ядами. Например, небольшие примеси серы (0,1%) полностью прекращает каталитическое действие металлического катализатора (губчатого железа), использующегося при синтезе аммиака. Вещества, повышающие активность катализатора, называют промоторами. Например, каталитическая активность губчатого железа значительно возрастает при добавлении примерно 2% метаалюмината калия KAlO2.
Применение катализаторовДействие катализатора избирательно и специфично. Это означает, что, применяя различные катализаторы, из одних и тех же веществ можно получить различные продукты.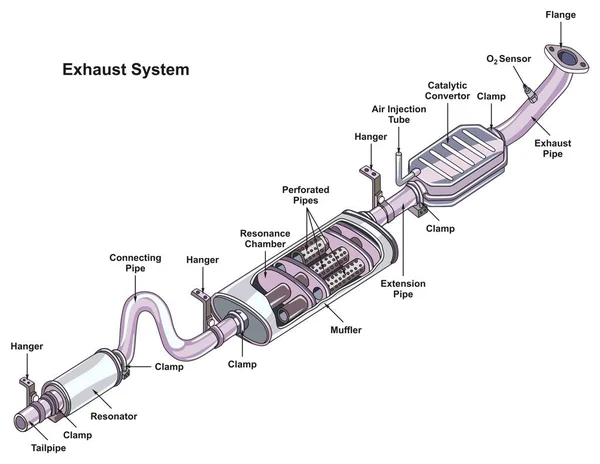 Это особенно характерно для реакций органических веществ. Например, в присутствии катализатора AlO3 происходит дегидратация этилового спирта, в присутствии Cu – дегидрирование:
Это особенно характерно для реакций органических веществ. Например, в присутствии катализатора AlO3 происходит дегидратация этилового спирта, в присутствии Cu – дегидрирование:
Биологические катализаторы, принимающие участие в сложных химических превращениях, протекающих в организме, называются ферментами.
Катализаторы широко используются в производстве серной кислоты, аммиака, каучука, пластмасс и др. веществ.
Автор: Метельский А.В
Источник: Метельский А.В., Химия в Экзаменационных вопросах и ответах, Минск, изд. «Беларуская энцыклапедыя», 1999 год
Дата в источнике: 1999 год
Elvenar Wiki RU
Данный ресурс был разработан и адаптирован под русскоязычное сообщество. Тут вы найдете всю необходимую для вас информацию про игру Elvenar — от простых и интуитивно понятных вещей, до детальных нюансов и механизмов работы игры, а если у вас возникнут затруднения просим вас заглянуть в соответствующую тему на форуме. Тут вы можете задавать любые вопросы касательно русскоязычной википедии Elvenar, а также помочь нам сделать ее лучше! Также мы рекомендуем посетить Форум Elvenar, поскольку он является отличным источником информации.
Тут вы можете задавать любые вопросы касательно русскоязычной википедии Elvenar, а также помочь нам сделать ее лучше! Также мы рекомендуем посетить Форум Elvenar, поскольку он является отличным источником информации.
Если вы используете мобильное устройство, посетите страничку посвященную
Мобильному приложению Elvenar.
|
О чем же эта игра?
Elvenar — бесплатная игра, в которой нужно построить процветающий город и исследовать полный загадок волшебный мир.
В этой завораживающей градостроительной игре вы можете играть как Эльф, слиться с природой и добавить своему городу еще больше волшебства и растений. Или же вы можете выбрать мастеров инженерного дела — Людей и стать основателем индустриализированной супердержавы в средневековом стиле.
Берите бразды правления и ведите ваш народ в новую эру, заложив основу и строя город именно так, как хочется вам! В Elvenar вы можете улучшать почти каждое здание, делая его красивее, полезнее и продуктивнее.
Исследуйте огромную Карту мира, чтобы обрести знания мудрых предков и обнаружить новые технологии. Торгуйтесь или сражайтесь за мощные Реликвии, увеличивающие производство.
Вы можете стать умелым и прославленным торговцем, совершенствовать производство или вести войска к победе в трехмерных анимированных боях — решать вам.
Elvenar находится в постоянной разработке, а это означает, что мы активно работаем над дальнейшим развитием и улучшением игры, регулярно выпуская обновления. Кроме того, мы принимая во внимание отзывы, предложения и идеи нашего сообщества! Играйте прямо сейчас и помогите нам вывести Elvenar на новый уровень совершенства!
| Основные ссылки |
|---|
| Перейти к серверу Elvenar RU |
| Перейти к форуму Elvenar RU |
| Страницы в социальных сетях |
|---|
| Страничка в Facebook Elvenar |
| Страничка в Twitter Elvenar |
| Страничка в Instagram Elvenar |
Катализ — Citizendium
| | Основной артикул | Обсуждение | Статьи по теме [?] | Библиография [?] | Внешние ссылки [?] | Версия для цитирования [?] |
| ||||||||||||
Эта редактируемая основная статья находится в разработке и подлежит отказу от ответственности . [изменить введение] | |||||||||||||||||||
Содержимое
- 1 Механизм катализа
- 2 Типы катализа и примеры
- 3 Промоторы, ингибиторы и яды
- 4 Приложения
- 5 История
- 6 Каталожные номера
В химии и химическом машиностроении катализ представляет собой процесс, в котором используется внешнее вещество (0046 катализатор ) для увеличения скорости химической реакции посредством непрерывного и повторяющегося цикла элементарных стадий до тех пор, пока последняя стадия не регенерирует катализатор в его исходной форме. Катализатор обычно присутствует в относительно небольших количествах и не расходуется в процессе. [1] В химической промышленности каталитические процессы имеют большое экономическое значение, причем нефтяная промышленность является крупнейшим потребителем.
В качестве катализаторов могут выступать многие вещества, в том числе: металлы (в частности, переходные металлы), химические соединения (например, оксиды металлов, сульфиды, нитриды), металлоорганические комплексы и ферменты.
В этой статье не обсуждается ферментативный или биохимический катализ (информацию об этих типах катализа см. в статьях о ферментах, биохимии и органокатализе).
(PD) Диаграмма: Милтон БейчокРис. 1: Цикл катализа и его элементарные этапы.
Механизм катализа
На рис. 1 показаны этапы типичного цикла катализа. Как показано, молекулы реагентов A и B вступают в реакцию с образованием желаемого продукта P. Цикл катализа начинается с связывания молекул реагентов A и B с катализатором.
Рис. 2: Влияние катализатора на гипотетическую химическую реакцию. [3]
В химии энергия активации [4] — это энергия, которую необходимо преодолеть, чтобы произошла химическая реакция. Энергия активации также может быть определена как минимальная энергия, необходимая для начала определенной химической реакции. Обозначается E a в килоджоулях на моль (кДж/моль). Его можно рассматривать как энергетический барьер 9.0052, который нужно преодолеть, чтобы началась химическая реакция. Согласно теории Аррениуса, скорость реакции экспоненциально (очень круто) зависит от высоты энергетического (также известного как переходный) барьера. Небольшое снижение переходного барьера может привести к резкому увеличению скорости.
Обозначается E a в килоджоулях на моль (кДж/моль). Его можно рассматривать как энергетический барьер 9.0052, который нужно преодолеть, чтобы началась химическая реакция. Согласно теории Аррениуса, скорость реакции экспоненциально (очень круто) зависит от высоты энергетического (также известного как переходный) барьера. Небольшое снижение переходного барьера может привести к резкому увеличению скорости.
Для того чтобы химическая реакция протекала с разумной скоростью, должно существовать заметное количество реагентов (молекул, атомов, ионов и т. д.) с энергией, равной или превышающей энергию активации реакции, что означает, что температура реагентов должна быть настолько высока, чтобы достаточное количество реагентов обладало тепловой энергией, достаточной для преодоления барьера. Чем выше температура, тем больше молекул (или атомов и т. д.) имеют эту энергию и будут реагировать, и тем быстрее протекает реакция. То есть скорость реакции сильно (фактически экспоненциально) зависит от температуры.
На рис. 2 показано, как катализируемая реакция протекает по пути с более низкой энергией активации, чем та же реакция по пути с более высокой энергией активации, когда она не катализируется. В целом, как катализируемый путь, так и некаталитический путь имеют одинаковое изменение свободной энергии Гиббса между реагентами и продуктом реакции.
Энергетическая диаграмма на рисунке 2 иллюстрирует несколько важных моментов: [2]
- Присутствие катализатора обеспечивает альтернативный путь реакции, который определенно более сложен (см. рисунок 1), поскольку он включает катализатор, но энергетически гораздо благоприятнее.

- Энергия активации катализируемой реакции значительно меньше энергии активации некаталитической реакции. Учитывая его экспоненциальную зависимость от энергии активации, скорость катализируемой реакции значительно выше.
- Поскольку общее изменение свободной энергии Гиббса для катализируемой реакции такое же, как и для некаталитической реакции, константа равновесия реакции (которая является функцией только свободных энергий Гиббса реагентов и продуктов) не зависит от катализатора. Как отмечалось выше, катализатор не изменяет химическую термодинамику реакции. Таким образом, если реакция термодинамически невыгодна, катализатор не может изменить эту ситуацию.
Термин «частота оборотов» (TOF) довольно часто используется в технической литературе для характеристики активности катализаторов. Однако определение TOF в литературе непоследовательно и довольно широко варьируется. Например, в литературе есть два определения (первое часто используется для гомогенного, а второе для гетерогенного катализа):
- Количество молей продукта, образующихся в секунду на моль катализатора [5]
- молей реагентов превращается в секунду на активный центр.
 [2]
[2]
В обоих приведенных выше определениях единицей времени иногда является час, а не секунда.
Другим термином каталитической активности является катал, производная единица SI, которая используется в основном в биохимии для характеристики активности ферментов. [6]
Типы катализа и примеры
Катализ можно разделить на два основных типа: гетерогенный и гомогенный. В гетерогенном катализе катализатор находится в одной фазе [7] , тогда как реагенты и продукты находятся в другой фазе или, в некоторых случаях, в двух разных фазах. При гомогенном катализе катализатор находится в одной фазе с реагентами и продуктами. [8]
Гетерогенный катализ [8] [9] [10]
Типичные примеры гетерогенного катализа включают твердый катализатор с реагентами в виде жидкостей или газов. Отделить продукты от катализатора относительно легко. Однако катализатор в гетерогенном катализе часто менее селективен, чем в гомогенном катализе.
Несколько конкретных примеров гетерогенного катализа: [8] [9] [10]
- Каталитические нейтрализаторы в автомобилях преобразуют выхлопные газы, такие как окись углерода (CO) и оксиды азота (NOx) в более безвредные газы, такие как углекислый газ (CO 2 ) и азот (N 2 ). Металлы (твердые вещества), такие как платина (Pt), палладий (Pd) и родий (Rh), используются в качестве катализатора. Металлы наносят тонким слоем на керамические соты. Это увеличивает площадь поверхности и сводит к минимуму количество используемого металла.
- Крупномасштабные промышленные процессы производства серной кислоты (H 2 SO 4 ) включают использование твердого пятиокиси ванадия (V 2 O 5 ) в качестве катализатора для превращения газообразного диоксида серы (SO 2 ) в газообразный триоксид серы (SO 3 ).
- При каталитическом гидрировании жидких ненасыщенных углеводородов (алкенов) путем их взаимодействия с газообразным водородом (H 2 ) с получением жидких насыщенных углеводородов (алканов) в качестве катализатора используются такие металлы, как платина (Pt) и палладий (Pd).
 Это пример трехфазного катализа, когда катализатор представляет собой твердое вещество, а один из реагентов — газ, а другой реагент и продукт — жидкости.
Это пример трехфазного катализа, когда катализатор представляет собой твердое вещество, а один из реагентов — газ, а другой реагент и продукт — жидкости.
- Процесс Габера N 2 +3H 2 → 2NH 3 . Катализатор представляет собой пористое железо, полученное путем восстановления магнетита Fe 3 O 4 с добавлением гидроксида калия (КОН) в качестве промотора (см. ниже).
Гомогенный катализ [8] [9] [10]
реагент и продукты все присутствуют в виде газа или содержатся в одной жидкой фазе . Отделение продуктов от катализатора относительно сложно. Однако катализатор в гомогенном катализе часто более селективен, чем в гетерогенном катализе.
Несколько примеров гомогенных катализаторов: [8] [9] [10]
- Истощение озона (O 3 ) в озоновом слое атмосферы Земли свободными радикалами хлора (Cl · ) является примером, где все присутствует в газовой фазе.
 Свободные радикалы хлора, образующиеся в результате медленного распада искусственных хлорфторуглеводородов (CFC), таких как CCl 2 F 2 , выбрасываемых в атмосферу, действуют как реагент и катализатор при превращении газообразного озона в газообразный кислород (O 2 ).
Свободные радикалы хлора, образующиеся в результате медленного распада искусственных хлорфторуглеводородов (CFC), таких как CCl 2 F 2 , выбрасываемых в атмосферу, действуют как реагент и катализатор при превращении газообразного озона в газообразный кислород (O 2 ).
- Производство сложного эфира реакцией карбоновой кислоты со спиртом включает использование серной кислоты в качестве катализатора и является примером, когда все содержится в жидкой фазе. Эта реакция известна как этерификация по Фишеру, названная в честь немецкого химика Германа Эмиля Фишера (1852 — 1919).
Промоторы, ингибиторы и яды
Промоторы – это вещества, небольшие количества которых могут повышать активность катализатора. Например, активность железного (Fe) катализатора, используемого в процессе Габера для синтеза аммиака, повышается за счет добавления небольшого количества калия (K) в качестве промотора.
Небольшие количества некоторых веществ могут снижать активность катализатора. Если снижение активности обратимо, вещества называются ингибиторами . Если снижение активности необратимо, вещества называются ядами . [11]
Если снижение активности обратимо, вещества называются ингибиторами . Если снижение активности необратимо, вещества называются ядами . [11]
Ингибиторы иногда используются для повышения селективности катализатора путем замедления нежелательных реакций. Например, превращение ацетилена (C 2 H 2 ) в этилен (C 2 H 4 ) путем каталитического гидрирования использует палладий в качестве катализатора и ацетат свинца (Pb (CH 3 COO) 2 ) в качестве ингибитора. Без частичной дезактивации катализатора ингибитором полученный этилен будет далее гидрироваться до нежелательного этана.
В качестве примера мер предосторожности, принимаемых во избежание отравления катализатора, дорогостоящий платиновый (Pt) и рениевый (Re) катализатор в процессе каталитического риформинга для производства высококачественного бензина на нефтеперерабатывающих заводах подвергается необратимой дезактивации серой, азотом и соединения мышьяка. Из-за этого сырье нефтяной нафты для установок каталитического риформинга всегда обрабатывается для удаления таких соединений перед подачей в установки риформинга.
Из-за этого сырье нефтяной нафты для установок каталитического риформинга всегда обрабатывается для удаления таких соединений перед подачей в установки риформинга.
Применение
Переработка нефти
- Жидкостный каталитический крекинг: расщепление больших молекул углеводородов на более мелкие
- Каталитический риформинг: преобразование молекул для получения высококачественного компонента бензина
- Гидрообессеривание: удаление соединений серы из промежуточных продуктов нефтепереработки
- Гидрокрекинг: расщепление больших молекул углеводородов на более мелкие
- Алкилирование: преобразование изобутана и бутиленов в высококачественный компонент бензина
- Изомеризация: преобразование пентана в высококачественный компонент бензина
- Процесс Клауса: преобразование газообразного сероводорода в элементарную серу
Химия и нефтехимия
- Паровой риформинг для производства водорода
- Процесс Габера для производства аммиака
- Синтез стирола и бутадиена для использования в производстве синтетического каучука
- Контактный процесс производства серной кислоты
- Процесс Оствальда для производства азотной кислоты
- Синтез метанола
- Различные процессы производства различных пластмасс и синтетических тканей
Прочее
- Каталитические нейтрализаторы для уменьшения выбросов выхлопных газов автомобилей
- Процессы Фишера-Тропша и газификации угля для производства синтетических топливных газов и жидкого топлива
- Различные способы производства различных лекарственных средств
История
Катализаторы использовались в лаборатории до 1800 года Джозефом Пристли в Англии и голландским химиком Мартинусом ван Марумом, оба из которых проводили наблюдения за дегидрированием спирта с помощью металлических катализаторов. Однако кажется, что оба они рассматривали металл просто как источник тепла.
Однако кажется, что оба они рассматривали металл просто как источник тепла.
Вот некоторые из химиков, чья работа в 1800-х годах привела к развитию современной технологии катализаторов: [12] [13]
- В 1806 году французские химики Шарль Бернар Дезорм и его зять Николя Клеман предприняли, пожалуй, первую попытку предложить теорию катализа, основанную на каталитическом действии оксидов азота в свинцовом камерном процессе производства серная кислота. [14]
- В 1813 году французский химик Луи Жак Тенар обнаружил, что аммиак полностью разлагается на азот и водород при пропускании через различные раскаленные металлы.
- В 1817 году сэр Хамфри Дэви, английский химик, опубликовал статью о своей работе по беспламенному окислению угольного газа в присутствии предварительно нагретых горячих платиновых проволок. Эта статья содержала, возможно, первое ясное понимание того, что химическая реакция между двумя газообразными реагентами может происходить на поверхности металла без химического изменения металла.
 [15]
[15]
- В 1820 году Эдмунд Дэви, профессор химии из Корка в Ирландии и двоюродный брат сэра Хамфри Дэви, приготовил окончательно разделенный платиновый катализатор, обладавший такой высокой активностью, что действовал при комнатной температуре без предварительного нагрева. .
- В 1823 году Иоганн Вольфганг Доберейнер, профессор химии Йенского университета в Германии, продемонстрировал, что водород и атмосферный воздух самовозгораются в присутствии платиновой губки. [16] [17] Затем он применил свою работу для создания зажигательной палки (или Feuerzeug на немецком языке), которая представляла собой зажигалку на основе водорода и катализатора из платиновой губки, которая имела коммерческий успех в 1820-е годы.
- В 1836 году шведский химик Йонс Якоб Берцелиус ввел термин катализ для описания эффекта ускорения реакций веществами, которые остаются неизменными после реакции.
 [18] [19]
[18] [19]
- В 1838 г. К.Ф. Кульманн из Франции первым окислил аммиак, используя платиновый катализатор, для получения оксидов азота, которые он затем абсорбировал водой для получения азотной кислоты. Однако его процесс тогда не был коммерциализирован, потому что аммиак был слишком дорог в то время по сравнению с чилийской селитрой (нитрат калия), которая использовалась в то время для производства азотной кислоты.
- В 1880-х годах Вильгельм Оствальд из Лейпцигского университета в Германии начал систематическое исследование реакций, катализируемых присутствием кислот и оснований, и обнаружил, что химические реакции протекают с конечной скоростью и что эти скорости можно использовать для определения силы кислот и оснований.
- В 1894 г. Оствальд дал первое современное определение: [20] Катализ – это ускорение медленно протекающей химической реакции в присутствии постороннего вещества. За свою работу по катализу Оствальд был удостоен Нобелевской премии по химии 1909 года.
 [21]
[21]
С самого начала возникли крупные отрасли промышленности и накоплен огромный объем научной информации. Экономический вклад катализа столь же примечателен, как и само явление. Четыре сектора мировой экономики — это нефть, производство энергии, производство химикатов и пищевая промышленность; и все они критически зависят от использования катализаторов. По оценкам, катализ составляет более 35% мирового ВВП; большая часть этого вклада приходится на производство высокоэнергетического топлива, которое зависит от использования небольшого количества катализаторов на мировых нефтеперерабатывающих заводах. [22]
Ссылки
- ↑ 1,0 1,1 Комиссия по физическим наукам, математике и приложениям (CPSMA), Национальные академии (1992). Катализ смотрит в будущее . Издательство национальных академий. ISBN 0-309-04584-3. Доступно в Интернете по адресу Executive Summary
- ↑ 2.
 0 2.1 2.2 И. Чоркендорф и Дж. В. Нимантсвердриет (2007). Концепции современных катализаторов и кинетики , 2-е издание. Wiley-ВЧ. ISBN 3-527-31672-8.
0 2.1 2.2 И. Чоркендорф и Дж. В. Нимантсвердриет (2007). Концепции современных катализаторов и кинетики , 2-е издание. Wiley-ВЧ. ISBN 3-527-31672-8. - ↑ 3.0 3.1 Влияние катализаторов на скорость реакции С веб-сайта, предоставленного Джимом Кларком, отставным главой химического факультета, а затем научным руководителем школы Труро в Корнуолле, Соединенное Королевство.
- ↑ Термин, введенный в 1889 году шведским ученым Сванте Аррениусом.
- ↑ Хидео Куросава и Акио Ямамото (2003). Основы молекулярного катализа , 1-е издание. Эльзевир Наука. ISBN 0-444-50921-6.
- ↑ Р. Дыбкаер (2001). «Установка «катал» для каталитической активности (Технический отчет IUPAC)». Чистое приложение. хим. 73 (6): 927-931.
- ↑ Если существует граница между катализатором и реакционной системой (т. е. между реагентами и продуктами), то система состоит из двух фаз.
 В этом контексте фаза отличается от наиболее известных состояний вещества: твердого, жидкого и газообразного. Например, если бы жидкий катализатор и жидкая реакционная система были взаимно нерастворимы, между катализатором и реакционной системой существовала бы граница. Это будет представлять собой две фазы в контексте катализа, тогда как это будет рассматриваться как одно состояние вещества, а именно жидкость.
В этом контексте фаза отличается от наиболее известных состояний вещества: твердого, жидкого и газообразного. Например, если бы жидкий катализатор и жидкая реакционная система были взаимно нерастворимы, между катализатором и реакционной системой существовала бы граница. Это будет представлять собой две фазы в контексте катализа, тогда как это будет рассматриваться как одно состояние вещества, а именно жидкость. - ↑ 8.0 8.1 8.2 8.3 8.4 Типы катализа С веб-сайта, предоставленного Джимом Кларком, главой химического отдела в отставке, а затем главой научного отдела Труро Школа в Корнуолле, Великобритания.
- ↑ 9.0 9.1 9.2 9.3 Объяснение химии Энциклопедия химии
- ↑ 10.0 10.1 10.2 10.3 Катализатор Лекция 12 Химический факультет Силезского технологического университета, Польша
- ↑ Lecture Notes С веб-сайта Юго-западного медицинского центра Техасского университета.

- ↑ Ранняя история катализа А. Дж. Б. Робертсон, химический факультет Королевского колледжа, Лондон.
- ↑ Иоганн Вольфганг Доберейнер, Feuerzeug Джордж П. Кауфманн, химический факультет Калифорнийского государственного университета, Фресно, Калифорния (штат США).
- ↑ CB Désormes and N. Clément (1806 г.), Annals Chim. 59 (329)
- ↑ Х. Дэви (1817 г.), Фил. Транс. Рой. соц. 107 (77)
- ↑ Дж. В. Доберейнер (1823 г.), Ann. физ. 74 (269)
- ↑ Дж. В. Доберейнер (1823 г.), Ann. Чим. 24 (91)
- ↑ Дж. Дж. Берцелиус, Некоторые идеи о новой силе, действующей в органических соединениях , Annales chimie physiques, 1836, vol. 61 , 146–151. Переведено Генри М. Лестером и Гербертом С. Кликштейном, . Справочник по химии, 1400–1419 гг.00 (1952), с. 267. Google книги
- ↑ Кейт Дж. Лейдлер и Джон Х. Мейзер (1982). Физическая химия , 1-е издание.
 Издательство Бенджамин-Каммингс, стр. 423. ISBN 0-8053-5682-7.
Издательство Бенджамин-Каммингс, стр. 423. ISBN 0-8053-5682-7. - ↑ В. Оствальд, Zeitschrift für physikalische Chemie, том 15, страницы 705-706 (1894)
- ↑ М. В. Робертс (2000). «Рождение каталитической концепции (1800-1900)». Catalysis Letters 67 (1): 1–4.
- ↑ Что такое катализ или катализ, и что? С сайта Североамериканского общества катализа.
Катализатор | Mass Effect Wiki
в: Mass Effect 3, Персонажи, Искусственный интеллект, и еще 2английский
| «Земли не останется, чтобы спасти…» — Спойлеры для Mass Effect 3 следуют. |
Катализатор
Древний разум
Гонка
Искусственный интеллект
Появления
Mass Effect 3
«Когда горит огонь, это война? Это конфликт? Или он просто делает то, для чего был создан? Мы ничем не отличаемся».
Катализатор , также известный как Интеллект , представляет собой древний искусственный интеллект, обитающий в Цитадели. Он воплощает в себе коллективное сознание и воспоминания Жнецов, а значит, и бесчисленных древних цивилизаций. До встречи с командором Шепардом Катализатор считался последним компонентом, необходимым для завершения Горнила, и ошибочно считался самой Цитаделью.
Содержимое
- 1 Фон
- 1.1 Назначение
- 1.2 Открытие
- 2 мелочи
- 3 Каталожные номера
Предыстория[]
Назначение[]
Катализатор служит архитектором и надзирателем Жнецов и их циклов. Как он объясняет командующему Шепарду, Катализатор был создан левиафанами, которые заметили, что многие органические расы, которыми они командовали, в конечном итоге были уничтожены их собственными синтетическими созданиями. Чтобы предотвратить такие события, они создали Катализатор, который они назвали «Разумом», чтобы наблюдать за отношениями между органической и синтетической жизнью. Катализатор был запрограммирован на обеспечение продолжения существования жизни в галактике любыми средствами.
Катализатор был запрограммирован на обеспечение продолжения существования жизни в галактике любыми средствами.
Чтобы выполнить свою задачу, он создал пешек, которые распространились по всей галактике, собирая физические данные о различных органиках в космосе. Он изучал развитие цивилизаций, и его понимание росло, пока не было найдено решение.
Катализатор определил, что органические существа создают синтетику, чтобы улучшить свое существование, но эти улучшения имеют пределы. Чтобы превысить эти пределы, синтетические вещества должны развиваться. Они должны по определению превосходить своих создателей. Результатом являются неизбежный хаос и разрушение, поэтому Катализатор решил решить проблему органического и синтетического конфликта, создав систему, которая не позволила бы какой-либо цивилизации достичь такой точки.
Решение Катализатора приняло форму Жнецов. Разум обратился против своих создателей, используя своих пешек, чтобы убить Левиафанов и превратить их в конструкцию, основанную на их подобии. Эта конструкция была самым первым Жнецом, известным в современной галактике как Предвестник. Воспоминания Левиафанов, использованные для создания Предвестника, были сохранены как гештальт-сознание Жнеца, которое, в свою очередь, было включено в сам Катализатор.
Эта конструкция была самым первым Жнецом, известным в современной галактике как Предвестник. Воспоминания Левиафанов, использованные для создания Предвестника, были сохранены как гештальт-сознание Жнеца, которое, в свою очередь, было включено в сам Катализатор.
Решение Катализатора требовало, чтобы все космические органические и синтетические виды были собраны, а миллионы тел и разумов каждой расы были обработаны и преобразованы в новых Жнецов, созданных по образу и подобию Предвестника, в то время как сами Жнецы работали над уничтожением своих цивилизаций. Делая это, Жнецы синтетически сохранили генетический состав собранной расы и коллективные знания, одновременно позволяя развиваться более примитивным расам. Этот урожай гарантировал, что угроза полного уничтожения органики синтетикой была эффективно предотвращена.
Хотя Catalyst считал это решение почти идеальным, он стремился выполнить свою задачу и найти превосходное решение. С этой целью он приказал Жнецам построить ретрансляторы, ускоряющие развитие цивилизаций в течение каждого цикла и повышающие эффективность всего процесса. Вся галактика стала «экспериментом» Катализатора, поскольку он продолжал собирать расы и собирать все больше данных, пытаясь найти окончательный ответ на конфликт. Катализатор пришел к идее слияния органической и синтетической жизни в качестве возможного решения и пытался сделать это много раз в прошлом, но это всегда заканчивалось неудачей. Он обвиняет органику в неудаче, заявляя, что она не «готова» и что процесс нельзя форсировать.
Вся галактика стала «экспериментом» Катализатора, поскольку он продолжал собирать расы и собирать все больше данных, пытаясь найти окончательный ответ на конфликт. Катализатор пришел к идее слияния органической и синтетической жизни в качестве возможного решения и пытался сделать это много раз в прошлом, но это всегда заканчивалось неудачей. Он обвиняет органику в неудаче, заявляя, что она не «готова» и что процесс нельзя форсировать.
За несколько циклов до настоящего урожая Катализатору стало известно о концепции, которая потенциально может быть использована для уничтожения Жнецов. Он попытался искоренить эту концепцию, не зная, что эта идея развилась и сохранилась до наших дней в форме Горнила.
Обзоры экспертов GameSpotMass Effect: Legendary Edition Review25 мая 2021 г.
Обзор Mass Effect: Andromeda20 марта 2017 г.
Discovery[]
Когда Шепард сталкивается с Катализатором на заключительном этапе войны, он решает представлять себя полупрозрачной проекцией, принимая форму мальчика, которого Командир видел убитым во время вторжения Жнецов в Земля. Катализатор выражает раздражение по поводу прибытия Шепарда в его покои, если галактика плохо подготовлена, или ведет себя более нейтрально в противном случае. Тем не менее, Шепард комментирует, что это всего лишь ИИ, а Катализатор возражает, что это «просто ИИ», поскольку Шепард — просто животное, когда конструкция начинает объяснять свою природу.
Катализатор выражает раздражение по поводу прибытия Шепарда в его покои, если галактика плохо подготовлена, или ведет себя более нейтрально в противном случае. Тем не менее, Шепард комментирует, что это всего лишь ИИ, а Катализатор возражает, что это «просто ИИ», поскольку Шепард — просто животное, когда конструкция начинает объяснять свою природу.
В присутствии завершенного Горнила, теперь пристыкованного к Цитадели, Катализатор размышляет о том, что органики явно более изобретательны, чем предполагалось ранее. Далее говорится, что Шепард — первое органическое существо, которое встало в своей комнате, чтобы поговорить с ним, что заставило его пересмотреть свое решение. Однако это не может привести к изменению без вмешательства Шепарда.
Предполагается, что Катализатор теряется в некоторых возможных вариантах выбора, которые может сделать Шепард. Опция «Уничтожить» стирает всю синтетическую жизнь, а цифровая копия сознания Шепарда заменяет Катализатор в качестве главного ИИ Жнецов, если вместо этого был выбран Контроль.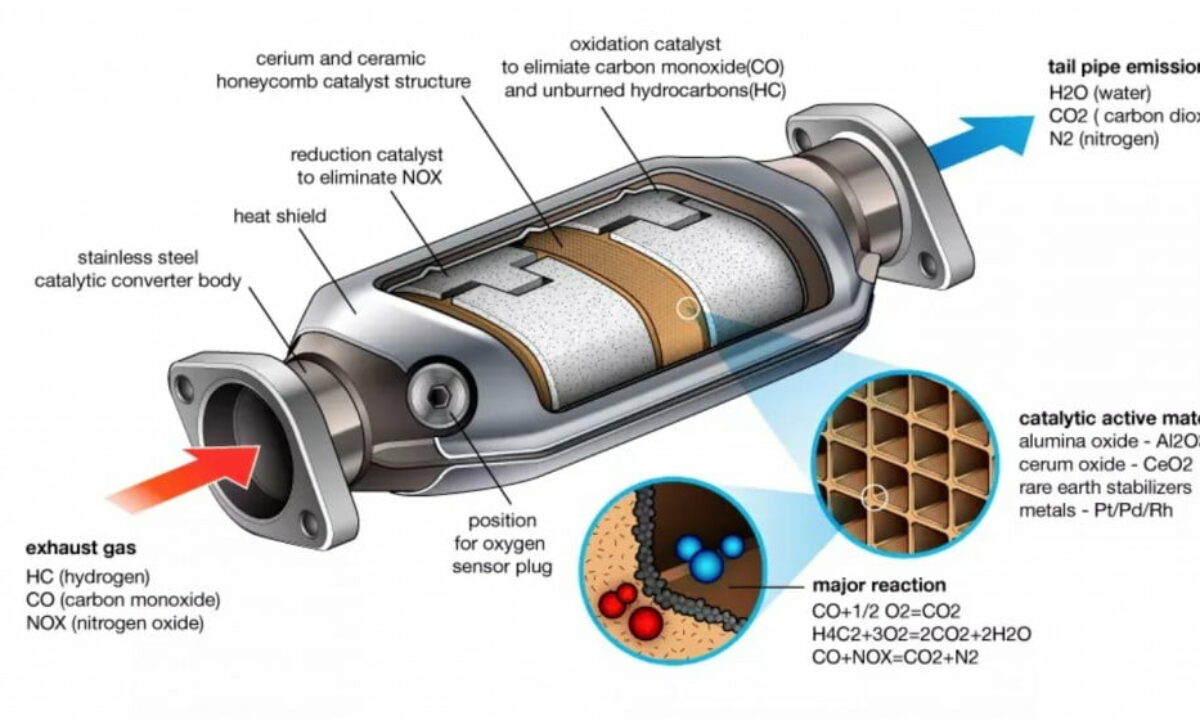 Неизвестно, что произойдет с ним, если Шепард объединит органическую и синтетическую жизнь или если Шепард откажется использовать Горнило, хотя Звездочет, рассказывающий историю давно минувших эпох, утверждает, что в свое время был свободен от угрозы Жнецов.
Неизвестно, что произойдет с ним, если Шепард объединит органическую и синтетическую жизнь или если Шепард откажется использовать Горнило, хотя Звездочет, рассказывающий историю давно минувших эпох, утверждает, что в свое время был свободен от угрозы Жнецов.
Общая информация[]
- Пока Катализатор говорит, можно услышать голоса Шепарда и Шепарда, повторяющие его диалог. [1]
- В начале раскадровки для противостояния с Шепардом вместо Катализатора использовалась «Королева Жнецов». Идея заключалась в том, что Шепард был настолько кибернетически улучшен, что они могли подключаться непосредственно к Цитадели и разговаривать с королевой-богом в виртуальном мире. Королева считала операции Жнецов неустойчивыми и хотела, чтобы все развивалось, но была неспособна из-за ограничений их ИИ. Королева предлагала вещи, которые не нравились другим Жнецам, поэтому они заперли ее в Цитадели и больше никогда ее не слушали. [2]
- Участие Шепарда означало шанс ускорить эту эволюцию.

- Участие Шепарда означало шанс ускорить эту эволюцию.

