Плотность электролита в аккумуляторе (таблица норм до и после зарядки)
Содержание
- Когда проверять плотность электролита в аккумуляторе
- Нормальная плотность электролита в АКБ
- Как замерить
- Как привести концентрацию к норме
Периодический контроль плотности электролита аккумулятора автомобиля входит в число обязательных сервисных операций во время эксплуатации АКБ. Этот важный параметр определяет соотношение воды и серной кислоты в жидком реагенте батареи – чем выше концентрация H2SO4, тем выше плотность и наоборот. В быту эта характеристика измеряется в граммах на кубический сантиметр (г/куб.см).
Когда проверять плотность электролита в аккумуляторе
Оптимально подобранный для достижения наилучших параметров батареи состав электролита меняется во время зарядки и разрядки аккумулятора. При разрядке батареи электрохимическая реакция с участием свинца, его диоксида и серной кислоты дает кристаллический сульфат свинца и воду – содержание H2SO4 в электролите падает, плотность жидкого реагента снижается. При зарядке батареи реакция идет в обратном порядке: сульфат свинца и вода превращаются в свинец, диоксид свинца и серную кислоту (плотность жидкости увеличивается).
При зарядке батареи реакция идет в обратном порядке: сульфат свинца и вода превращаются в свинец, диоксид свинца и серную кислоту (плотность жидкости увеличивается).
Если бы реакции протекали строго симметрично, плотность после цикла разряд-заряд была бы ровно такой же, как и до него. На практике полного равновесия достичь невозможно. Часть сульфата свинца останется непрореагировавшим, соответственно, часть воды в электролите не заменится серной кислотой. В итоге плотность электролита уменьшится.
Также к изменению соотношения воды и H2SO4 ведет естественное испарение жидкости. Вода испаряется быстрее кислоты, поэтому при неплотно завернутых пробках плотность электролита также вырастет.
Читайте также
Как часто нужно менять аккумулятор в автомобиле
Отсюда правила периодичности контроля плотности. Ее надо замерять:
- После зарядки батареи от внешнего ЗУ.

- После «кипения» аккумулятора.
- При снижении уровня жидкости в элементах (по любой причине).
- Просто периодически (хотя бы пару раз в год – с наступлением лета и с приходом холодов, а лучше каждые 3 месяца).
Изменение концентрации жидкого реагента часто связано с общим снижением количества электролита в банках. Поэтому одновременно с контролем плотности надо замерить и уровень жидкости в каждом элементе батареи. Если уровень в норме, часть электролита надо удалить и добавить жидкий реагент с соответствующей концентрацией.
Замер уровня электролита.Нормальная плотность электролита в АКБ
Нормальной плотностью электролита заряженного до максимума аккумулятора считается 1,27 г/куб.см. С учетом погрешности измерений можно считать нормой значения в пределах 1,26..1,28 г/куб.см. При меньшей концентрации кислоты ее становится недостаточно для протекания электрохимических реакций, емкость и токоотдача батареи снижаются. А если оставить аккумулятор с низкой плотностью жидкости на морозе, электролит может замерзнуть. Такой аккумулятор придется заменить. При более высокой плотности ускоряются процессы коррозии и склонность к сульфатации.
Такой аккумулятор придется заменить. При более высокой плотности ускоряются процессы коррозии и склонность к сульфатации.
На указанное значение нормальной плотности электролита в аккумуляторе можно ориентироваться в климате Средней полосы России круглогодично. Если АКБ эксплуатируется в других климатических условиях, то плотность надо скорректировать, причем делать это надо дважды в год при наступлении нового сезона. В более жарких регионах концентрацию серной кислоты надо уменьшить, в холодных – увеличить. Это оптимизирует течение электрохимических реакций и позволит более полно использовать возможности аккумулятора. Кроме этого, в условиях пониженных температур повышение плотности ведет к снижению температуры замерзания электролита, что может уберечь АКБ от выхода из строя.
| Климат | Сезон | Плотность электролита при полностью заряженной АКБ, г/куб.см |
|---|---|---|
| Холодный (температура января от минус 30 до минус 50) | Лето | 1,28 |
| Зима | 1,3 | |
| Умеренный и холодный (январь от минус 8 до минус 30) | Круглый год | 1,27 |
| Теплый (январь от минус 7 до +4 | Круглый год | 1,23 |
Жаркий (+4. .+7) .+7) | Круглый год | 1,23 |
Не стоит менять концентрацию электролита вслед за каждым изменением погоды. Вполне достаточно оптимизировать состав жидкого реагента в начале лета и при наступлении зимы.
Как замерить
В первую очередь, надо полностью зарядить аккумулятор. Дальнейшая процедура должна проводиться при температуре +22..+28 градусов, поэтому батарею надо выдержать в комнате с такими условиями хотя бы час. На практике идеальные кондиции бывают не всегда, поэтому во многих случаях придется брать поправку на температуру – с ее ростом плотность снижается (при неизменной концентрации), а с падением – увеличивается. Поправку можно взять из таблицы.
| Температура жидкого реагента, град.С | Поправка к показаниям прибора, г/куб.см. |
|---|---|
| -25..-11 | +0,03 |
| -10..+4 | +0,02 |
| +5..+19 | +0,01 |
| +20..+30 | 0 |
+31. .+45 .+45 | -0,01 |
| +45 и выше | -0,02 |
Для замера плотности используется специальный прибор – ареометр. Подойдет любой, позволяющий измерить плотность более 1 г/куб.см, но лучше применять специальный для автомобильного электролита. Его пределы измерения оставляют обычно 1,1..1,3 г/куб.см (с приемлемой для точного считывания шкалой), что закрывает практически все случаи, с которыми можно столкнуться на практике. Бытовой спиртометр не подойдет – большинство таких приборов рассчитаны на измерение плотности ниже 1 г/куб.см.
Современные ареометры совмещены с грушей для отбора проб (такой прибор еще называют денсиметром). Если ее нет, понадобится дополнительно резиновая груша и стакан из химически инертного материала. Сначала надо втянуть их банки достаточное количество электролита.
Забор электролита денсиметром из банки АКБ.Если прибор комбинированный, можно сразу считать по шкале измеряемое значение.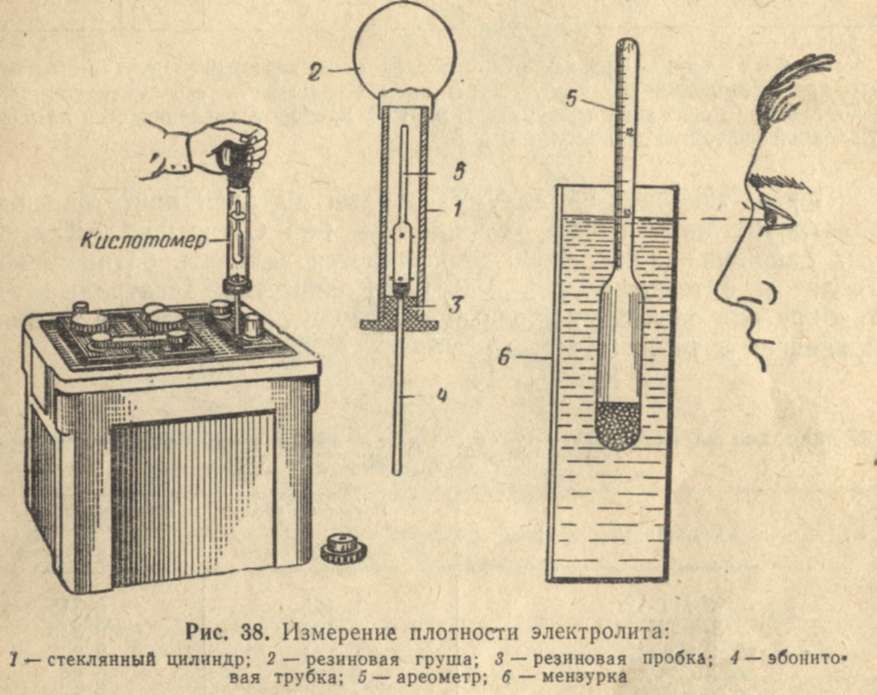 Если обычный – вылить из груши электролит в стакан и в нем произвести замер. Считывание показаний происходит по отметке, соответствующей уровню жидкости. Потом надо вернуть электролит обратно в банку аккумулятора.
Если обычный – вылить из груши электролит в стакан и в нем произвести замер. Считывание показаний происходит по отметке, соответствующей уровню жидкости. Потом надо вернуть электролит обратно в банку аккумулятора.
Считывание показаний ареометра.
Как привести концентрацию к норме
Если концентрация электролита полностью заряженной АКБ отклоняется от нормы, ее надо скорректировать:
- если плотность выше нормы, добавляется дистиллированная вода;
- если ниже нормы – добавляется серная кислота (корректирующий электролит с повышенной плотностью).
Корректирующий электролит плотностью 1,34 г/куб.см.
Вода дистиллированная в емкости 1 литр.
Обычную водопроводную (даже родниковую) воду доливать в батарею нельзя из-за наличия примесей с непредсказуемым составом. Растворенные соли могут осесть на пластинах, уменьшив их полезную площадь, а другие вещества могут вызвать неконтролируемые реакции, снижающие емкость, токоотдачу и срок службы батареи.
Сколько надо добавлять воды или кислоты – можно определить расчетным путем. Но это игра для тех, кто не боится вычислений. В этом случае можно воспользоваться правилом креста (оно же конверт Пирсона). Для этого надо знать, как пересчитать плотность в концентрацию в процентах, объем в массу и т.п. Проще всего довести плотность до нормы опытным путем. Долить немного воды, перемешать (например, встряхнув батарею или подождав пару часов), затем замерить плотность еще раз. Если необходимо, снова добавить жидкости, сообразуясь с предыдущим изменением концентрации.
Доливать жидкость в банку удобно с помощью воронки или шприца.Также существуют необслуживаемые батареи. В них операции с контролем электролита исключены. Но если АКБ обычной конструкции, то лучше следить за состоянием жидкого реагента, тогда аккумулятор прослужит долго и надежно.
В них операции с контролем электролита исключены. Но если АКБ обычной конструкции, то лучше следить за состоянием жидкого реагента, тогда аккумулятор прослужит долго и надежно.
что это за величина, норма, как определить, можно ли снизить (повысить)
Чтобы понять, каково химическое состояние электролита, необходимо произвести его анализ и замерить плотность (p) вещества.
Электролитная (р) обусловливается многими причинами, поэтому необходимо умение правильно ее определять, ведь от этого определения будет зависеть и работа любого авто.
Параметр – плотность (p)
Скалярная физическая величина, которая определяется отношением массы (m) тела к его объему (V), и есть понятие (р). У электролита для аккумуляторов на основе свинца эта величина будет выражена в граммах на кубический см.
Определить (р) кислотного вещества на глаз невозможно. Чтобы точно измерить ее, понадобится специальный «агрегат».
Устройство для измерения (p)
В качестве устройства по измерению плотности электролита может выступить обыкновенный медицинский шприц V=10 куб. см, а также весы, которые работают как можно точнее.
см, а также весы, которые работают как можно точнее.
Далее с помощью незамысловатых действий начинаем измерять:
- Взвешиваем медицинский шприц на весах и записываем его вес.
- Натягиваем на шприц трубочку из резины и опускаем ее в банку аккумулятора.
- Набираем в шприц примерно десять миллилитров кислотного вещества.
- Кладем по новой шприц на весы (но уже без трубки) и заново отмечаем результат.
- Затем вычисляем:
- m (шприца с электролитом) — m (пустого шприца) = a;
- a:10.
Так мы получим точный результат (р) в 1 аккумуляторном сосуде. Далее таким же методом делается замер кислотосодержащей жидкости во всех банках.
Постоянное измерение (р) в таком режиме становится делом муторным и надоедающим. Поэтому есть другой способ измерения параметра электролита. И производится он ареометром (прибором для точного определения удельного веса жидкости и крепости раствора).
Ареометр представляет собой колбу со стеклянным поплавком внутри. Внутренняя часть поплавка утяжелена свинцовой дробью. Когда жидкость набирается в колбу, поплавок строго находится в положении вертикали.
Внутренняя часть поплавка утяжелена свинцовой дробью. Когда жидкость набирается в колбу, поплавок строго находится в положении вертикали.
От чего зависит плотность электролита
Кислотосодержащей жидкости в аккумуляторе свойственно меняться. Это зависит от ряда причин:
- Зависит от заряда аккумулятора (прямая взаимосвязь).
- Если корпус АКБ негерметичен. Потеря жидкости, а затем разбавление ее с помощью дистиллированной воды значительно снизят плотность.
- Замена воды электролитом. При испарении жидкости (в жару), плотность увеличится.
- Электролит приготовлен неверно. Обычно при самостоятельной заготовке.
- Усиленное испарение воды из аккумуляторных сосудов в жаркий период.
Почему нарушилась концентрация кислотной жидкости, можно определить и дома. Но вот насколько отклонилось это значение, для этого надо знать его стандартную величину.
Необходимая (p) жидкого вещества в АКБ
Плотность электролита зависит от климатических условий, в которых используется кислотная АКБ.
Плотность в зимнее время года
В зимний период времени надо обязательно поддерживать состояние SO4 в электролите. Иначе ему будет грозить замерзание при температурах ниже нулевой отметки.
(р) полного аккумулятора будет в пределах 1,27-1,28 грамм на кубический см. При таких параметрах АКБ не страшен будет мороз и в минус 70 градусов.
Если же (р) снижается до отметки 1,20 гр на см в кубе, жидкое вещество при t= -30 гр. по Ц. застынет.
Поэтому всегда необходимо следить за тем, чтобы аккумулятор при низких температурах был обязательно заряжен, ведь при замерзании электролита (р) его достаточно увеличится в V.
Если не соблюдать этих простых правил и все отправить на самотек, можно потерять АКБ раз и навсегда. Внутренние пластины разрушатся, и аккумулятор станет неисправным.
Плотность в летнее время года
В результате испарения воды в летний период времени (р) дано свойство самопроизвольно повышаться.
При работе с повышенной плотностью эксплуатация АКБ значительно снизится. Кислотная жидкость может погубить сепараторы аккумулятора.
Кислотная жидкость может погубить сепараторы аккумулятора.
Чтобы этого не случилось, необходимо в жаркое время года электролит обязательно разбавлять дистиллированной водой. Постоянный контроль за ним поможет избежать множество отрицательных последствий.
Как проверяется (р) в АКБ
Для того чтобы постоянно измерять плотность содержимого АКБ, необходимо воспользоваться ареометром. Далее:
- открутить пробки АКБ;
- ввести узкий конец в сосуд батареи;
- груша вверху оборудования сожмется. Отпускаем верхнюю часть, и отрицательное давление заполнит полностью сосуд электролитом.
С помощью шкалы поплавка узнаем точную концентрацию кислотосодержащей жидкости.
Измерение величины (р) в необслуживаемой АКБ
В необслуживаемых батареях нет на верхнем корпусе изделия дырок, через которые бы возможно было измерить плотность электролита. Они были не предусмотрены производителем изначально. А значит, и измерение (р) внутри АКБ невозможно.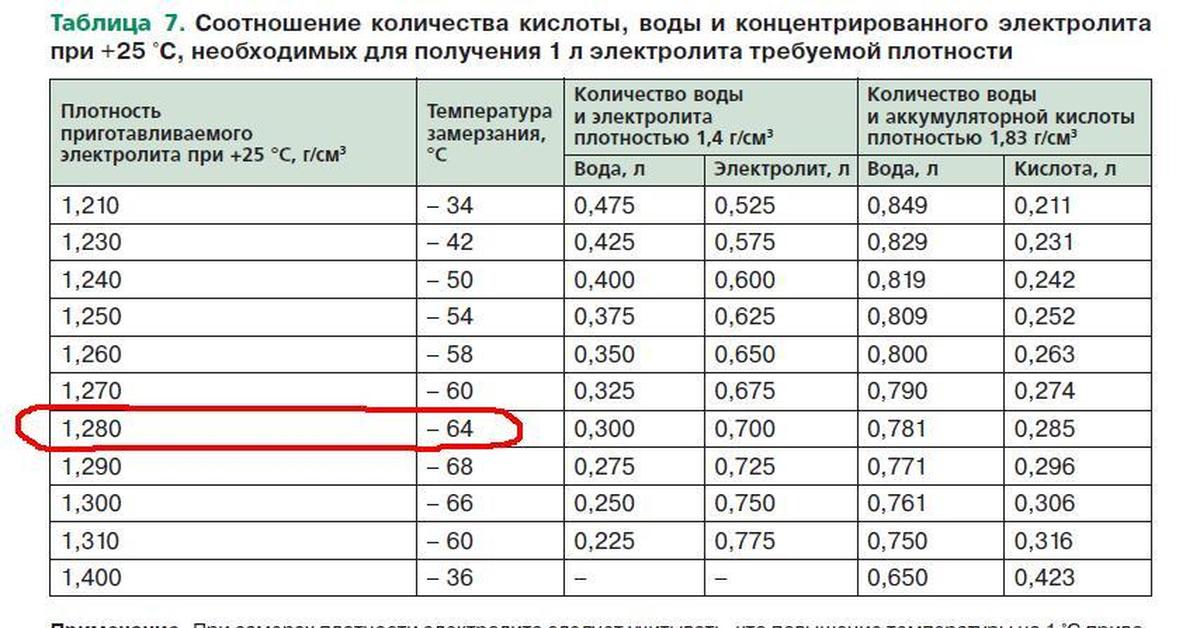 Или?!
Или?!
Все невозможное – возможно. Умелые мастера и тут нашли выход. Они с легкостью убрали преграду и улучшили работу изделия, в котором были небольшие отклонения.
При помощи обыкновенной дрели были высверлены в верхнем корпусе (крышка) батареи отверстия, и доступ внутрь для каждой банки стал открытым.
И благодаря «дуновению волшебной палочки» необслуживаемая модель стала обслуживаемой.
Далее делается специальная резьба для просверленных дыр, изготавливаются пластиковые пробки с соответствующей по диаметру отверстий резьбой. Их вставляют в отверстия, и АКБ становится обслуживаемой.
Существует и метод №2
Он не менее популярный, чем предыдущий. Здесь уже в работе понадобится сверло, с помощью которого просверливаются шесть дырочек, через которые откроется доступ к банке аккумулятора.
После замера плотности электролита корпус изделия можно восстановить с помощью герметика из силикона. Герметизировать крышку надо со всей осторожностью, нельзя допускать попадания мелких стружек на отверстиях внутрь прибора.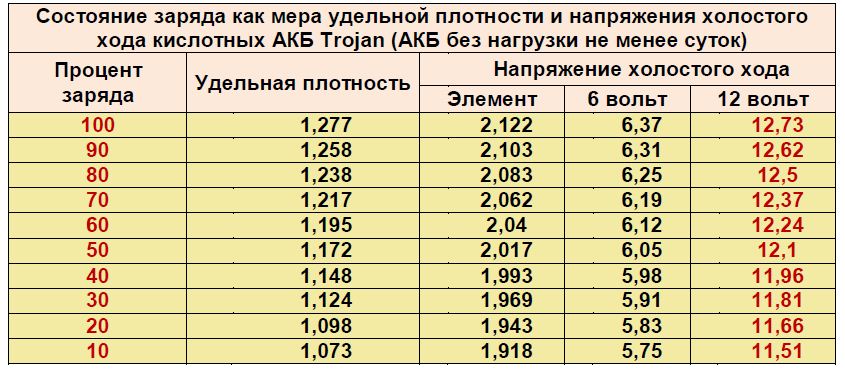
Для этого с помощью самодельного крючка, сделанного из проволоки, постараемся осторожно выпрямить часть продавленной пластмассы.
Помните! В результате механического повреждения изделия (просверленные дырки), аккумуляторная гарантия пропадает. Но это не самое страшное. Неправильные действия могут привести к выходу оборудования из строя. Стружки, попавшие внутрь АКБ, также значительно снизят жизнь батареи.
Как увеличить плотность электролита
Плотность электролита обычно снижается в негерметичных изделиях. Добавление дистиллированной h3O и является данной причиной. Наступает разница в концентрации банок аккумулятора.
Если (р) не получается привести к одинаковому значению во всех сосудах с помощью ЗУ, то потребуется заменить кислотную жидкость новым электролитом.
Восполним плотность электролита в следующей очередности:
- из банки, где нарушен состав кислотного вещества, убираем с помощью груши все ее содержимое;
- затем начинаем восполнять этот пробел, заливая новую электролитную смесь в сосуд.

Если плотность электролита не увеличится, то данную процедуру необходимо повторить по новой.
Как снизить плотность электролита
Если концентрация плотности электролита превышает отметку 1,28 г/см3, ее надо понижать, иначе это может привести к потере работоспособности аккумуляторной батареи.
Понижение (р) выполняется так же, как и повышение.
Оценка плотности энергии · Мэтт Лейси
Инвентаризация лития
С 2016 года многие тысячи из вас посетили этот веб-сайт из-за его научного содержания — спасибо всем за посещение! Теперь начинается процесс переноса образовательных частей этого сайта в мой новый проект Lithium Inventory. Lithium Inventory задуман как бесплатный и открытый центр знаний в области аккумуляторной науки и электрохимии.
Вы здесь: Дом » Наука » Литий-серные батареи » Оценка плотности энергии
Пару лет назад я сделал электронную таблицу Excel, чтобы оценить, на чем будет основываться гравиметрическая плотность энергии (или, точнее, *удельная энергия*) увеличенного литий-серного (Li-S) элемента. различные параметры и показатели эффективности из экспериментальных испытаний. В то время я работал над проектом с заявленной целью производства элемента мощностью 400 Втч/кг в конце проекта (амбициозная цель, и хотя в целом проект был очень успешным и продуктивным, далеко от этой цели).
Недавно я перевел эту таблицу в приложение Shiny, и теперь она доступна здесь. Я подумал, что было бы интересно связать это приложение со страницей, описывающей различные параметры, откуда берутся значения по умолчанию, которые я выбрал, и какие значения кажутся реалистичными с учетом текущей литературы.
Откройте приложение здесь
Приложение довольно простое и должно выглядеть так, как показано на скриншоте ниже. Просто измените значения, как вам нравится, и посмотрите, что произойдет.
Плотность энергии рассчитывается очень просто:
$$\text{плотность энергии} = \frac{Q_d \cdot E_{\text{mean}}}{\sum m_x}$$
где \(Q_d\) — «поверхностная емкость» (или площадь разрядной емкости) электрода в мАч/см2, \(E_\text{mean}\) — среднее напряжение разряда, а \(\sum m_x\) есть сумма всех масс всех компонентов в г/см2. Произведение Q и E дает энергию, а деление на сумму всех масс дает плотность энергии для всего пакета ячеек.
Можно изменить следующие параметры:
- Использование серы (мАч/г) – более узнаваемо, разрядная емкость, выраженная на единицу массы серы.
 Значение по умолчанию равно 900, что примерно соответствует тому, что мы получаем в типичных тестовых батареях, которые мы создавали в течение последних 18 месяцев. Теоретически это 1672. Литературные значения встречаются повсюду, обычно между 600 и 1000, но иногда сообщалось о значениях ~ 1200 и выше, но реже.
Значение по умолчанию равно 900, что примерно соответствует тому, что мы получаем в типичных тестовых батареях, которые мы создавали в течение последних 18 месяцев. Теоретически это 1672. Литературные значения встречаются повсюду, обычно между 600 и 1000, но иногда сообщалось о значениях ~ 1200 и выше, но реже. - Среднее напряжение разряда (В) — по умолчанию 2,13, что также характерно для наших аккумуляторов. Теоретическая, по свободной энергии образования Гиббса, равна 2,24.
- Содержание серы (мг/см 2 ) — Количество серы на положительном электроде. Значение по умолчанию равно 3, что является типичным для нашего текущего исследования и разумным минимальным значением для практической системы. Литературные значения чаще всего составляют от 0,5 до 2, но относительно редко сообщаются значения >4.
- Доля серы (%) — Доля композита положительного электрода, которая представляет собой элементарную серу. Оставшаяся фракция обычно представляет собой проводящие добавки и связующие вещества.
 По умолчанию 65, это то, что мы используем. Литературные значения чаще всего находятся между 40 и 60, при этом сообщается до 80.
По умолчанию 65, это то, что мы используем. Литературные значения чаще всего находятся между 40 и 60, при этом сообщается до 80. - Отношение электролит/сера (мкл/мг) — Отношение объема электролита к массе серы в электроде. Значение по умолчанию — 5, что является наименьшим целочисленным значением, при котором наши клетки работают более нескольких циклов (мы использовали 6 в большинстве наших недавних публикаций). Литературные значения чаще всего не сообщаются, но варьируются от 6 до 100. В нескольких недавних статьях сообщается, что «оптимальное» значение находится между 10 и 20. До сих пор я не видел значений ниже 6 ни в одной опубликованной статье. за исключением статьи Sion Power 2010 года [здесь] — работая в обратном направлении от рисунка в этой статье, описывающего элементы емкостью 2,8 Ач, можно оценить отношение E / S примерно. 2.4 соответствовали батареям со сроком службы ~50 циклов.
- Плотность электролита (г/см 3 ) — не требует пояснений.
 Значение по умолчанию — 1,09, это то, что я ранее оценил плотность нашего стандартного электролита (1 M LiTFSI, 0,25 M LiNO
Значение по умолчанию — 1,09, это то, что я ранее оценил плотность нашего стандартного электролита (1 M LiTFSI, 0,25 M LiNO - Масса сепаратора (мг/см 2 ) – по умолчанию 0,894, что соответствует массе пористых полиэтиленовых сепараторов, которые мы использовали в последние годы.
- Толщина лития (мкм) — Толщина литиевого отрицательного электрода. Значение по умолчанию — 50, что вполне приемлемо для практичной батареи. Мы используем литиевую фольгу толщиной 125 и 30 мкм. Литературные ценности встречаются редко. Литиевая фольга продается в широком диапазоне толщин. Наиболее часто используемая фольга в академических лабораториях, вероятно, находится в диапазоне 100–1000 мкм.
- Толщина алюминия (мкм) — Толщина алюминиевого (положительного) токосъемника. Значение по умолчанию — 14, приемлемое для типичных литий-ионных аккумуляторов.
- Толщина меди (мкм) – Толщина медного (отрицательного) токосъемника.
 Значение по умолчанию — 9, приемлемое для типичных литий-ионных аккумуляторов. Было высказано предположение, что если избыток литиевого отрицательного электрода достаточно высок, он может быть его собственным токосъемником, и поэтому медь не потребуется; плотность металлического лития составляет часть плотности меди и (очевидно) дешевле на единицу площади.
Значение по умолчанию — 9, приемлемое для типичных литий-ионных аккумуляторов. Было высказано предположение, что если избыток литиевого отрицательного электрода достаточно высок, он может быть его собственным токосъемником, и поэтому медь не потребуется; плотность металлического лития составляет часть плотности меди и (очевидно) дешевле на единицу площади.
Попробуйте изменить параметры в диапазонах, которые я предложил выше для начала. Есть над чем подумать: насколько высокой будет плотность энергии при значениях в этих диапазонах? Какая часть клетки составляет активную массу (т. е. Li и серу?) Какой самый большой вклад в массу? Что еще нам нужно улучшить, чтобы достичь, скажем, 400 или 500 Втч/кг?
Внимание! Упаковка ячеек (в настоящее время) не включена в эти расчеты! Плотность энергии ячейки, конечно, будет зависеть от массы упаковки. Это частично зависит от формата (размера, типа и т. д.) ячейки. Я бы предположил, что разумная оценка клеточной упаковки составляет около 10% от общей массы клетки, но это всего лишь обоснованное предположение.
Также обратите внимание: Избыток на отрицательном электроде также указан в приложении — это важно! Если он отрицательный, это означает, что емкость на литиевом электроде ограничена, и плотность энергии элемента будет снижена. Это учитывается в расчетах.
Полезная литература по теме: Hagen et al (2015), Urbonaite et al (2015), Pope et al (2015), Mikhaylik et al (2010), Berg et al (2015).
Я также написал отдельный пост, предоставляющий некоторый контекст этой странице. Вы можете найти это здесь.
Включите JavaScript для просмотра комментариев на платформе Disqus.comments на платформе Disqus
Как химический состав батареи определяет производительность
Химические реакции лежат в основе конструкции батареи Аккумуляторы с продуманной конструкцией обеспечивают эффективное, надежное и безопасное питание вашего оборудования в течение длительного срока службы. Чтобы достичь этой комбинации идеалов, инженеры оценивают определенные параметры конструкции, включая требуемое напряжение и мощность, продолжительность рабочего цикла, температурные условия, цену и многое другое, чтобы определить свой выбор конструкции.
Химия аккумуляторов, возможно, является наиболее фундаментальным выбором при проектировании. По своей сути все батареи представляют собой удобно упакованные электрохимические реакции. Способность батареи накапливать и разряжать электричество напрямую зависит от типа химической реакции.
В этой статье мы подробно рассмотрим, как химия влияет на производительность. Затем мы рассмотрим свойства некоторых распространенных химических веществ.
Для разработка, тестирование и производство нестандартного аккумуляторного блока выберите Ave. Мы создадим аккумуляторные блоки, идеально подходящие для вашего конкретного применения. Свяжитесь с нами по телефону для получения дополнительной информации о процессе или запросите предложение сегодня .
Химический состав батарей влияет на напряжение, плотность энергии, перезаряжаемость, саморазряд, срок службы и безопасность. Аккумуляторная батарея состоит из одного или нескольких упакованных аккумуляторных модулей. Батарейный модуль состоит из гальванических элементов, расположенных параллельно или последовательно. Электрохимический элемент, также называемый гальваническим элементом, состоит из трех основных частей: анода , катода и электролита . Вместе анод, катод и электролит обеспечивают произойдет реакция окисления/восстановления .
Батарейный модуль состоит из гальванических элементов, расположенных параллельно или последовательно. Электрохимический элемент, также называемый гальваническим элементом, состоит из трех основных частей: анода , катода и электролита . Вместе анод, катод и электролит обеспечивают произойдет реакция окисления/восстановления .
Реакции окисления/восстановления связаны с потоком электронов . Когда железо окисляется, атомы железа отдают электроны, а молекулы кислорода приобретают электроны. Разница между ржавым куском металла и батареей заключается в разделении этих двух событий. Это заставляет электроны течь по цепи, чтобы завершить реакцию. При разряде анод теряет электроны, а катод их приобретает. Электролит способствует этим реакциям и позволяет ионам существовать в растворе.
Во время разрядки батареи анод окисляется и отдает электроны. Электроны текут по цепи к катоду, вызывая реакцию восстановления. Электролит обеспечивает обмен ионами. При зарядке аккумулятора процесс обратный. Состав анода, катода и электролита изменяет многие свойства батареи.
Электролит обеспечивает обмен ионами. При зарядке аккумулятора процесс обратный. Состав анода, катода и электролита изменяет многие свойства батареи.
Вот некоторые электрические свойства, которые зависят от химического состава батареи:
Напряжение элемента
Все гальванические элементы одного химического состава производят одинаковое номинальное напряжение . Это связано с тем, что напряжение напрямую связано с благоприятностью реакции окисления/восстановления. Более благоприятные реакции производят более высокие напряжения. Например, литий-ионные аккумуляторы имеют номинальное напряжение около 3,6 В.
Плотность энергии
Напряжение — не единственный показатель ценности батареи. Вы можете получить любое необходимое вам напряжение и ток при правильном расположении ячеек последовательно и параллельно. В зависимости от ваших потребностей, это может быть тяжелым, громоздким и дорогим. Плотность энергии измеряет энергию, запасенную батареей, по отношению к ее размеру. Гравиметрическая плотность энергии измеряется в ватт-часах на килограмм (Втч/кг).
Плотность энергии измеряет энергию, запасенную батареей, по отношению к ее размеру. Гравиметрическая плотность энергии измеряется в ватт-часах на килограмм (Втч/кг).
Перезаряжаемость
Общеизвестно, что химические реакции протекают в двух направлениях. Вы можете начать с реагентов и получить продукты или использовать продукты для повторного получения реагентов. Если вы примените обратное напряжение и ток, вы можете заставить анод принимать электроны, а катод отдавать их, перезаряжая батарею — по крайней мере, в теории. На практике отменить некоторые реакции может быть чрезвычайно сложно. Первичные элементы — это батареи, химический состав которых делает их перезарядку неэкономичной или небезопасной. Это одноразовые батарейки. Вторичные элементы , также известные как перезаряжаемые батареи, основаны на легко обратимой электрохимии. В этой статье мы сосредоточимся на химии вторичных клеток.
Саморазряд и срок службы
В идеальном мире мы могли бы заряжать и разряжать батареи снова и снова без потери производительности или оставлять их на полке на месяцы без потери заряда. В реальном мире гальванические элементы страдают от нежелательных химических реакций. Пока батарея лежит на полке, происходят спонтанные химические реакции, которые истощают заряд батареи. это называется саморазряд .
Аналогичным образом, когда батарея заряжается и разряжается, происходят нежелательные химические реакции, которые снижают способность батареи накапливать электричество. Количество циклов, которое батарея может использовать до того, как она перестанет работать должным образом, составляет циклов жизни .
Как скорость саморазряда, так и продолжительность срока службы зависят от химического состава батареи. Однако они также зависят от условий использования и хранения.
Экономика, окружающая среда и безопасность
Наконец, примите во внимание экологические и экономические соображения. Некоторые химические вещества для аккумуляторов просто дороже других. Литий-ионные элементы популярны и не зря, но нехватка металлического лития делает их дорогими.
Некоторые химические вещества для аккумуляторов просто дороже других. Литий-ионные элементы популярны и не зря, но нехватка металлического лития делает их дорогими.
В своих экономических расчетах также следует учитывать вопросы охраны окружающей среды и безопасности. Некоторые химические вещества аккумуляторов очень токсичны или вызывают коррозию, что может осложнить утилизацию.
Химикаты на основе никеляБудучи доступными и проверенными, химические вещества на основе никеля имеют множество применений. В этой статье мы сосредоточимся на трех основных химических соединениях никеля: никель-кадмий, никель-металлогидрид и никель-железо. Химия никель-цинк и никель-водород также существуют, хотя они нашли меньшее применение. Никель-водородные батареи особенно широко используются на спутниках из-за их широкого диапазона допустимых температур.
Никель-кадмиевые
Никель-кадмиевые (NiCd) батареи прочные, эластичные и имеют длительный срок службы. Их напряжение также очень стабильно, настолько, что состояние заряда нельзя определить по падению напряжения, как у других аккумуляторов. NiCd элементы можно заряжать очень быстро без ущерба для безопасности. Наконец, никель-кадмиевые аккумуляторы являются одними из самых доступных вторичных аккумуляторов на рынке.
Их напряжение также очень стабильно, настолько, что состояние заряда нельзя определить по падению напряжения, как у других аккумуляторов. NiCd элементы можно заряжать очень быстро без ущерба для безопасности. Наконец, никель-кадмиевые аккумуляторы являются одними из самых доступных вторичных аккумуляторов на рынке.
Однако никель-кадмиевые аккумуляторы имеют некоторые недостатки. Во-первых, хотя они превосходят свинцово-кислотные батареи по плотности энергии, они работают хуже, чем другие современные химические батареи. Во-вторых, они имеют высокую скорость саморазряда .
В NiCd батареях наблюдается интересное, но неудобное явление: эффект памяти . Эффект памяти заключается в том, что со стороны никель-кадмиевые батареи «вспоминают», насколько глубоко они были разряжены в прошлом, и обеспечивают только такую глубину разряда в будущих циклах. Это вызвано накоплением кристаллов соли, которые блокируют электрод.
Образование кристаллов вызывает эффект памяти. Наросты кристаллов блокируют активную часть анода. Верхнее изображение показывает нормальное образование кристаллов на аноде. На нижнем изображении видны крупные обструктивные кристаллы. Источник: Aero Electric
Наросты кристаллов блокируют активную часть анода. Верхнее изображение показывает нормальное образование кристаллов на аноде. На нижнем изображении видны крупные обструктивные кристаллы. Источник: Aero Electric
Наконец, и это, пожалуй, самое главное, никель-кадмиевые элементы представляют опасность для окружающей среды. Кадмий очень токсичен, а электролитом является гидроксид калия, очень сильное основание. Эти опасности затрудняют правильную утилизацию NiCd элементов. Хотя NiCd-элементы иногда считаются устаревшими, они по-прежнему используются в нишевых приложениях, таких как авиация.
Ознакомьтесь со следующими характеристиками никель-кадмиевой батареи:
- Номинальное напряжение элемента : 1,2 В
- Плотность энергии : ~45-80 Втч/кг
- Анод : Гидроксид никеля
- Катод : Гидроксид кадмия
- Электролит : Гидроксид калия
- Саморазряд : ~10%
- Опасность для окружающей среды : Токсичный, коррозионный 9 0078
- 1,2 В
- ~60-120 Втч/кг
- 20% в течение 24 часов, затем 10% в месяц
- Номинальное напряжение элемента : ~1,2 В
- Плотность энергии : ~50 Втч/кг
- Анод 900 04 : Железо
- Катод : Оксид никеля гидроксид
- Электролит : Гидроксид калия
- Саморазряд : 20-30% в месяц
- Опасность для окружающей среды : Коррозионный
- Номинальное напряжение элемента : ~2 В
- Плотность энергии : 30-50 Втч/кг
- Анод 90 004 : ведущий (с другими)
- Катод : диоксид свинца
- Электролит : серная кислота
- Саморазряд : 5% в месяц
- Опасность для окружающей среды : токсичный, коррозионный 9003 3
- Номинальное напряжение элемента : 3,6 В
- Плотность энергии : 110-265 Втч/кг
- Анод : углерод, кремний, другие
- Катод : соединения лития
- Электролит : литий соли в органических растворителях
- Саморазряд : от 0,35% до 2,5% в месяц
- Опасность для окружающей среды : Горючий органический электролит 04
Из договоренности элементов в систему управления температурным режимом, многие факторы определяют производительность аккумуляторной батареи. Химический состав батареи является фундаментальным выбором при проектировании и выборе батареи.

Никель-металлогидрид
Никель-металлогидридные (NiMH) элементы представляют собой более современную версию NiCd элементов. На первый взгляд, элементы NiMH все еще очень похожи на элементы NiCd — в них по-прежнему используется щелочной электролит, такой как гидроксид калия, а в качестве катода по-прежнему используется гидроксид никеля.
На первый взгляд, элементы NiMH все еще очень похожи на элементы NiCd — в них по-прежнему используется щелочной электролит, такой как гидроксид калия, а в качестве катода по-прежнему используется гидроксид никеля.
Основное отличие состоит в том, что в ячейках NiMH токсичный кадмий заменен на более эффективные аноды. Точный состав варьируется — отсюда и использование слова «металл», — но все аноды представляют собой сплавы редкоземельных металлов. Такая замена увеличивает стоимость, но делает их более экологичными и обеспечивает большая емкость , уменьшает эффект памяти , снижает чувствительность к температуре .
Ознакомьтесь со следующими характеристиками никель-кадмиевых аккумуляторов:
9000 3 Никель-железо
Никель-железные элементы встречаются редко, возможно, из-за их высокой цены, низкой плотности энергии и высокого саморазряда. Тем не менее, они эластичны, долговечны и устойчивы к высоким температурам.
Тем не менее, они эластичны, долговечны и устойчивы к высоким температурам.
Ознакомьтесь с техническими характеристиками никель-железной батареи:
Свинцово-кислотные аккумуляторы — рабочие лошадки. Эти прочные и надежные батареи обеспечивают питание по низкой цене и имеют низкий уровень саморазряда. Помимо экологических проблем, связанных со свинцовыми и сильнокислотными электролитами, основными недостатками свинцово-кислотных аккумуляторов являются вес и низкая плотность энергии. Это делает их идеальными для ситуаций, когда вес не имеет большого значения, например, автомобили, тележки для гольфа, вилочные погрузчики и источники бесперебойного питания.
Это делает их идеальными для ситуаций, когда вес не имеет большого значения, например, автомобили, тележки для гольфа, вилочные погрузчики и источники бесперебойного питания.
Химический состав свинцово-кислотных аккумуляторов различается. Свинец составляет большую часть анода в виде сетки. Однако свинец слишком мягок, чтобы выдерживать собственный вес, поэтому для улучшения структурной целостности и электрохимических свойств используются такие металлы, как сурьма, кальций, олово или селен.
Ознакомьтесь со следующими характеристиками свинцово-кислотных аккумуляторов:
Сегодня литий-ионные (Li-ion) аккумуляторы являются самой популярной вещью в области хранения энергии. Они обеспечивают высокую плотность энергии и при этом остаются легкими, что делает их востребованными для телефонов, компьютеров, электромобилей и многого другого.
Они обеспечивают высокую плотность энергии и при этом остаются легкими, что делает их востребованными для телефонов, компьютеров, электромобилей и многого другого.
В литий-ионных батареях фактически не используется чистый металлический литий. Как и натрий, литий обладает высокой реакционной способностью, и ранние литий-металлические батареи были склонны к возгоранию и взрыву — знакомая проблема для литиевых батарей.
Вместо этого литий-ионные аккумуляторы имеют катоды из ионных соединений лития. Существует несколько химических катодов, включая оксид лития-кобальта (LiCoO2), фосфат лития-железа (LiFePO4), оксид лития-марганца (LiMn2O4) и оксид лития-никель-марганца-кобальта (LiNiMnCoO2).
Аноды для литий-ионных аккумуляторов состоят из пористого материала, такого как графит, который связывает ионы лития и высвобождает их в электролит во время разрядки аккумулятора. Силиконовые аноды также являются перспективными анодными материалами. В будущем графен (листы углерода толщиной в один атом) может использоваться в качестве анодов.
В качестве электролитов в литий-ионных элементах используются соли лития, растворенные в (воспламеняющихся) органических соединениях. Твердые керамические электролиты могут предложить многообещающую альтернативу.
У литий-ионных химикатов есть два основных недостатка: стоит и хрупкость . Литий может быть дорогостоящим, а добыча лития является интенсивным и вредным для окружающей среды процессом. Однако такие металлы, как кобальт, используемые в литий-ионной химии, повышают цены на аккумуляторы не меньше, а то и больше, чем одноименный литий.
Помимо высокой стоимости, литий-ионные аккумуляторы требуют особых условий эксплуатации, поскольку они чувствительны к перезарядке и быстрому разряду. Литий-ионные аккумуляторы заслужили репутацию огневых или взрывоопасных отказов . Благодаря правильному проектированию и тестированию, защите цепи, правильному использованию и предотвращению повреждений этих проблем можно избежать.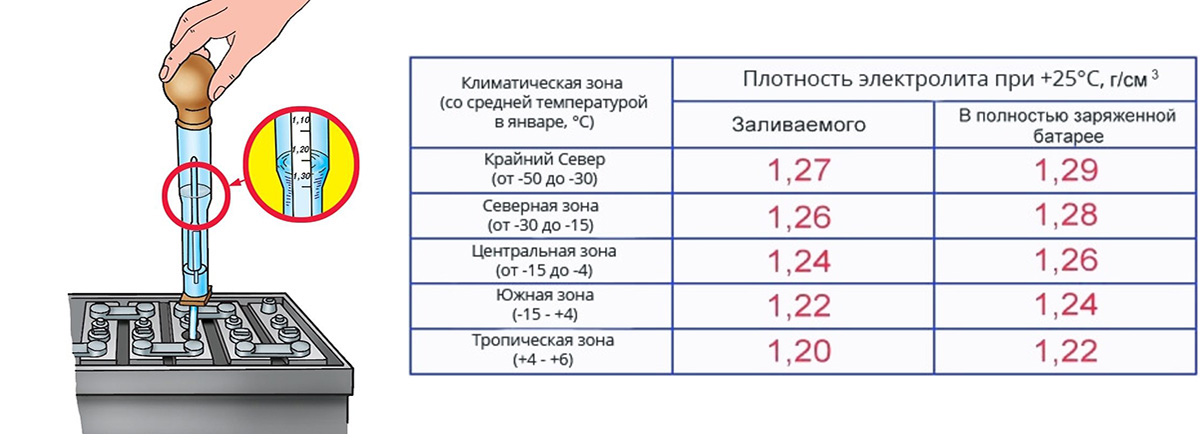 Но факт остается фактом: литий-ионные аккумуляторы хрупкие.
Но факт остается фактом: литий-ионные аккумуляторы хрупкие.
В этом видео из EE World Online показано, что происходит, когда вы удаляете защитные схемы и игнорируете рекомендации по безопасности для литий-ионных аккумуляторов:
Ознакомьтесь со следующими характеристиками литий-ионных аккумуляторов:
