Принцип работы аккумуляторной батареи (АКБ)
Назначение, устройство и принцип работы аккумулятора
Назначение автомобильной аккумуляторной батареи понятно каждому мало-мальски сведущему в технических вопросах автолюбителю. С первой ее функцией — обеспечением запуска двигателя — мы сталкиваемся каждый день. Есть и вторая — реже применяемая, но от того не менее значимая — использование в качестве аварийного источника питания при выходе из строя генератора. Кроме того, на современных автомобилях с электроникой на борту аккумулятор выполняет роль сглаживателя пульсаций напряжения, выдаваемого генератором.
Все стартерные батареи, выпускаемые в настоящее время для автомобилей, являются свинцово-кислотными. В основу их работы заложен известный еще с 1858 г., и по сей день остающийся практически неизменным принцип двойной сульфатации.
Любая автомобильная батарея представляет из себя корпус — контейнер, разделенный на шесть изолированных ячеек — банок.
Каждая банка является законченным источником питания, напряжением порядка 2.1 В. В банке находится набор положительных и отрицательных пластин, отделенных друг от друга сепараторами. Как известно из школьного курса физики, две разнозаряженные пластины уже сами по себе являются источником постоянного напряжения, параллельное же их соединение увеличивает ток.
Последовательное соединение шести банок и дает батарею с напряжением порядка 12.6 В. Любая из пластин, как положительная, так и отрицательная, есть не что иное, как свинцовая решетка, заполненная активной массой. Активная масса имеет пористую структуру с тем, чтобы электролит заходил в как можно более глубокие слои и охватывал больший ее объем. Роль активной массы в отрицательных пластинах выполняет свинец, в положительных — перекись свинца.
Вес залитой АКБ ёмкостью 55 Ач составляет около 18 кг. Эта цифра складывается из массы электролита — 5кг (что соответствует 5,5 л), массы свинца и всех его соединений — 11 кг, а также 1,5 кг, приходящегося на долю бака и сепараторов.
Долговечность работы АКБ.
Средний срок службы современных АКБ при условии соблюдения правил эксплуатации составляет 4-5 лет.
Наиболее губительными для батарей являются глубокие разряды. Оставленные на ночь включенными световые приборы, либо другие потребители способны разрядить ее до плотности 1.12 — 1.15 г/см3, т.е. практически до воды, что приводит к главной беде аккумуляторов — сульфатации свинцовых пластин.
Пластины покрываются белым налетом, который постепенно кристаллизуется, после чего батарею практически невозможно восстановить. Отсюда вытекает главный вывод — необходимо постоянно следить за состоянием батареи, периодически замерять плотность электролита. Особенно актуально это в зимнее время. Следует отметить, что сульфатация в определенных пределах — явление нормальное и присутствует всегда.
Если же разряжать батарею длительное время, не давая ей «подпитки», то падение плотности ниже критического значения неизбежно приводит к образованию кристаллов сульфата свинца, не вступающих в реакцию ни при каких обстоятельствах.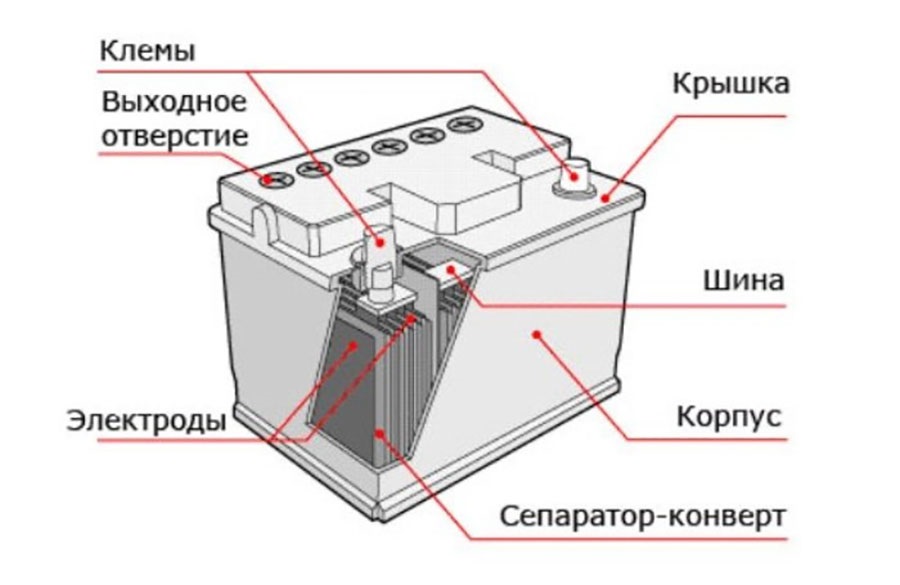 А это означает, что начался необратимый процесс сульфатации.
А это означает, что начался необратимый процесс сульфатации.
Опасен для батареи и перезаряд. Это происходит при неисправном регуляторе напряжения. При этом электролит начинает «кипеть» — происходит разложение воды на кислород и водород и понижение уровня электролита. Вот почему необходимо следить за зарядным напряжением. Естественно, это не составляет труда, если на панели приборов присутствует вольтметр. Если его нет?
В этом случае подключите тестер (в режиме вольтметра) между «+» и «массой» аккумуляторной батареи. Нормальный зарядный режим батареи обеспечивается в диапазоне 14,2±0.7В. В более древних авто напряжение в норме было порядка 14 В, в современных ближе к верхней границе 14,5…14,8 В. Если напряжение меньше, то стоит проверить натяжение ремня, надежность контактных соединений цепей системы электроснабжения. Если же это не помогает — неисправность нужно искать в регуляторе напряжения, а это уже другая история и не без участия электрика. Также вина ложится на регулятор, если напряжение превышает 14. 6…15 В.
6…15 В.
Рекомендации по эксплуатации
Оптимальным способом зарядки батареи, является ее заряд от бортовой сети автомобиля (естественно, при условии исправности последней).
При данном способе происходит постоянное перемешивание электролита и наиболее полное его проникновение во внутренние слои активной массы. Однако было бы ошибочным полагать, что заряд батареи начинается сразу же после пуска двигателя и продолжается все время, пока двигатель в работе. Исследования показывают, что батарея принимает заряд в сильной зависимости от прогрева электролита.
Именно этим и опасен довольно распространенный способ эксплуатации транспортных средств. Холодный запуск зимой с получасовым движением до работы, и затем редкие непродолжительные поездки на протяжении рабочего дня не дают прогреться электролиту и, следовательно, зарядиться Вашей батарее. Тем самым разряженность АКБ увеличивается изо дня в день и в итоге может привести к печальному результату.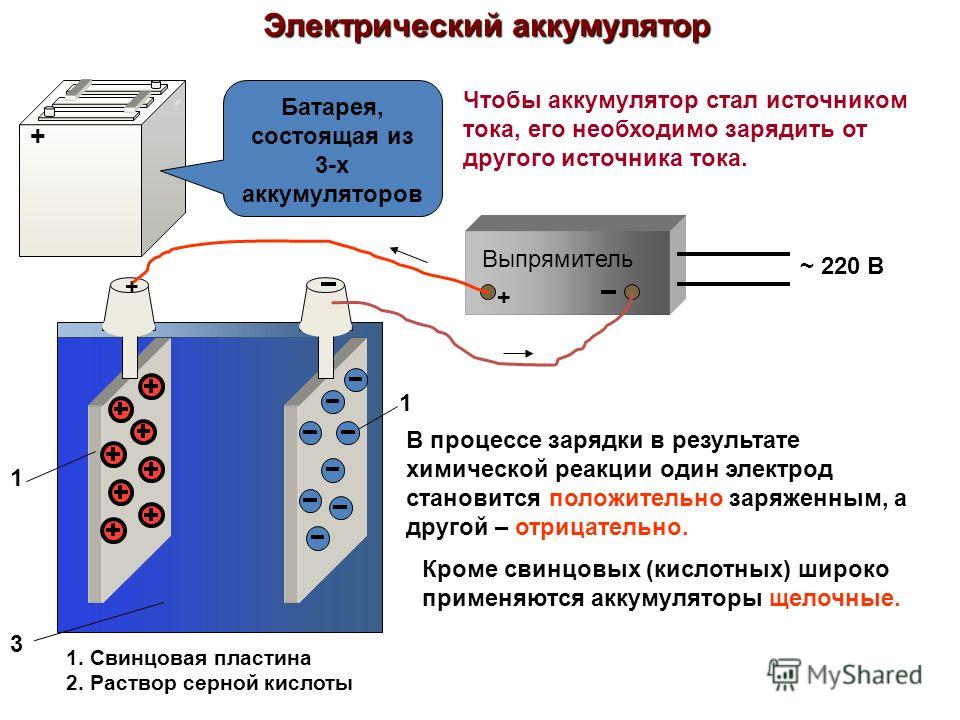
Физические процессы, происходящие при пуске двигателя, отличаются от процессов при разряде батареи потребителями. При пуске участвует не весь объем активной массы и электролита, а лишь та ее часть, которая находится на поверхности пластин и соприкасающийся с поверхностью пластин электролит. Поэтому, после неудачной попытки запустить двигатель, следует подождать некоторое время для того, чтобы электролит перемешался, плотность его выровнялась, он проник в поры активной массы. Нормальный запуск двигателя при однократном вращении стартера в течении 10с забирает ёмкость 300А х 10с = 3000 Ас = 0.83 Ач, что составляет около 1.5% от ёмкости аккумулятора.
При медленном же разряде участвуют не только поверхностные слои активной массы, но и глубинные, потому и разряд происходит более глубокий. Однако это не означает, что стартерные режимы не так губительны для батареи — стартером точно также можно разрядить батарею до критической величины.
Каковы же признаки выхода из строя батареи? Батарея не заряжается, плотность низкая и не повышается в процессе заряда. Большой саморазряд — батарея зарядилась, но не держит заряд. Можно попытаться потренировать батарею, однако если произошло осыпание активной массы пластин, либо кристаллизация сульфата свинца, то это уже не исправить.
Большой саморазряд — батарея зарядилась, но не держит заряд. Можно попытаться потренировать батарею, однако если произошло осыпание активной массы пластин, либо кристаллизация сульфата свинца, то это уже не исправить.
Вообще, освоить способ оценки степени возможной разрядки батареи от каких-либо действий (в том числе и осознанных) не составит большого труда. Необходимо усвоить несколько истин и запомнить несколько цифр.
1. Батарея начинает более-менее принимать заряд лишь только после прогрева электролита до положительной температуры (как вы понимаете, при температуре воздуха -20° С температура электролита в батарее хранящегося на свежем воздухе автомобиля будет примерно такой же).
2. Коэффициент полезного действия процесса зарядки составляет примерно 50%.
3. Каждый автомобильный генератор характеризуется следующими показателями:
ток отдачи генератора при работе двигателя на холостом ходу.
ток отдачи генератора при работе двигателя на номинальных оборотах.
Для многих автомобилей эти цифры имеют следующие значения:
Таблица 1
| Ток отдачи на холостом ходу | От 16 до 35 A |
| Ток отдачи на номинальных оборотах | От 42 до 85 А |
Очень важна величина потребления энергии автомобильными приборами:
Таблица 2
Потребитель | Ток, А |
| Зажигание | 2 |
| Габариты | 4 |
| Ближний свет | 9 |
| Дальний свет | 10 |
| Обогрев заднего стекла | 10-11 |
Вентилятор отопителя (печки):
| 5-7 10-11 |
| Cтеклоочистители | 3-5 |
| Магнитола | 5 |
| Итого: | 38-48 |
Таким образом, оставленные включенными габариты за три часа «съедят» 4А х 3ч= 12 Ач ёмкости батареи, что соответствует разряду приблизительно на 20%. Это не страшно для одного раза. Однако повторив это ещё раз, Вы уже рискуете не завести свою машину, особенно, если дело происходит зимой, т.к. разряд составит порядка 40% (тем более, что к тому же зимой батареи, как правило, эксплуатируются более разряженными).
Это не страшно для одного раза. Однако повторив это ещё раз, Вы уже рискуете не завести свою машину, особенно, если дело происходит зимой, т.к. разряд составит порядка 40% (тем более, что к тому же зимой батареи, как правило, эксплуатируются более разряженными).
Аналогично посчитаем, что Вы имеете при продолжительной работе двигателя на холостом ходу. Как уже показано выше, ток отдачи генератора автомобиля на холостом ходу, в среднем, составляет 24А. Вычитаем из этой величины 2А, необходимые для обслуживания системы зажигания. Остается 22А. Используя таблицу 2, нетрудно посчитать, чем стоит пожертвовать с тем, чтобы хоть немного осталось на зарядку АКБ.
Для владельцев иномарок с автоматической коробкой передач картина ещё более печальная. Обычно, стоя в пробке или на светофоре, мы не переключаемся на нейтральную передачу, а жмём ногой на тормоз. Это понижает обороты двигателя от стандартных 800-900 об./мин. до 600-700 об./мин., что, соответственно понизит ток генератора, а стоп-сигналы добавят ещё пару ампер потребления тока. Да и обогрев заднего стекла у немцев, например, существенно мощнее, чем у отечественных автомобилей.
Да и обогрев заднего стекла у немцев, например, существенно мощнее, чем у отечественных автомобилей.
Следует знать, что зимние условия эксплуатации автомобиля в принципе очень тяжелы для аккумуляторной батареи. Наверняка будут полезны следующие данные. Результаты исследований говорят о том, что при эксплуатации автомобиля в обычных и в то же время очень тяжелых, для АКБ, условиях (испытания в режиме эксплуатации «город-зима-ночь») аккумулятор получает порядка 1Ач в час. Следовательно, если, как в примере, приведенном выше, при запуске двигателя (зимой, при работе стартера 10 сек) расходуется 0,83 Ач энергии аккумулятора, то для восполнения этой энергии двигатель должен проработать, хотя бы 0,83*1=0,83 час=50 минут. Если же это время движения меньше, а плюс расход на дополнительные приборы отопления, обогрева, освещения и музыкального сопровождения, то получается, что Ваш АКБ хронически недозаряжается, чем неизбежно идёт к своей преждевременной кончине и обрекает Вас на риск остаться в одно прекрасное, морозное утро не у дел!!!
Терминология
Аккумуляторная батарея — один из основных элементов электрооборудования автомобиля, поскольку она накапливает и хранит электроэнергию, обеспечивает запуск двигателя в различных климатических условиях, а также питает электроприборы при неработающем двигателе.
Автомобильные свинцово-кислотные 12-вольтовые АКБ состоят из 6-ти последовательно соединенных элементов (банок), объединенных в общий корпус. Из каждой банки осуществляется газоотвод, конструкции могут существенно отличаться.
Электролит представляет собой раствор серной кислоты в дистиллированной воде (для средней полосы России плотностью 1.27-1.28 г/см3при t=+20°С). Кипение электролита — бурное выделение газа при электролитическом разложении воды с выделением кислорода и водорода. Это происходит во время заряда батареи.
Саморазряд — самопроизвольное снижение ёмкости АКБ при бездействии. Скорость саморазряда зависит от материала пластин, химических примесей в электролите, его плотности, от чистоты верхней части корпуса батареи и продолжительности ее эксплуатации.
Напряжение полностью заряженной аккумуляторной батареи без нагрузки (ЭДС — электродвижущая сила) должно находиться в пределах 12.6-12.9 В. Напряжение в бортовой сети автомобиля при работающем двигателе несколько выше, чем на клеммах АКБ, и должно находиться в пределах 13,8-14,8 В (0,2 В от крайних значений). Значение напряжения ниже 13.8 В ведет к недозаряду батареи, а выше 14.4В — к перезаряду, что пагубно сказывается на ее сроке службы.
Значение напряжения ниже 13.8 В ведет к недозаряду батареи, а выше 14.4В — к перезаряду, что пагубно сказывается на ее сроке службы.
Полярность аккумуляторной батареи — термин, определяющий расположение токосъемных выводов на ее корпусе. На зарубежных батареях полярность может быть прямой или обратной, т. е. ориентировка положительного и отрицательного выводов относительно корпуса может быть различной. По российскому стандарту (если смотреть со стороны выводов) отрицательный (-) должен располагаться справа, положительный (+) слева.
Емкость батареи — способность батареи принимать и отдавать энергию — измеряется в ампер-часах (Ач). Для оценки ёмкости батареи принята методика 20-ти часового разряда током 0.05С20 (т.е. током, равным 5% от номинальной ёмкости). Т.е., если ёмкость батареи 55Ач, то разряжая ее током 2.75 А, она полностью разрядится за 20 часов. Аналогично для батарей ёмкостью 60Ач полный 20-ти часовой разряд произойдет при чуть большем токе разряда — 3А.
Данная характеристика определяет возможность питать потребителей в экстремальной ситуации (при отказе генератора). Характеризуется объемом активной массы.
Значение тока холодного старта при -18°С (по DIN) — Величина тока, которую батарея способна отдать при пуске двигателя при температуре -18°С. Наиболее важная характеристика, напрямую сказывающаяся на пуске двигателя. Ведь при -20°С ток, потребляемый стартером, составляет порядка 300А. (Для пуска в летнее время горячего двигателя этот же показатель равен 100-120А.) Значение стартового тока определяется конструкцией батареи, пластин, сепараторов. Чем ниже внутреннее сопротивление батареи, тем выше стартовый ток, тем надежнее пуск двигателя при низких температурах.
Резервная ёмкость — время, в течении которого батарея сможет обеспечить работу потребителей в аварийном режиме. Величина резервной ёмкости, выраженная в минутах, последнее время все чаще проставляется изготовителями батарей после значения тока холодного старта.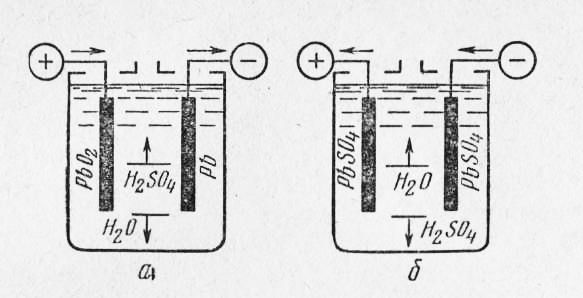
Корпус современных АКБ — изготавливается из пластмассы, в большинстве случаев полупрозрачной, позволяющей контролировать уровень электролита. Необслуживаемые батареи.
Сразу следует оговориться, что этот термин не должен пониматься буквально и восприниматься как руководство к бездействию. Это название говорит об улучшенных потребительских свойствах батареи. Необслуживаемые АКБ требуют долива воды не чаще одного раза в год при условии использования их на автомобилях с исправным электрооборудованием и среднегодовым пробегом 15-20 тыс. км. Встречаются конструкции, исключающие всякое вмешательство на всем протяжении срока службы, но они особенно критичны к состоянию автомобильного электрооборудования.
Большинство необслуживаемых батарей выпускаются заводами-изготовителями, залитыми электролитом. Так как эти батареи имеют значительно меньший саморазряд, они могут храниться от 6 месяцев до 1 года без подзаряда. Саморазряд новых необслуживаемых батарей за 12 месяцев может составить до 50% от номинальной ёмкости.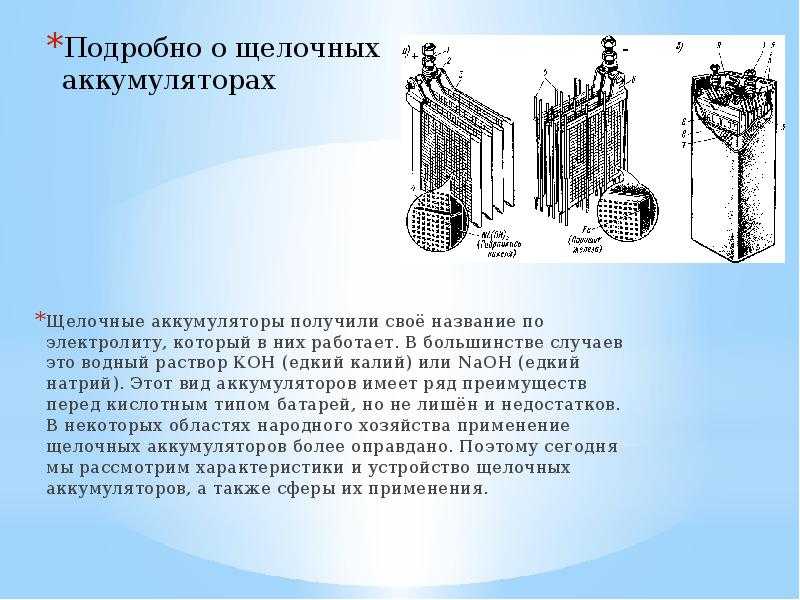
Выбор и покупка АКБ
Убедитесь, что выбираемая батарея соответствует конструктивным особенностям вашего автомобиля (ёмкость, место установки, способ крепления, полярность, форма и размер токосъемных выводов). Специализированные торговые фирмы имеют каталоги всего ассортимента, в которых систематизирована информация о модификациях и технических характеристиках.
Нецелесообразно на автомобиль с устаревшей системой электрооборудования устанавливать батарею, исключающую долив воды. Это приведет к сокращению ее срока службы или отказу. Емкость батареи не должна существенно отличаться от указанной заводом-изготовителем автомобиля. Несоблюдение этого условия приводит к резкому сокращению службы как батареи так и стартера.
Очень неплохо знать рекомендуемую величину пускового тока стартера для Вашего автомобиля. На многих автомобилях устанавливаются стартеры с редуктором. Это позволяет существенно уменьшить величину пускового тока в первые моменты запуска, особенно в сильные морозы, а значит существенно продлить жизнь Вашего аккумулятора.
Внимательно изучите текст гарантийного талона. Обратите особое внимание на те разделы, где перечислены: случаи, исключающие гарантийное обслуживание; адреса гарантийных мастерских; условия эксплуатации.
Маркировка аккумулятора должна иметь ссылку на стандарт (DIN, SAE, En или другие). В маркировке по стандарту SAE не указывается значение ёмкости в ампер-часах (Ач). Указание ёмкости в Ач в стандарте SAE – косвенный признак подделки. Наиболее подвержены подделкам дорогие аккумуляторы известных фирм-изготовителей, поэтому приобретать их лучше в торговых фирмах, заслуживающих доверие.
Большинство фирм-изготовителей кодирует дату выпуска АКБ. Современные необслуживаемые батареи допускают достаточно длительное хранение без существенной потери своих потребительских свойств, поэтому дата изготовления менее актуальна. Предпочтительнее приобретать залитый качественным заводским электролитом аккумулятор. Он готов к работе, легко поддается проверке. Не залитый сухозаряженный аккумулятор требует дополнительного времени и затрат на подготовку к эксплуатации.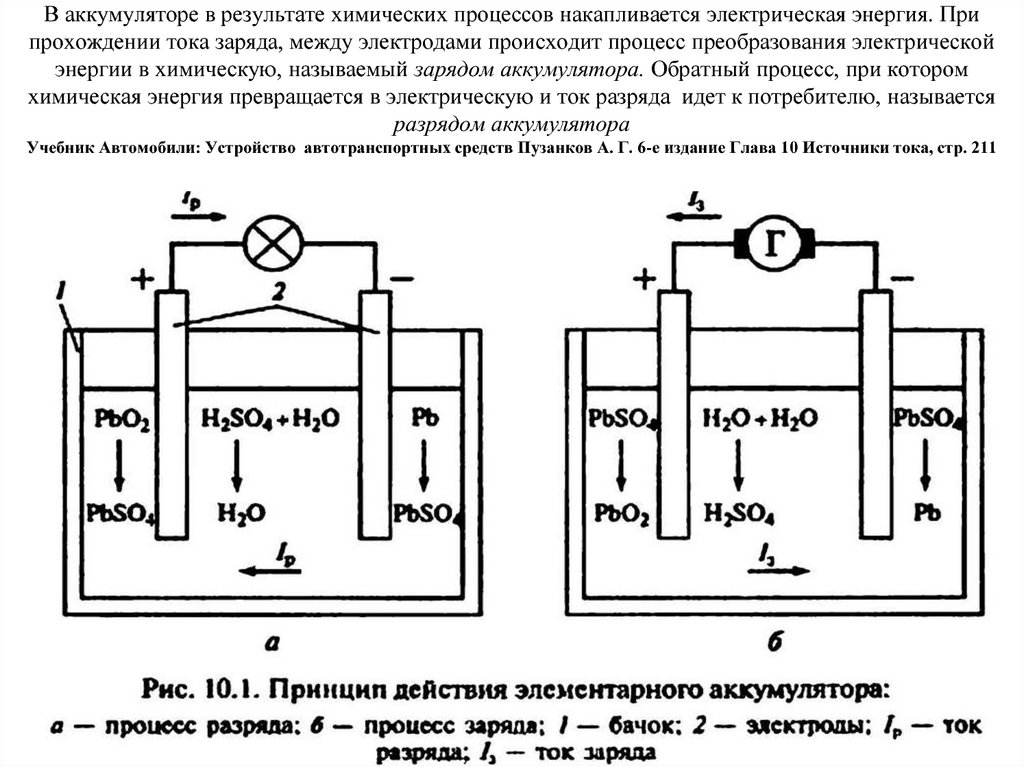
Не спешите отдать деньги! Вы вправе требовать проверки аккумулятора. Первым делом сдерите с него защитную упаковочную пленку, какой бы красивой она ни была, и убедитесь, что корпус не поврежден – такое случается довольно часто. Затем попросите продавца измерить плотность электролита – она не должна быть ниже номинальной более чем на 0,02 г/см3 и одинаковой во всех банках, что соответствует примерно 80-процентной заряженности батареи. Последнюю проверку следует провести с нагрузочной вилкой – ее вольтметр должен показать 12.5–12.9 В при отключенной нагрузке, а при включенной – не опускаться в течение 10 секунд ниже 11В.
В случае отклонения от этих значений, батарея может оказаться частично или полностью непригодной к эксплуатации. Если вам отказывают в проверке аккумулятора, не могут подтвердить качество товара сертификатом, гарантийным талоном, то лучше отказаться от покупки.
Установка АКБ
Перед установкой батареи обязательно полностью удалите с нее полиэтиленовую пленку. Газоотводные отверстия должны быть открытыми. Обратите внимание на правильность подключения. Клеммы АКБ рекомендуется зачистить и после закрепления смазать вазелином. Это делается для предохранения контактов от попадания влаги и окисления места контактов. Особенно это касается силовых проводов с медными (а не свинцовыми) наконечниками.
Газоотводные отверстия должны быть открытыми. Обратите внимание на правильность подключения. Клеммы АКБ рекомендуется зачистить и после закрепления смазать вазелином. Это делается для предохранения контактов от попадания влаги и окисления места контактов. Особенно это касается силовых проводов с медными (а не свинцовыми) наконечниками.
Очень важно уделить внимание проводам. Клеммы необходимо зачистить не только со стороны аккумулятора, но и с другой стороны. Место, куда крепится массовый провод (-) надо тоже тщательно зачистить от краски, масла и прочей грязи. Контакт затянуть туго. Это же касается клеммы на стартёре. Невнимание к проводам и контактам может очень сильно «выйти боком» зимой на морозе.
Обратите внимание, что на многих автомобилях батарея стоит довольно близко к выпускному коллектору. То есть летом ей будет довольно жарко, а это для батареи очень плохо! На «правильных» машинах предусмотрена термоизоляция АКБ от двигателя.
Рекомендации по эксплуатации и обслуживанию
Условия эксплуатации оказывают существенное влияние на срок службы аккумуляторной батареи. Частые запуски двигателя и поездки на короткие расстояния, неисправности электрооборудования (стартер, генератор, реле-регулятор), дополнительные потребители электроэнергии, несвоевременное обслуживание способны сильно сократить срок ее службы.
Частые запуски двигателя и поездки на короткие расстояния, неисправности электрооборудования (стартер, генератор, реле-регулятор), дополнительные потребители электроэнергии, несвоевременное обслуживание способны сильно сократить срок ее службы.
При продолжительном движении по трассе батарея может перезаряжаться (кипеть) — в городе с малыми пробегами и «пробками» она, как правило, разряжается (см. выше).
Генератор (при холостых оборотах двигателя) зимой не обеспечивает работу большинства штатных потребителей, не говоря о дополнительных. К включенным габаритным огням, ближнему свету фар, стоп-сигналам, указателям поворота, аудиоаппаратуре добавляются обогрев заднего стекла и вентилятор отопителя. Ежедневный недозаряд батареи постепенно уменьшает ее ёмкость, что в итоге приводит к невозможности запуска двигателя стартером.
Отказ аккумуляторной батареи может быть вызван и током утечки в электрооборудовании автомобиля. Это происходит, когда при отключении всех потребителей один или часть из них остается включенным в электрическую цепь (неисправны выключатель или реле).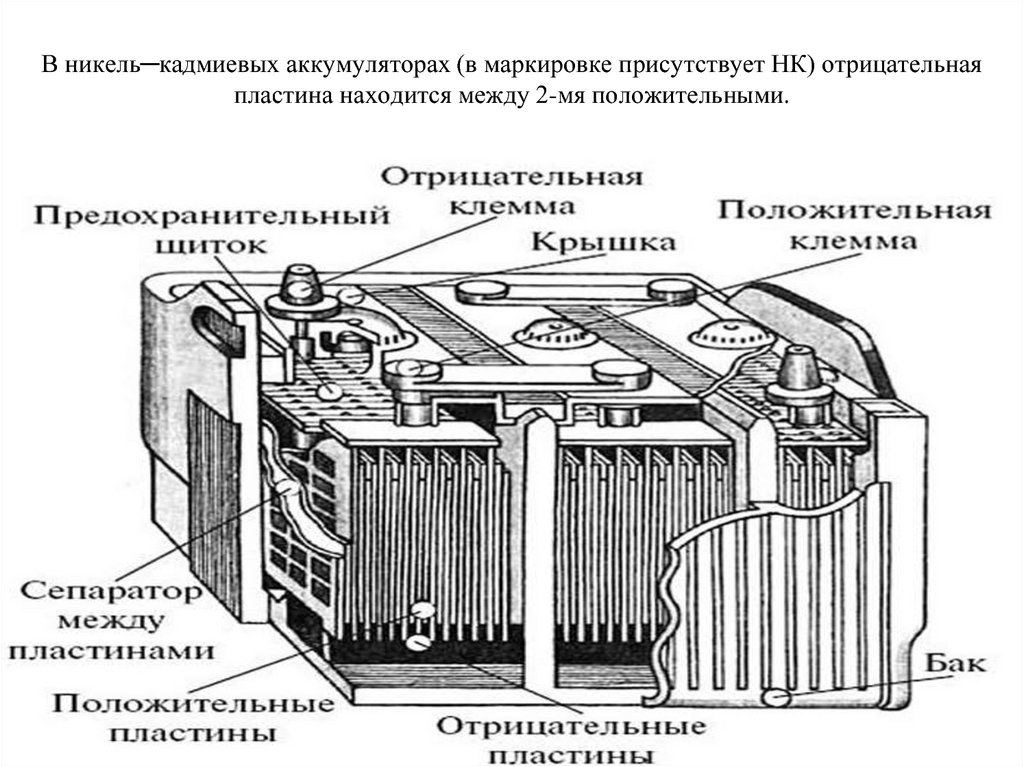 Виновником может быть и сигнализация. После глубокого разряда АКБ может не восстановить свою первоначальную номинальную ёмкость. Батарея не сможет нормально работать, если для запуска двигателя требуется продолжительное включение стартера (неисправны системы питания, зажигания).
Виновником может быть и сигнализация. После глубокого разряда АКБ может не восстановить свою первоначальную номинальную ёмкость. Батарея не сможет нормально работать, если для запуска двигателя требуется продолжительное включение стартера (неисправны системы питания, зажигания).
Обслуживание АКБ в процессе эксплуатации сводится к проверке и приведению в соответствие с требованиями: уровня и плотности электролита; чистоты и надежности крепления электрических соединений батареи с корпусом автомобиля, параметров электрооборудования автомобиля. Необходимо также очищать и смазывать выводы и клеммы, содержать батарею в чистоте. Протирайте верхнюю поверхность водным раствором питьевой соды. Доведение плотности электролита до требуемой производится путем заряда батареи от стационарного зарядного устройства. Значение зарядного тока в амперах (А) не должно превышать 1/10 ёмкости батареи (упрощенно).
Продление жизни новой батарее
Коротко об этом сказать трудно. В первую очередь, следует залить электролит, точно соответствующий не только климатической зоне, но и сезону эксплуатации. Если батарея будет работать только в теплое время года, то плотность электролита может быть 1.20 г/см3, а если до -15°С — 1.24 г/см3 и т.д. Такая точность, безусловно, снизит скорость сульфатации пластин, следовательно, увеличит долговечность батареи.
Если батарея будет работать только в теплое время года, то плотность электролита может быть 1.20 г/см3, а если до -15°С — 1.24 г/см3 и т.д. Такая точность, безусловно, снизит скорость сульфатации пластин, следовательно, увеличит долговечность батареи.
На срок службы АКБ значительно влияет средняя степень заряженности, которая зависит от исправности реле-регулятора. Необходимо, чтобы эта величина поддерживалась не ниже 75%. справка:
Установлено, что отклонение регулируемого напряжения на 10…12% вверх или вниз от оптимального сокращает срок службы батареи в 2…2.5 раза.
Во-первых, отрегулируйте двигатель так, чтобы он легко заводился с пол оборота. Это предохранит АКБ от глубокого разряда. При пуске двигателя стартером через аккумуляторную батарею проходит ток в несколько сот Ампер, что не способствует ее долговечности. Поэтому, чем легче пуск двигателя, тем лучше для АКБ: она прослужит дольше.
Cправка:
Сокращение времени работы стартера вдвое при шести-восьми ежедневных пусках повышает срок службы аккумуляторной батареи приблизительно в 1. 5 раза. Во-вторых, отрегулируйте при необходимости реле-регулятор, чтобы напряжение было в пределах 13.8…14.4В. Это одно из важнейших условий. В-третьих, никогда не позволяйте снизиться уровню электролита в банках ниже требуемого.
5 раза. Во-вторых, отрегулируйте при необходимости реле-регулятор, чтобы напряжение было в пределах 13.8…14.4В. Это одно из важнейших условий. В-третьих, никогда не позволяйте снизиться уровню электролита в банках ниже требуемого.
Cправка:
Падение (выкипание при высокой температуре воздуха) уровня дистиллированной воды может снизить срок службы батареи на 30%. Эти простые советы, продлят жизнь АКБ.
Особенности эксплуатации АКБ в зимний период
Первое! Проверить напряжение генератора при заведённом моторе, которое должно соответствовать 13.8…14.4В. Это питание АКБ, без которого ей не жить!!!
Второе! Обязательно провести ревизию всех силовых проводов, клемм и контактов. Клеммы зачистить мелкой шкуркой. Контакты на АКБ тоже зачистить и затянуть. Можно затем смазать литолом, чтобы к контактам не попадала влага.. С другой стороны силовых проводов так же провести ревизию контактов.
Третье! Замерим плотность электролита во всех банках без исключения. Норма 1.27-1.28 г/см3. У Вас далеко не так!? Значит, снимаем батарею и ставим на зарядку. Ни в коем случае не пытаемся повысить плотность электролита добавлением концентрированной кислоты, какая бы низкая не была его плотность. Желаемого же результата — повышения ёмкости батареи при этом не произойдет.
Норма 1.27-1.28 г/см3. У Вас далеко не так!? Значит, снимаем батарею и ставим на зарядку. Ни в коем случае не пытаемся повысить плотность электролита добавлением концентрированной кислоты, какая бы низкая не была его плотность. Желаемого же результата — повышения ёмкости батареи при этом не произойдет.
Прикуривание от другого автомобиля
Для российских автовладельцев нормальная ситуация, когда сосед просит «прикурить» его аккумулятор. Для этой нехитрой процедуры помимо автомобиля с заряженным аккумулятором, необходимы ещё и правильные провода. Те провода, что продаются на рынках имеют просто ужасное качество. Мало одного того, чтобы эти провода были медными и достаточно большого сечения. Необходимы очень качественные «крокодилы», обеспечивающие большую площадь контакта и большое усилие зажима, и необходим хороший контакт между проводом и «крокодилом». Не забываем, что по этим проводам у нас потечёт около 200 ампер!
Чтобы не навредить сложным электронным системам вашей собственной машины, эта, казалось бы, элементарная процедура требует соблюдения строгой последовательности действий.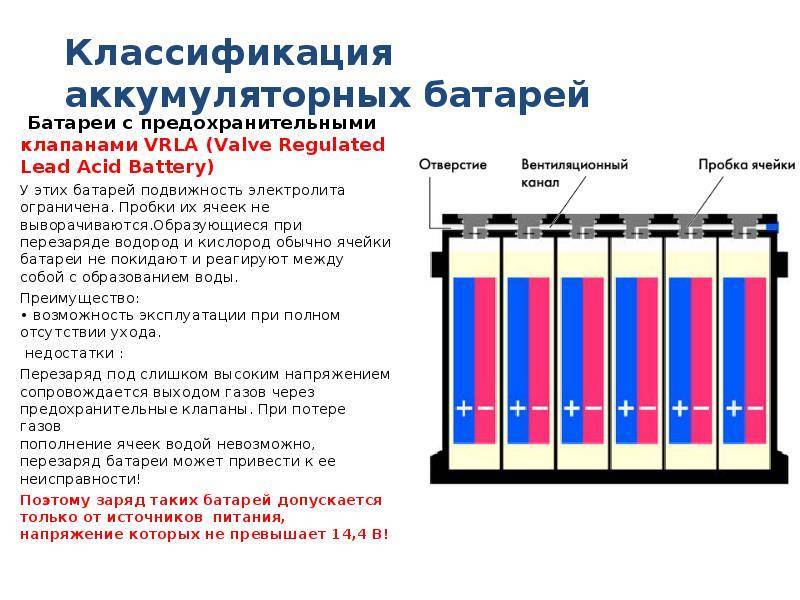
Соедините красный кабель с клеммой (+) на заряженном аккумуляторе.
Соедините другой конец красного кабеля с клеммой (+) на «севшем» аккумуляторе.
Соедините черный кабель с клеммой (-) на заряженном аккумуляторе.
Соедините другой конец черного кабеля с чистой точкой заземления на блоке двигателя или на шасси, главное — подальше от аккумулятора, карбюратора, топливных шлангов и т.п., прикуриваемого авто. В момент подсоединения будьте готовы к небольшой искре.
Следите, чтобы оба кабеля не касались движущихся деталей.
Запустите автомобиль с заряженным аккумулятором и дайте ему поработать не менее одной минуты.
Попробуйте запустить автомобиль с «севшим» аккумулятором. Если двигатель не заведется, подождите несколько минут и повторите попытку. Если же заведется, дайте ему поработать несколько минут в таком положении.
Выключите автомобиль с заряженным аккумулятором.
При отсоединении кабеля следуйте описанной выше процедуре в обратной последовательности.
Совет от Eugenijus K.Eugenijus K. :
На машине, от которой прикуривают (источник) надо врубить печку (вентилятор) на полный ход — и зимой, и летом. Дело в том, что индуктивный (реактивный) характер сопротивления работающего электродвигателя практически полностью гасит тот самый бросок (фронт) напряжения, который на машинах с «звенящей» проводкой (Авдотья 100, Субару Легаси до 1996-го и многие другие) может убить бортовой компьютер.
Особенности эксплуатации АКБ в летний период
Не удивляйтесь, если однажды вам будет трудно или вообще не завести машину в жаркую погоду. Теплое время года — такое же испытание, как и холод. Тепло ускоряет химические процессы. Неисправности и дефекты электрической системы автомобиля или аккумулятора незамедлительно скажутся на состоянии батареи. Но, скорее всего, узнаете вы об этом в самый неподходящий момент. Например, ночью во время дождя, когда придется включить освещение, вентиляцию и стеклоочистители. Поэтому не расслабляйтесь. Лето — самый подходящий период для покупки нового аккумулятора.
Поэтому не расслабляйтесь. Лето — самый подходящий период для покупки нового аккумулятора.
Летом автомобилист не сразу заметит, что в аккумуляторе плотность электролита и его уровень в банках недостаточные. Но чем выше температура окружающей среды, тем активнее электрохимические процессы. В результате электролиза кислород вступает во взаимодействие с пластинами, а ставший свободным водород испаряется. Таким образом из электролита исчезает вода. Как только уровень раствора оказывается ниже уровня пластин, начинается сульфатация пластин (сульфат свинца растворяется в электролите, а затем оседает на поверхности пластин уже в виде крупных нерастворимых кристаллов и происходит изоляция пластин от электролита). Емкость батареи уменьшается. Электрохимические реакции останавливаются. Аккумулятор выходит из строя.
Имейте в виду, что во время длительного хранения аккумулятора происходит саморазряд (снижение ёмкости). Оставлять батарею в разряженном состоянии не рекомендуется: в этом случае вода испаряется и открываются пластины.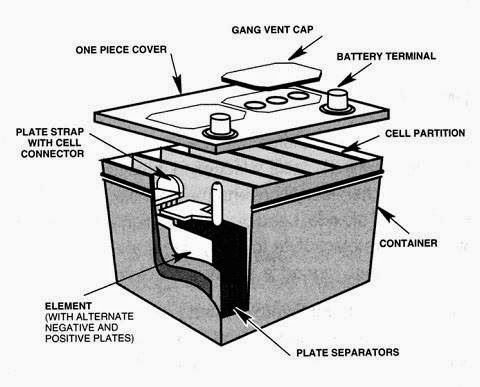 А дальше все, как описано выше.
А дальше все, как описано выше.
Саморазряд увеличивается от высокой температуры, грязи и электролита (воды) на крышке батареи. Еще одна причина возникновения паразитных токов — неодинаковая плотность электролита в разных банка
Вернуться назад
Что такое аккумуляторная батарея — устройство, состав и принцип работы АКБ
Содержание
- Определение АКБ и его функция в автомобиле
- Устройство аккумуляторной батареи и принцип ее работы
- По каким технологиям изготавливают
- Технология GEL
- Технология AGM
- Технология EFB
Основным источником электроэнергии в автомобиле является генератор – от него питаются все потребители при работающем двигателе. Но мотор сначала надо запустить. Для этого в машине установлена аккумуляторная батарея.
Определение АКБ и его функция в автомобиле
Аккумуляторная батарея (АКБ) – электрохимический возобновляемый источник электрической энергии. Он может снабжать потребителей до исчерпания заряда, после чего может быть перезаряжен. Количество циклов заряд-разряд ограничено, оно определяет жизненный ресурс батареи.
Количество циклов заряд-разряд ограничено, оно определяет жизненный ресурс батареи.
В автомобиле основное назначение АКБ — запуск двигателя. От аккумулятора запитывается стартерный двигатель, который приводит во вращение вал мотора, а также бензонасос (если он с электроприводом) и другие необходимые для старта узлы. После окончания последовательности пусковых операций на номинальный режим выйдет генератор, и вся нагрузка бортсети (включая возобновление потраченной на пуск энергии АКБ) перейдет на него.
Также аккумулятор может запитать потребителей, если двигатель не запущен. В штатном режиме это может быть аварийное светосигнальное оборудование, охранная сигнализация, в темное время суток – габаритные фонари и т.п. В нештатной ситуации могут быть обеспечены питанием и другие потребители — автозвук, световое оборудование при ремонте и диагностике и т.п. Надо лишь помнить, что время пользования до следующего заряда ограничено.
Устройство аккумуляторной батареи и принцип ее работы
Самый простой аккумулятор состоит из двух электродов – положительного из оксида свинца, отрицательного из свинца. Оба электрода помещены в раствор серной кислоты. При подключении потребителя начинают протекать химические реакции.
Оба электрода помещены в раствор серной кислоты. При подключении потребителя начинают протекать химические реакции.
Всего их при заряде-разряде несколько десятков, но для понимания работы АКБ наиболее важны следующие:
- при разряде на аноде (плюсовом электроде) диоксид свинца при взаимодействии с серной кислотой восстанавливается до сульфата свинца с образованием воды;
- при этом на катоде (минусовом электроде) свинец окисляется с образованием сульфата свинца (PbSO4).
В итоге происходит два важных для эксплуатации явления:
- Содержание серной кислоты в электролите падает (уменьшается плотность электролита).
- На пластинах выпадает плохо растворимый в кислоте осадок сульфата свинца.
При заряде реакции идут в обратном направлении:
- на катоде в результате реакции из сульфата свинца образуется свинец и кислотный остаток серной кислоты, катод заряжается отрицательным потенциалом;
- на аноде сульфат свинца с водой образуют серную кислоту и чистый свинец, заряжая электрод положительно.
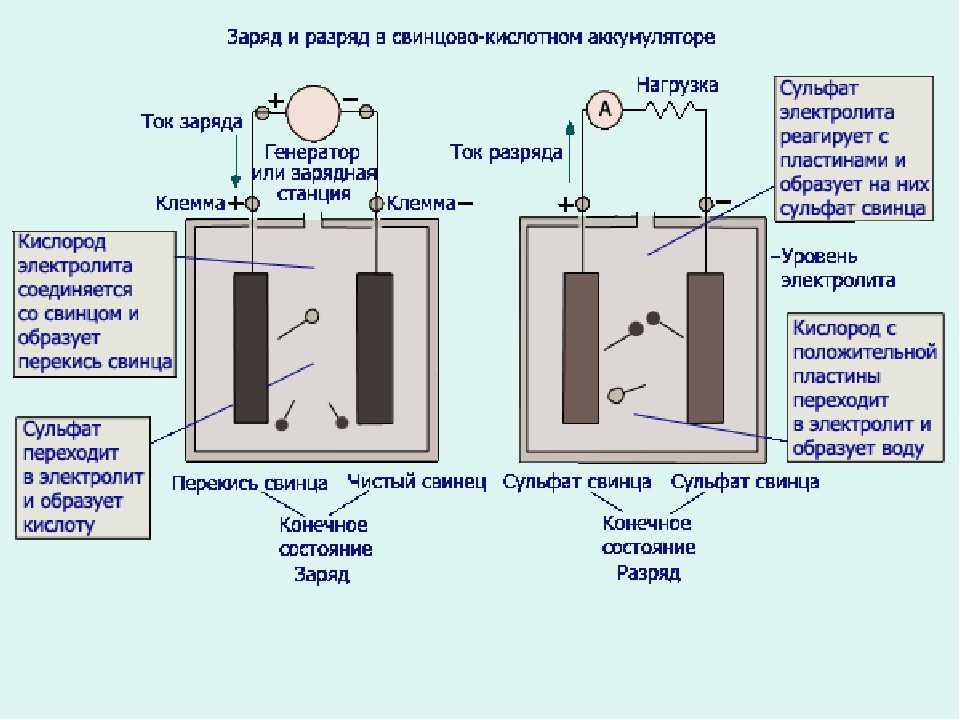
Итогом реакций становится:
- Растворение сульфата свинца.
- Увеличение содержания серной кислоты и повышение плотности электролита.
- Появление электродвижущей силы (ЭДС), достигающей 2,1 вольта.
Если процессы протекают строго симметрично, то выпадающий осадок PbSO4 полностью растворяется. На практике такого не бывает, полное равновесие соблюсти сложно. Поэтому пластины постепенно покрываются слоем сульфата, маскирующим полезную площадь. В итоге емкость АКБ снижается. Этот процесс называется сульфатацией.
Пластины, покрытые слоем кристаллов сульфата свинца.Последствия «кипения» аккумулятора – выплескивание электролита и образование осадка при высыхании.В практических конструкциях изначально свинцовые решетчатые пластины заполняют намазкой из смеси оксида свинца и свинцового сурика (с химической точки зрения — соединение свинца и кислорода). При первом заряде происходит формовка пластин. Во время реакции с серной кислотой на одном аноде образуется оксид свинца в губчатом виде, на другом – металлический свинец (также в пористой форме). Емкость аккумулятора зависит от площади пластин, поэтому практическое устройство элемента аккумуляторной батареи выглядит как пакет из анодных и катодных пластин, набранных поочередно и соедиенных параллельно.
Емкость аккумулятора зависит от площади пластин, поэтому практическое устройство элемента аккумуляторной батареи выглядит как пакет из анодных и катодных пластин, набранных поочередно и соедиенных параллельно.
По каким технологиям изготавливают
Стремление улучшить работу свинцово-кислотных аккумуляторов привело к созданию новых технологий производства элементов. В первую очередь, это замена легирующей добавки. Вместо сурьмы сейчас широко применяется кальций. Его добавка придает свинцовым пластинам повышенную прочность, в результате появилась возможность сделать их более тонкими без потери жесткости конструкции. В электрохимических реакциях кальций не участвует. Кальциевые батареи имеют и другое достоинство – пониженная склонность к газообразованию при зарядке. Такой аккумулятор не склонен к «кипению». Это кардинально снижает расход воды во время эксплуатации. Также за последние годы популярность завоевали батареи в необслуживаемом исполнении.
Тематическое видео: Революционная твердотельная батарея от Toyota
Технология GEL
В этих аккумуляторах электролит загущен до состояния геля специальными добавками. Главное достоинство батареи – необслуживаемое исполнение и практическая невозможность пролива электролита. Даже при небольших повреждениях корпуса гель не вытечет. Также созданы условия для рекомбинации газов в толще электролита. Водород и кислород, даже если они образуются при зарядке, не улетучиваются, а реагируют в толще геля с образованием воды. Малая часть газов, не поучаствовавшая в рекомбинации, улетучивается в пространство над электролитом. Когда давление достигает определенного предела, оно сбрасывается в атмосферу через специальный клапан. Другим плюсом является возможность эксплуатации почти в любом положении. Электрохимические реакции в таком элементе не отличаются от реакций в обычном аккумуляторе, принцип работы гелевой батареи абсолютно такой же, поэтому ЭДС одного элемента составляет те же 2,1 вольта.
Другим плюсом является возможность эксплуатации почти в любом положении. Электрохимические реакции в таком элементе не отличаются от реакций в обычном аккумуляторе, принцип работы гелевой батареи абсолютно такой же, поэтому ЭДС одного элемента составляет те же 2,1 вольта.
Читайте также
Типы автомобильных аккумуляторов и их обозначение
Главный минус АКБ с загущенным электролитом – пониженная динамика электрохимических реакций. Результатом этого становится пониженная токоотдача, которая не позволяет применять гелевые АКБ в качестве автомобильных стартерных. Зато такие батареи используют в качестве тяговых аккумуляторов, буферных элементов и в качестве источников питания, не требующих сервиса, на удаленных объектах (устройства телемеханики, ретрансляторы связи и т.п).
Необслуживаемый гелевый аккумулятор.Более подробно в статье: Гелевый аккумулятор для автомобиля — плюсы и минусы
Технология AGM
Эта технология позволяет в полной мере использовать преимущества пластин, легированных кальцием. Тонкие пластины собирают в компактный пакет, а чтобы избежать короткого замыкания, между ними прокладывают сепаратор-разделитель, как показано на рисунке в разрезе.
Тонкие пластины собирают в компактный пакет, а чтобы избежать короткого замыкания, между ними прокладывают сепаратор-разделитель, как показано на рисунке в разрезе.
Он изготовлен из волокнистого материала (обычно, стекловолокна). Пространство между волокнами заполнено электролитом, который удерживается внутри сепаратора капиллярными силами, поэтому свободной жидкости в такой батарее тоже нет. Часть межволоконного пространства оставлена незаполненным – небольшое количество газов, которое все же образуется во время эксплуатации, рекомбинирует в этих пустотах.
Технология EFB
Строение аккумуляторов, изготовленных по данной технологии, является промежуточным между традиционными батареями и AGM. Пластины (обычно, каждая положительная) такой АКБ помещены в сетчатый сепаратор, который позволяет расположить электроды более компактно без риска короткого замыкания. Внутри корпуса находится электролит в свободном виде, но часть его абсорбируется сеткой разделителя, которая позволяет держать пластины постоянно смоченными раствором серной кислоты.
Кроме того, сепаратор снижает вымывание обмазки пластин и удерживает ее от осыпания, что положительно сказывается на сроке службы АКБ, увеличивая количество возможных циклов. Такие батареи обладают многими достоинствами аккумуляторов AGM, но их производство значительно дешевле.
Устройство аккумулятора EFB.Несмотря на развитие литий-ионных технологий, кислотно-свинцовые батареи еще долго будут занимать свои ниши в сфере автономных источников питания. Предпосылками к этому служат их дешевизна, конструкция, отработанная десятилетиями, относительно долгий срок службы при эксплуатации в соответствующих условиях.
Что такое электролит в батарее? (Принцип работы и типы аккумуляторов)
От высокотехнологичного электромобиля до дешевой игрушечной машинки с дистанционным управлением питание аккумуляторов стало неотъемлемой частью нашей повседневной жизни. На протяжении многих лет мир использовал дорогие источники энергии для выполнения повседневных задач.
Однако, после достаточного количества разработок, батареи оказались эффективным изобретением в качестве источника и хранения электроэнергии. Внутренний электролит в аккумуляторе является одним из основных компонентов, которые делают все волшебство.
Внутренний электролит в аккумуляторе является одним из основных компонентов, которые делают все волшебство.
В сегодняшнем посте мы обсудим, что такое электролит в аккумуляторе и как его сделать в домашних условиях.
Содержание
- Что такое электролит в батарее?
- Как электролиты работают в батарее?
- Из чего состоит электролит батареи?
- Общие типы батарей с их электролитами
- Как сделать раствор электролита для батареи?
- Резюме
Что такое электролит в батарее?
Электролит в батарее представляет собой вещество, которое дает ионы (электрически заряженные атомы, которые приобрели или потеряли электроны) при растворении в воде или жидкостях. Благодаря движению положительных и отрицательных ионов раствор проводит электрический ток, который течет между двумя электродами — анодом и катодом.
Электролит батареи может быть жидким или твердым, в зависимости от типа батареи. Однако потенциальными электролитами могут быть любые среды, содержащие ионы.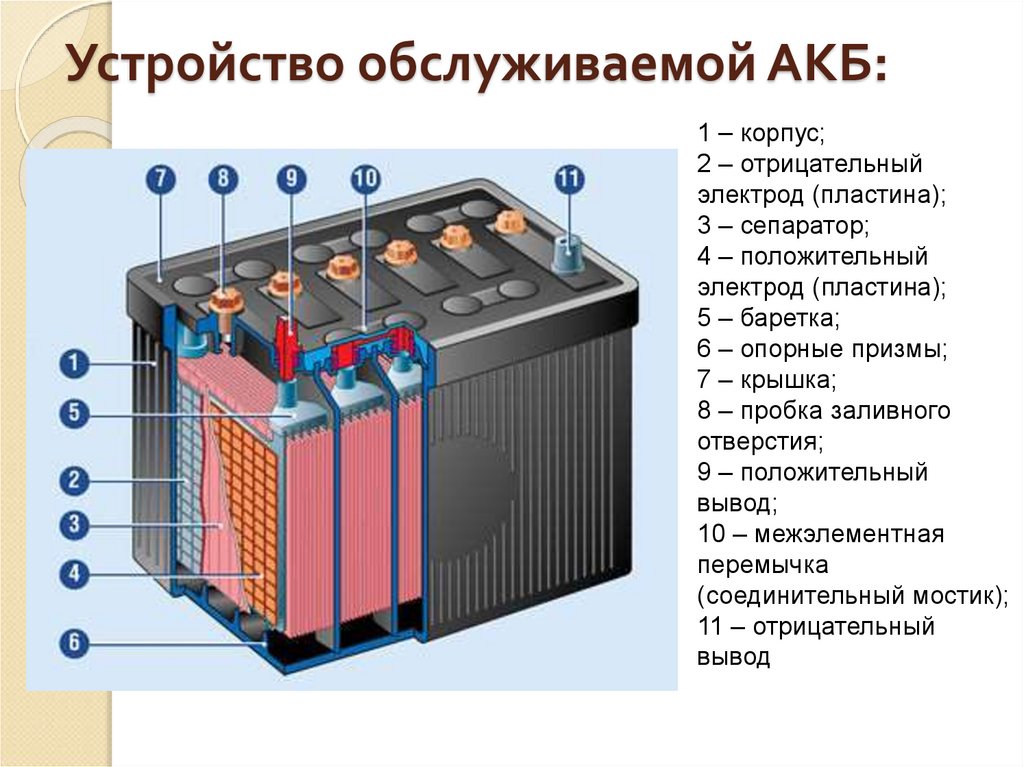
Электролиты можно разделить на сильные и слабые химические соединения. Сильные электролиты — это те, которые почти или полностью ионизируются в растворе, а слабые — частично.
Как электролиты работают в батарее?
Чтобы понять, как работает электролит батареи, нам сначала нужно изучить основные компоненты батареи — анод, катод и электролит (который разделяет две клеммы). Поскольку мы уже обсуждали электролит выше, давайте рассмотрим анод и катод.
Анод – это отрицательная клемма или восстановительный электрод, который окисляет и высвобождает электроны во внешнюю цепь во время электрохимической реакции.
С другой стороны, катод – это положительный вывод или окислительный электрод. Он восстанавливается в ходе электрохимической реакции, приобретая электроны, выделяемые анодом во внешнюю цепь.
Электролит обеспечивает среду для перемещения электрического заряда в виде ионов между двумя клеммами. Катионы с положительным зарядом движутся к катоду, а анионы с отрицательным зарядом — к аноду.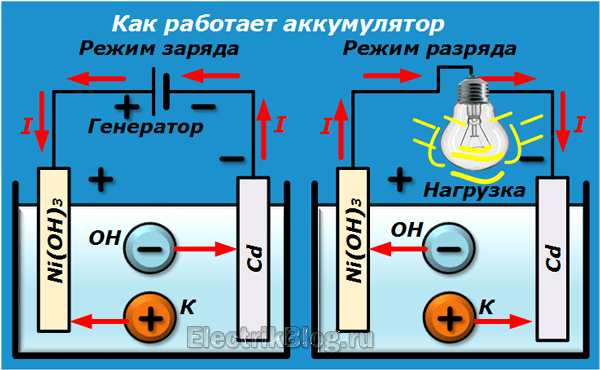 Кроме того, электролит приводит подходящее химическое вещество, необходимое для реакции, в контакт с клеммами, что преобразует накопленную энергию в пригодную для использования электрическую энергию.
Кроме того, электролит приводит подходящее химическое вещество, необходимое для реакции, в контакт с клеммами, что преобразует накопленную энергию в пригодную для использования электрическую энергию.
Полезная электрическая энергия встречается с подключенным устройством, будь то лампочка или пылесос, и питает его.
Из чего состоит электролит батареи?
Электролит батареи состоит из растворимых солей, кислот или оснований. Однако точный характер электролита зависит от типа батареи и требуемой величины тока.
Например, в обычных щелочных бытовых батареях используется гидроксид калия, который является сильным электролитом и поэтому обладает высокой электропроводностью. С другой стороны, свинцово-кислотный аккумулятор в автомобилях использует серную кислоту в качестве электролита и вызывает требуемую реакцию.
Давайте рассмотрим некоторые типы аккумуляторов с подходящими для них электролитами.
Распространенные типы батарей с их электролитами
1.
 Свинцово-кислотные
Свинцово-кислотныеСвинцово-кислотные аккумуляторы — это аккумуляторы, в которых для химических реакций используется кислый электролит (серная кислота) и металлический свинец (Pb). Серная кислота — очень коррозионное вещество, растворимое в воде. Он бесцветный, с легким желто-зеленым оттенком. Однако он обесцвечивается до коричневатого оттенка из-за ржавчины в результате анодной коррозии, возникающей при растворении анода в электролите.
Для контролируемой химической реакции металлический свинец погружается в серную кислоту, в результате чего батарея вырабатывает электричество. Этот химический процесс извлечения тока из свинцово-кислотного аккумулятора известен как разрядка.
Кроме того, когда аккумулятору необходимо перезарядиться, реагенты (ранее использовавшиеся для выработки электроэнергии) можно регенерировать, пропуская ток через аккумулятор извне. Этот процесс известен как перезарядка.
Свинцово-кислотная батарея имеет большой вес, но вырабатывает высокое напряжение.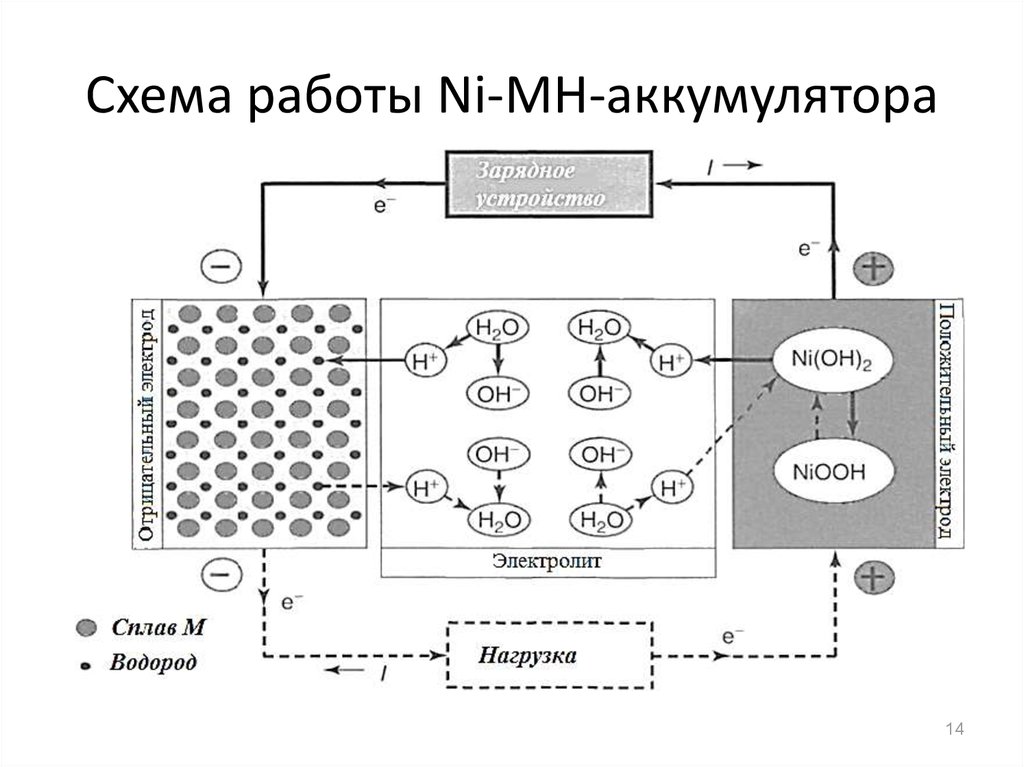 Он оснащен ячейками 2 В, что означает, что он имеет четное количество вольт. Наиболее распространенные свинцово-кислотные батареи имеют напряжение 2 В, 6 В, 12 В и 24 В.
Он оснащен ячейками 2 В, что означает, что он имеет четное количество вольт. Наиболее распространенные свинцово-кислотные батареи имеют напряжение 2 В, 6 В, 12 В и 24 В.
Поэтому он обычно используется в машинах, ИБП (источниках бесперебойного питания) и системах, которые требуют высокой мощности для работы и не имеют значения веса батареи.
2. Никель-кадмиевые (NiCd)
Электролит, используемый в никель-кадмиевых (NiCd) батареях, представляет собой тридцатипроцентный раствор гидроксида калия (КОН) в дистиллированной воде. При комнатной температуре его удельный вес остается между 1,240 и 1,300.
По сравнению со свинцово-кислотными батареями никель-кадмиевые батареи дороже, но имеют более высокую плотность энергии, что означает, что они могут хранить больше энергии на единицу веса. Он также служит дольше, чем свинцово-кислотные аккумуляторы, поскольку у него больше жизненных циклов, около 2000-2500.
3. Никель-металл-гидридный (NiMH)
Никель-металл-гидридный (NiMH) аккумулятор использует тот же электролит, что и NiCd, а именно гидроксид калия.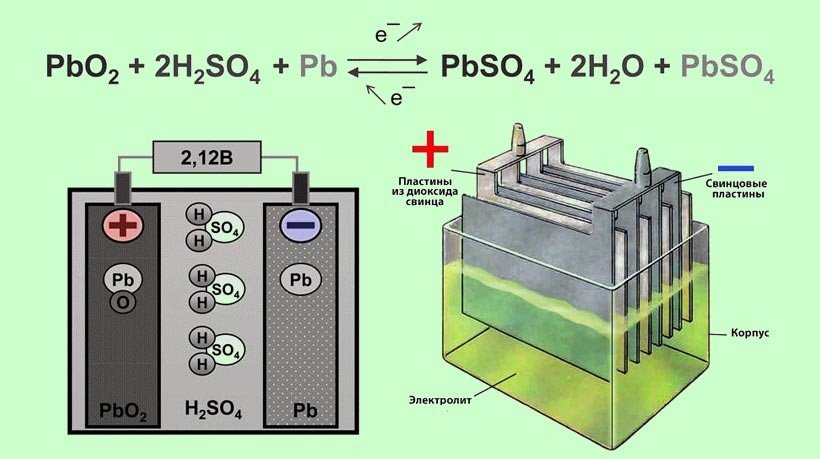 Гидроксид калия, также известный как едкий калий, представляет собой неорганическое соединение и сильное основание, широко используемое в большинстве мягких и жидких мыл. Электролит бесцветен и имеет множество промышленных применений.
Гидроксид калия, также известный как едкий калий, представляет собой неорганическое соединение и сильное основание, широко используемое в большинстве мягких и жидких мыл. Электролит бесцветен и имеет множество промышленных применений.
Батарея содержит электроды, изготовленные из уникальных металлов, таких как никель, кобальт, марганец и алюминий, которые также присутствуют в литий-ионных батареях. Однако батарея NiMH более хрупкая, чем литий-ионная и никель-кадмиевая.
4. Литий-ионные (Li-ion)
В литий-ионных (Li-ion) батареях используются электролиты, состоящие из солей лития, таких как гексафторфосфат лития (LiPF6) в органическом растворителе. Литий-ионные аккумуляторы работают как с гелевым или сухим полимером, так и с жидким электролитом.
Элементы литий-ионных аккумуляторов легкие и обладают высокой плотностью энергии, что дает им преимущество перед любыми аккумуляторными элементами. Они способны генерировать мощность 3,6 В, что делает их полезными в широком диапазоне приложений, таких как транспортные средства, силовое оборудование и портативные устройства, такие как ноутбуки и сотовые телефоны.
Как сделать раствор электролита для аккумулятора?
Когда в вашей жидкостной батарее заканчивается топливо (электролит), вы можете сделать его дома, а не покупать.
Хотя для приготовления раствора электролита требуются некоторые школьные знания химии, вы все равно можете сделать его, следуя этому руководству. Однако действовать нужно осторожно, так как процесс приготовления электролита опасен.
Прежде чем начать, решите, какой химический раствор вы хотите использовать для приготовления электролита. Обычно для аккумуляторов больше всего подходят сильные кислоты, растворенные в чистой смеси воды. Вода помогает стабилизировать активность ионов водорода. Вы можете использовать серную кислоту, если у вас есть свинцовые электроды, и азотную кислоту для никелевых электродов.
Примечание. Без состава чистой воды небольшой ток может взорвать аккумулятор.
Инструменты, которые вам понадобятся
Помимо вышеперечисленных химикатов, для эффективного выполнения процесса вам потребуется следующее оборудование.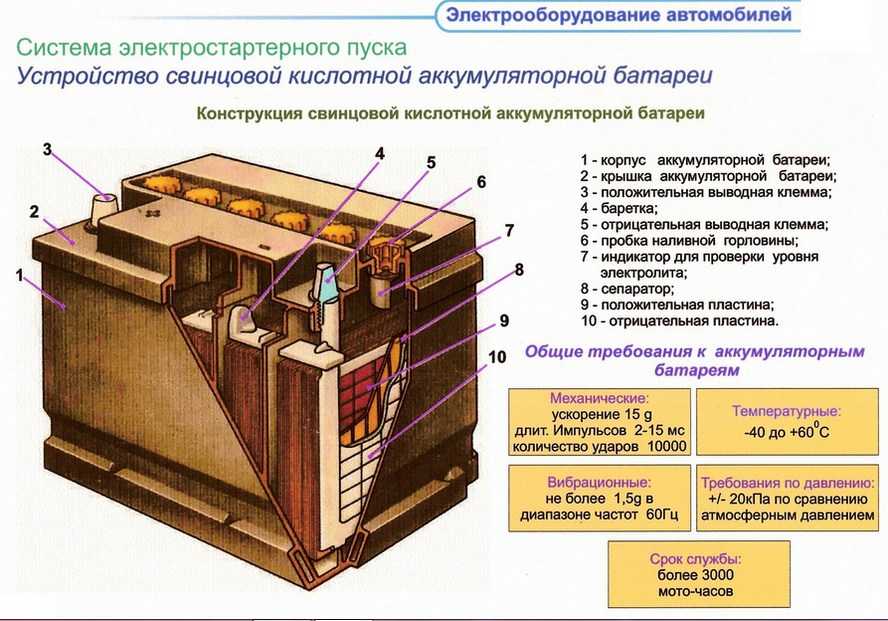
- Не менее трех толстых изолирующих контейнеров
- Кислотостойкие перчатки
- Очки
- Захват
- Мультиметр
- Ареометр
- Чертежные трубы (желательно прозрачные)
- Аптечка с пищевой содой для лечения кислотных ожогов
Шаги
Все собралось? Если да, то следуйте следующим шагам!
- Возьмите изолированный контейнер и наполните его водой. Обязательно измерьте объем, прежде чем наливать его. Вы также можете оставить немного воды в другом контейнере, если вам нужно разбавить раствор. В любом случае используйте чистую воду, чтобы исключить риск загрязнения, которое может вызвать нежелательные химические реакции.
- Затем осторожно возьмите контейнер с кислотой с помощью захвата и вылейте его в воду. Если на поверхности появляются чрезмерные пузырьки, приостановите процесс на несколько секунд и дайте им рассеяться. Вы можете вылить остальную кислоту, как только исчезнут пузырьки.

- В этот момент раствор электролита должен иметь высокую температуру. Таким образом, вы можете накрыть его, чтобы позволить любым загрязнениям иметь место. Однако убедитесь, что горячий воздух выходит.
- Когда раствор в контейнере остынет, используйте ареометр, чтобы проверить его крепость и добавить жидкости по мере необходимости.
- Как только вы наберете необходимую силу, аккуратно залейте кислотный раствор в гнезда батареи. Для этого вы можете использовать волочильные трубы, один конец которых находится на дне контейнера, а другой — в батарейном отсеке.
- Надев кислотостойкие перчатки, наклоняйте контейнер под постепенно увеличивающимся углом, чтобы раствор кислоты попал в гнездо для батареи. Заполните каждый аккумуляторный отсек примерно на три четверти.
- Когда слоты заполнены, снимите трубу и закройте слоты. Вот и все! Ваша батарея готова генерировать энергию.
Наконец, используйте мультиметр, чтобы проверить, какое напряжение выдает ваша батарея на клеммах.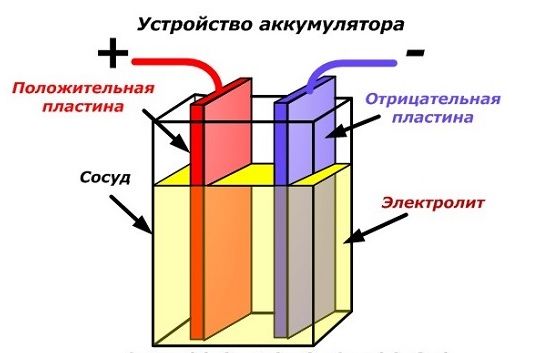 Будем надеяться, что батарея в порядке!
Будем надеяться, что батарея в порядке!
Резюме
Электролит в батарее представляет собой раствор, который позволяет заряженным ионам и току проходить через катодные и анодные клеммы. Электролит имеет определенные химические характеристики, которые реагируют с электродами, и реакция преобразует накопленную энергию в пригодную для использования электрическую энергию.
Электролиты обычно состоят из растворов сильных кислот, таких как серная и азотная кислота, но обычно электролит может состоять из растворимых солей, кислот и оснований.
Мы надеемся, что этот пост был вам полезен. Если вы сегодня узнали что-то новое, не забудьте поделиться этим с друзьями!
Принцип работы литий-ионного аккумулятора — E-Lyte Innovations GmbH
Литий-ионные батареи относятся к группе батарей, которые генерируют электрическую энергию путем преобразования химической энергии посредством окислительно-восстановительных реакций на активных материалах, т.
В обычных литий-ионных батареях ионы Li + перемещаются между положительным электродом (обычно из слоистого оксида переходного металла) и отрицательным электродом на основе графита по принципу «кресла-качалки» (см. видео) .
Термин «разрядка» используется для обозначения процесса, при котором батарея подает электрическую энергию на внешнюю нагрузку. Электролит в этой системе содержит дополнительные ионы Li + для обеспечения быстрого переноса ионного заряда внутри элемента.
Помимо ионной проводимости, электролит выполняет другие важные функции:
Поддержка образования эффективных межфазных фаз (например, межфазных границ твердого электролита, SEI или межфазных фаз катодного электролита, CEI), которые:
Способствуют безопасности клеток – будучи инертными по отношению к другим материалам, таким как:
- Сепаратор
- Токосъемники
- Проводящие добавки, связующие
- Корпус ячейки
Шаг 1 — Исходное состояние (состояние заряда (SOC) 0%)
При разряде ионы Li + — находятся в материале положительного электрода.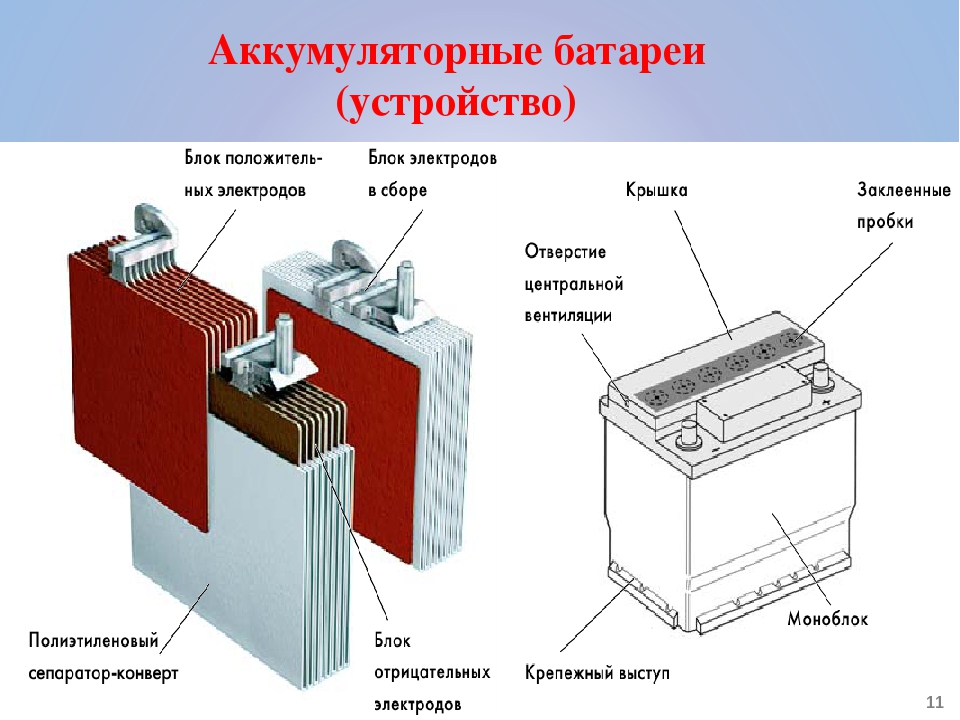 Таким образом, положительный электрод является источником ионов Li
Таким образом, положительный электрод является источником ионов Li
Шаг 2 — Формирование SEI и CEI
В самом начале первого процесса зарядки электроны мигрируют из материала положительного электрода (окисление) через внешний проводник в материал отрицательного электрода (восстановление). Для обеспечения зарядовой нейтральности Li + -ионы деинтеркалируют из материала положительного электрода в электролит и мигрируют через электролит в материал отрицательного электрода для последующего хранения. В результате этих реакций на границах раздела электролит/поверхность отрицательного электрода и электролит/положительный электрод соответственно образуются граничные фазы, так называемые SEI и CEI.
Этап 3. Электродные реакции
После формирования SEI и CEI далее Li 9Ионы 0161 + деинтеркалируют из материала положительного электрода в электролит и мигрируют через него в материал отрицательного электрода для последующего включения в последний.
Положительный электрод:
LI M O 2 → LI (1- x ) M O  +
+
Отрицательный электрод:
C 6 + x · E — + x · LI + → LI x C 6 903 C 6
C 6 C 6 9000 3 C 6 9000 3 C 6 9000 C 6 9000 C 6 9000 . O 2 → Li x C 6 + Li (1- x ) MO 2Шаг 4 — Изменение цвета при интеркаляции/деинтеркаляции в графит
В зависимости от количества ионов Li + , встроенных в отрицательный электрод (в зависимости от состояния заряда, SOC), он меняет цвет с черного на красный (ранний SOC) на золотой (100% SOC).
Шаг 5.
 Выписка
ВыпискаПри разряде происходят обратные реакции. Электродные реакции:
Положительный электрод = «катод» (восстановление)
Li (1- x ) M O 2 + x ·e – + x ·Li + → Li M O 2
Negative Электрод = «анод» (окисление)
LI x C 6 → C 6
Шаг 6 — Принцип кресла-качалки
После разряда (SOC 0%) ионы Li + восстанавливаются в материале положительного электрода, из которого они изначально были получены. Возвратно-поступательное движение Li + -ионов напоминает движение кресла-качалки, поэтому этот принцип получил название «принцип кресла-качалки».
Особенно первый цикл (зарядка и разрядка) связан с необратимой потерей ионов Li + в SEI и CEI, а также в материале отрицательного электрода. В результате меньше Li + -ионы теперь могут накапливаться в отрицательном электроде в следующем цикле заряда, что приводит к уменьшению емкости батареи.
В литий-ионном аккумуляторе происходят различные процессы старения, которые снижают производительность аккумулятора в течение периода использования и сильно зависят от химического состава элемента и предполагаемого использования аккумулятора. В частности, правильный выбор электролита оказывает огромное влияние на эти механизмы старения и еще раз подчеркивает важность электролитов, изготовленных по индивидуальному заказу.
Для оптимизации литий-ионных аккумуляторов в отношении удельной энергии и плотности энергии, срока службы и безопасности было предпринято много усилий для дальнейшего расширения возможностей применения ЛИА. В частности, растущие потребности в литий-ионных батареях с высокой удельной энергией и плотностью энергии, особенно для автомобильных приложений, стимулируют исследовательские усилия во всем мире. Плотность энергии и удельная энергия аккумуляторов по определению — это количество энергии, запасенной в данной системе на единицу объема и на единицу массы соответственно. Произведение удельной емкости на среднее напряжение разряда дает удельную энергию, и это соотношение находит выражение в уравнении 1:
Плотность энергии и удельная энергия аккумуляторов по определению — это количество энергии, запасенной в данной системе на единицу объема и на единицу массы соответственно. Произведение удельной емкости на среднее напряжение разряда дает удельную энергию, и это соотношение находит выражение в уравнении 1:
E = C · U (1)
Согласно уравнению 1 кажется разумным, что большая часть текущих исследований сосредоточена на новых материалах положительных электродов с более высокими рабочими напряжениями (подход с высоким напряжением) и/или повышенной удельной емкостью (высокопроизводительный подход). Высоковольтные катодные материалы сильно ограничены узким окном электрохимической стабильности современных электролитов на основе карбонатов (≈1,0 – 4,4 В против Li/Li + ) и усилить конструкцию внутренне стабильных электролитов или подходящих добавок к электролиту, позволяющих создавать высоковольтные литий-ионные батареи.
Мы с нетерпением ждем вашего сообщения
Имя
Пожалуйста, оставьте это поле пустым.
