Значение слова «Катализатор» в 10 онлайн словарях Даль, Ожегов, Ефремова и др.
Поделиться значением слова:КАТАЛИЗАТОР, -а, м. (спец.). Вещество, изменяющее скорость химической реакции. || прил. катализаторный, -ая, -ое.
Ударение: катализа́тор м.
- Вещество, увеличивающее скорость химической реакции.
- перен. Факт, явление и т.п., способствующие развитию чего-л.
КАТАЛИЗА́ТОР, катализатора, ·муж. (см. катализ» title=’что такое катализ, значение слова катализ в словаре Ушакова’>катализ) (·хим. ). Вещество, ускоряющее или замедляющее химическую реакцию, само при этом не изменяющееся.
биокатализатор, гопкалит, сиккатив, сульфурилхлорид, ускоритель, фермент, фотокатализатор, электрокатализатор, энзим
катализа́тор,
катализа́торы,
катализа́тора,
катализа́торов,
катализа́тору,
катализа́торам,
катализа́тор,
катализа́торы,
катализа́тором,
катализа́торами,
катализа́торе,
катализа́торах
а, м.
1. Вещество, изменяющее скорость химической реакции. Катализаторный — относящийся к катализатору, катализаторам. СТАБИЛИЗАТОР» title=’СТАБИЛИЗАТОР, СТАБИЛИЗАТОР это, что такое СТАБИЛИЗАТОР, СТАБИЛИЗАТОР толкование’>СТАБИЛИЗАТОР.
2. перен. О явлении, способствующем развитию, изменению чего-нибудь Свобода — к. общественного прогресса.
Катализатор Википедия
Схема протекания реакции с катализаторомКатализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Ингибитор не является противоположным понятием, так как расходуется в ходе реакции[источник не указан 440 дней].
Катализаторы в химии[ | ]
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества
Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO[1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со +3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции[2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные
Катализатор — Википедия. Что такое Катализатор
Что такое Катализатор
Схема протекания реакции с катализаторомКатализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Противоположное понятие — ингибитор.
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества[1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al 2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO[1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции[2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня[2].
Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня[2].
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счёт неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.[4]
См. также
Примечания
- ↑ 1 2 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ 1 2 Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия.
 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X. - ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru. Архивировано 25 августа 2011 года.
Ссылки
Что такое автомобильный катализатор и как проверить (или удалить)
Одной из систем очистки выхлопных газов автомобиля является каталитический нейтрализатор отработавших газов, который называют катализатором или нейтрализатором, хотя это то же самое. Расскажем что это такое и как проверить самому, рассмотрим основные причины, если он забит.
Что это такое
Катализатор — устройство, которое располагается в выхлопной системе и нужно для очистки выходящих оттуда газов. С помощью химических реакций в данном устройстве вредные вещества превращаются в менее пагубные, которые выходят наружу. Т.е. из выхлопной трубы после его работы выходит воздух с минимальными загрязнениями.
С помощью химических реакций в данном устройстве вредные вещества превращаются в менее пагубные, которые выходят наружу. Т.е. из выхлопной трубы после его работы выходит воздух с минимальными загрязнениями.
Катализатор начинает работать только после нагревания, т.е. при пуске холодного двигателя он бездействует.
Вместе с ним работают кислородные датчики, которые определяют состав смеси и соотношение воздуха с бензином в горючей смеси. Ведь от этого соотношения зависит, какая будет смесь: обогащённая или обеднённая. Кислородные датчики, в зависимости от показаний, управляют работой катализатора.
Располагается катализатор в выхлопной трубе между двигателем и глушителем, закрытое снизу (обязательно!) дополнительным экраном, потому что при сильном нагреве он раскаляется почти докрасна.
Как проверить: работает или нет
У катализатора бывает ТРИ состояния: рабочее, полурабочее, нерабочее. Рассмотрим эти три состояния и как ведет себя машина при каждом из них. В рабочем состоянии машина работает нормально, лампочка ошибки на панели приборов не загорается при работе двигателя, претензий ни к чему нет.
В рабочем состоянии машина работает нормально, лампочка ошибки на панели приборов не загорается при работе двигателя, претензий ни к чему нет.
В «полурабочем» состоянии начинаются проблемы. Машина ведет себя как-то не так:
- Временами (или всегда) пропадает тяга и «приемистость» на больших оборотах; вчера «тянула» нормально, а сегодня ее вроде бы что-то «за зад держит».
- По утрам и в состоянии «на горячую» машина стала заводиться хуже, двигатель приходится долго «гонять» стартером, чтобы завелся.
- Иногда «куда-то пропадают обороты»: давите на педаль газа, а стрелка тахометра с трудом добирается до двух или четырех тысяч и там останавливается. Машина начинает чрезмерно потреблять бензин.
Возможна еще такая проверка — подтверждение «полурабочего» состояния. Когда у Вас начались подобные проблемы, надо завести двигатель и «утопить» педаль до упора. Если двигатель начнет медленно поднимать обороты и остановится где-то на двух-трех тысячах, а дальше — ни в какую — возможны проблемы с катализатором.
В «нерабочем» состоянии машина заводится долго, а когда заведется – то глохнет почти сразу же или не заводится, т.е. даже не «схватывает».
«Третье состояние» проверить просто: надо в момент пуска машины подойти к выхлопной трубе и посмотреть (почувствовать, например, приложенной рукой) – идут оттуда выхлопные газы или нет.
Как удалить катализатор авто
Вопросы экологии и покупки нового не рассматриваем – 99% автолюбителей просто удаляют его, т.к. новый катализатор стоит дорого из-за содержания в нём платины. Хочется предостеречь от распространенной ошибки: всегда удаляйте его полностью, а не пробивайте только отверстие. Кто даст гарантию, что время это отверстие не забьется?
После удаления внимательно осмотрите внутренность той емкости, в которой находился катализатор и увидите «прикипевшую» к поверхности металлическую сеточку, одну или несколько. Ее удаляйте тоже.
Можно вырезать катализатор и вварить гофровую трубу. Это даст не жесткое соединение мотора и выпускной системы, а также дополнительное охлаждение газов.
Возможно ли почистить катализатор
Это зависит от степени и вида загрязнения. Если он забился серой и парафином после заправки плохим бензином — то ничего не поможет. В этом случае меняют на новый или ставят обманку. Другое дело, если забился серой. Специальная автохимия его может очистить.
Каталитический нейтрализатор: устройство и принцип работы
В составе выхлопных газов автомобиля содержится довольно много токсичных веществ. Для предотвращения их попадания в атмосферу используется специальное устройство, получившее название “каталитический нейтрализатор” (более известный как “катализатор”). Он устанавливается на автомобилях, оснащенных двигателями внутреннего сгорания, работающих как на бензине, так и на дизельном топливе. Зная принцип работы катализатора, вы сможете понять важность его работы и оценить последствия, которые может вызвать его удаление.
Конструкция и функции каталитического нейтрализатора
Устройство каталитического нейтрализатораНейтрализатор является частью системы выхлопа. Он располагается сразу за выпускным коллектором двигателя. Катализатор состоит из:
Он располагается сразу за выпускным коллектором двигателя. Катализатор состоит из:
- Металлический корпус (монтажный мат), имеющий входной и выходной патрубки.
- Керамический блок (монолит). Представляет собой пористую структуру с множеством ячеек, которые увеличивают площадь соприкосновения выхлопных газов с рабочей поверхностью.
- Каталитический слой – специальное напыление на поверхностях ячеек керамического блока, состоящее из платины, палладия и родия. В последних моделях для напыления иногда используется золото – драгоценный металл, который имеет более низкую стоимость.
- Металлический кожух. Выполняет функции теплоизоляции и защиты катализатора от механических повреждений.
Главная функция каталитического нейтрализатора – это нейтрализация трех основных токсических компонентов отработавших газов, поэтому он получил свое название – трехкомпонентный. Вот эти нейтрализуемые компоненты:
- Окислы азота NOx – компонент смога, причина кислотных дождей, ядовиты для человека.

- Угарный газ СО – смертельно опасен для человека при концентрации в воздухе от 0,1%.
- Углеводороды CH – компонент смога, отдельные соединения канцерогены.
Принцип действия катализатора
На практике трехкомпонентный каталитический нейтрализатор имеет следующий принцип действия:
- Выхлопные газы из двигателя попадают внутрь керамических блоков, где проникают в ячейки, полностью заполняя их.
- Металлы-катализаторы палладий и платина провоцируют реакцию окисления, в результате которой несгоревшие углеводороды СН преобразуются в водяной пар, а угарный газ СО в углекислый.
- Восстановительный металл-катализатор родий преобразует NOx (оксид азота) в обычный безвредный азот.
- В атмосферу выпускаются очищенные отработавшие газы.
Если в автомобиле установлен дизельный двигатель, то возле катализатора всегда находится сажевый фильтр. Иногда эти два элемента могут быть совмещены в единую конструкцию.
Рабочая температура катализатора играет решающую роль в эффективности процесса нейтрализации токсичных компонентов. Реальное преобразование начинается только после достижения 300°С. Идеальной, с точки зрения эффективности и срока службы, считается температура от 400 до 800°С. В диапазоне температур от 800 до 1000°С наблюдается ускоренное старение нейтрализатора. Длительная работа при температуре свыше 1000°С оказывает губительное воздействие на катализатор. Альтернативой керамике, выдерживающей высокие температуры, является металлическая матрица из гофрированной фольги. Катализаторами в такой конструкции выступают платина и палладий.
Реальное преобразование начинается только после достижения 300°С. Идеальной, с точки зрения эффективности и срока службы, считается температура от 400 до 800°С. В диапазоне температур от 800 до 1000°С наблюдается ускоренное старение нейтрализатора. Длительная работа при температуре свыше 1000°С оказывает губительное воздействие на катализатор. Альтернативой керамике, выдерживающей высокие температуры, является металлическая матрица из гофрированной фольги. Катализаторами в такой конструкции выступают платина и палладий.
Срок службы катализатора
Разрушение керамического блока катализатораСредний ресурс катализатора составляет 100 тыс. километров пробега, но при правильной эксплуатации он может исправно функционировать и до 200 тыс. километров. Основные причины раннего износа – неисправность двигателя и качество топлива (топливовоздушной смеси). При наличии обедненной смеси происходит перегрев, а при слишком богатой возникает засорение пористого блока остатками несгоревшего топлива, что препятствует протеканию необходимых химических процессов. Это приводит к тому, что срок службы каталитического нейтрализатора существенно снижается.
километров пробега, но при правильной эксплуатации он может исправно функционировать и до 200 тыс. километров. Основные причины раннего износа – неисправность двигателя и качество топлива (топливовоздушной смеси). При наличии обедненной смеси происходит перегрев, а при слишком богатой возникает засорение пористого блока остатками несгоревшего топлива, что препятствует протеканию необходимых химических процессов. Это приводит к тому, что срок службы каталитического нейтрализатора существенно снижается.
Еще одной распространенной причиной неисправности керамического катализатора являются механические повреждения (трещины), возникающие при механических воздействиях. Они провоцируют быстрое разрушение блоков.
При возникновении неисправностей работа каталитического нейтрализатора ухудшается, что фиксируется при помощи второго лямбда-зонда. В этом случае электронный блок управления сообщит о неисправности, выдав на приборной панели ошибку «CHECK ENGINE». Также признаками выхода из строя являются дребезжание, увеличение расхода топлива и ухудшение динамики. В этом случае его меняют на новый (оригинального производства или универсальный). Почистить или восстановить катализаторы невозможно, а поскольку это устройство имеет высокую цену, многие автомобилисты предпочитают просто удалить его.
В этом случае его меняют на новый (оригинального производства или универсальный). Почистить или восстановить катализаторы невозможно, а поскольку это устройство имеет высокую цену, многие автомобилисты предпочитают просто удалить его.
Можно ли удалить катализатор
При удалении катализатора его очень часто заменяют на пламегаситель. Последний выравнивает поток выхлопных газов. Его установка рекомендуется для устранения неприятных шумов, которые возникают при удалении катализатора. При этом, если вы выбрали именно удаление, лучше полностью снять устройство и не прибегать к рекомендациям некоторых автомобилистов пробить в нем отверстие. Подобная процедура улучшит ситуацию только на время.
В автомобилях, соответствующих экологическим стандартам Евро-3, помимо удаления катализатора необходима перепрошивка электронного блока управления. Ее обновляют до версии, в которой отсутствует каталитический нейтрализатор. Также можно установить эмулятор сигнала кислородного датчика, который избавит от необходимости перепрошивать ЭБУ.
Наилучшим решением при поломке каталитического нейтрализатора будет его замена на оригинальную деталь в специализированном сервисе. Таким образом будет исключено вмешательство в конструкцию автомобиля, а его экологический класс будет соответствовать заявленному производителем.
Что такое катализатор? (с иллюстрациями)
Катализатор — это любое вещество, которое ускоряет химическую реакцию. Он может быть органическим, синтетическим или металлическим. Процесс, посредством которого это вещество ускоряет или замедляет реакцию, называется катализом.
Ученые часто добавляют катализатор в химический раствор, чтобы вызвать реакцию. Для любого процесса требуется энергия, известная как энергия активации. Без помощи катализатора количество энергии, необходимое для разжигания конкретной реакции, велико. Когда он присутствует, энергия активации снижается, благодаря чему реакция протекает более эффективно. Вещество обычно работает либо путем изменения структуры молекулы, либо путем связывания с молекулами реагентов, заставляя их объединяться, реагировать и выделять продукт или энергию. Например, для соединения газов кислорода и водорода с образованием воды требуется катализатор.
Когда он присутствует, энергия активации снижается, благодаря чему реакция протекает более эффективно. Вещество обычно работает либо путем изменения структуры молекулы, либо путем связывания с молекулами реагентов, заставляя их объединяться, реагировать и выделять продукт или энергию. Например, для соединения газов кислорода и водорода с образованием воды требуется катализатор.
Без помощи катализатора химические реакции могут никогда не произойти или на их прохождение потребуется значительно больше времени.Когда происходит химическая реакция, сам катализатор не изменяется и не является частью конечного результата. В большинстве случаев его можно многократно использовать в последующих реакциях.
В большинстве случаев его можно многократно использовать в последующих реакциях.
Иногда вместо ускорения реакции катализатор замедляет реакцию, которая обычно не происходит или происходит очень медленно.Этот тип вещества является отрицательным катализатором, который также называют ингибитором. Ингибиторы важны в медицине, где они имеют решающее значение при лечении психических заболеваний, высокого кровяного давления, рака и множества других проблем со здоровьем.
Катализатор используется в двух типах условий: химических или биохимических. Наиболее часто в биохимических реакциях используются ферменты. Ферменты — это узкоспециализированные белки, которые ускоряют определенные химические реакции. Они делают жизнь возможной. Например, фермент, содержащийся в слюне, при контакте расщепляет пищу для переваривания. Без этого человеку потребовались бы недели, чтобы переварить нашу пищу.
Наиболее часто в биохимических реакциях используются ферменты. Ферменты — это узкоспециализированные белки, которые ускоряют определенные химические реакции. Они делают жизнь возможной. Например, фермент, содержащийся в слюне, при контакте расщепляет пищу для переваривания. Без этого человеку потребовались бы недели, чтобы переварить нашу пищу.
также важны в лабораторных условиях, а также в производстве и промышленности.Одним из самых известных является каталитический нейтрализатор, который помогает предотвратить автомобильные выбросы и снизить расход топлива. Удобрения также являются катализаторами, ускоряющими рост растений.
Катализаторы ускоряют химическую реакцию.
Определение катализатора — Химический словарь
Что такое катализатор?
Катализатор — это вещество, которое ускоряет химическую реакцию, но не расходуется в ходе реакции; следовательно, катализатор может быть восстановлен химически без изменений в конце реакции, которую он использовал для ускорения, или катализатор .
Обсуждение
Чтобы химические вещества вступили в реакцию, их связи должны быть перегруппированы, потому что связи в продуктах отличаются от связей в реагентах. Самый медленный шаг в перегруппировке связи приводит к так называемому переходному состоянию. — химическое соединение, которое не является ни реагентом, ни продуктом, но является промежуточным звеном между ними.
Реагент ⇄ Переходное состояние ⇄ Продукт
Для формирования переходного состояния требуется энергия. Эта энергия называется энергией активации или E a .Чтение приведенной ниже диаграммы слева направо показывает прогресс реакции, когда реагенты проходят через переходное состояние и становятся продуктами.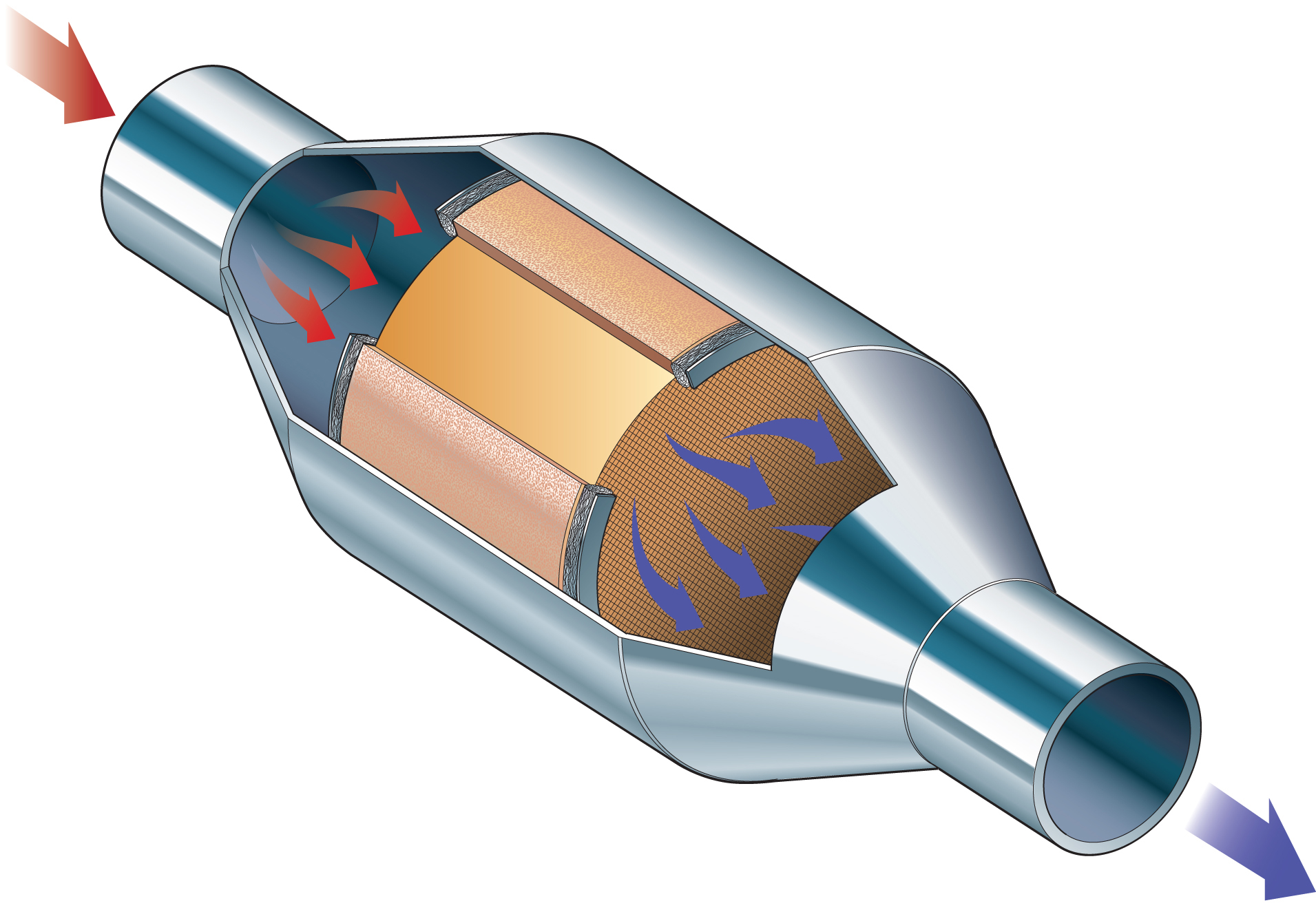
Преодолевая барьер
Энергию активации можно рассматривать как барьер для химической реакции, барьер, который необходимо преодолеть. Если барьер высокий, немногие молекулы обладают достаточной кинетической энергией, чтобы столкнуться, сформировать переходное состояние и пересечь барьер. Реагенты с энергией ниже E a не могут пройти через переходное состояние, чтобы вступить в реакцию и стать продуктами.
Катализатор работает, обеспечивая другой путь реакции, с более низким E и . Катализаторы снижают энергетический барьер. Другой путь позволяет упростить перегруппировку связей, необходимую для превращения реагентов в продукты, с меньшим потреблением энергии. В любой заданный интервал времени присутствие катализатора позволяет большей части реагентов набрать достаточно энергии, чтобы пройти через переходное состояние и стать продуктами.
Пример 1: Процесс Габера
Процесс Габера, который используется для получения аммиака из водорода и азота, катализируется железом, которое обеспечивает атомные центры, на которых связи реагентов могут легче перестраиваться с образованием переходного состояния.
N 2 (газ) + 3H 2 (газ) ⇌ 2NH 3 (газ)
Пример 2: Ферменты
В нашем организме и в других живых существах ферменты используются для ускорения биохимических реакций. Фермент — это разновидность катализатора.
Сложная жизнь была бы невозможна без ферментов, позволяющих протекать реакциям с подходящей скоростью.
Формы ферментов вместе с местами на ферменте, которые связываются с реагентами, обеспечивают альтернативный путь реакции, позволяя конкретным молекулам объединяться, чтобы сформировать переходное состояние с пониженным энергетическим барьером активации.
На схеме ниже длинноцепочечный фермент обеспечивает места для молекул реагентов, которые собираются вместе, чтобы сформировать переходное состояние с низкой энергией активации.
Катализаторы не могут изменить положение химического равновесия — прямая и обратная реакции ускоряются, так что константа равновесия K eq не изменяется. Однако, удаляя продукты из реакционной смеси по мере их образования, на практике можно увеличить общую скорость образования продукта.
Однако, удаляя продукты из реакционной смеси по мере их образования, на практике можно увеличить общую скорость образования продукта.
видов катализа
Катализатор находится в той же фазе, что и реагенты. Обычно все присутствует в виде газа или в одной жидкой фазе. Примеры содержат по одному из них. . .
Примеры гомогенного катализа
Реакция между персульфат-ионами и иодид-ионами
Это реакция раствора, которую вы можете встретить только в контексте катализа, но это прекрасный пример!
Персульфат-ионы (пероксодисульфат-ионы), S 2 O 8 2- , являются очень сильными окислителями.Иодид-ионы очень легко окисляются до йода. И все же реакция между ними в растворе в воде очень медленная.
Если вы посмотрите на уравнение, легко понять, почему это так:
Для реакции требуется столкновение двух отрицательных ионов. Этому серьезно помешает отталкивание!
Катализированная реакция полностью устраняет эту проблему. Катализатором могут быть ионы железа (II) или железа (III), которые добавляются в один и тот же раствор.Это еще один хороший пример использования соединений переходных металлов в качестве катализаторов из-за их способности изменять степень окисления.
Катализатором могут быть ионы железа (II) или железа (III), которые добавляются в один и тот же раствор.Это еще один хороший пример использования соединений переходных металлов в качестве катализаторов из-за их способности изменять степень окисления.
Для аргументации в качестве катализатора примем ионы железа (II). Как вы вскоре увидите, на самом деле не имеет значения, используете ли вы ионы железа (II) или железа (III).
Ионы персульфата окисляют ионы железа (II) до ионов железа (III). В процессе ионы персульфата восстанавливаются до ионов сульфата.
Ионы железа (III) являются достаточно сильными окислителями, чтобы окислять иодид-ионы до йода.В процессе они снова восстанавливаются до ионов железа (II).
Обе эти отдельные стадии в общей реакции включают столкновение между положительными и отрицательными ионами. Это будет гораздо более успешным, чем столкновение двух отрицательных ионов в некаталитической реакции.
Что произойдет, если в качестве катализатора использовать ионы железа (III) вместо ионов железа (II)? Просто реакции происходят в другом порядке.
Разрушение атмосферного озона
Это хороший пример гомогенного катализа, где все присутствует в виде газа.
Озон, O 3 , постоянно образуется и снова распадается в высоких слоях атмосферы под действием ультрафиолетового света. Обычные молекулы кислорода поглощают ультрафиолетовый свет и распадаются на отдельные атомы кислорода. Они имеют неспаренные электроны и известны как свободные радикалы . Они очень реактивны.
Кислородные радикалы могут затем соединяться с обычными молекулами кислорода с образованием озона.
Озон также можно снова разделить на обычный кислород и кислородный радикал, поглощая ультрафиолетовый свет.
Это образование и распад озона происходит постоянно. Взятые вместе, эти реакции останавливают большое количество вредного ультрафиолетового излучения, проникающего в атмосферу и достигающего поверхности Земли.
Каталитическая реакция, в которой мы заинтересованы, разрушает озон и, таким образом, останавливает его поглощение ультрафиолетового излучения.
Хлорфторуглероды (CFC), такие как CF 2 Cl 2 , например, широко использовались в аэрозолях и в качестве хладагентов.При их медленном распаде в атмосфере образуются атомы хлора — свободные радикалы хлора. Они катализируют разрушение озона.
Это происходит в два этапа. В первом случае озон расщепляется и образуется новый свободный радикал.
Катализатор на основе хлор-радикала регенерируется второй реакцией. Это может происходить двумя способами в зависимости от того, попадает ли радикал ClO в молекулу озона или радикал кислорода.
Если он попадает в кислородный радикал (образованный в результате одной из реакций, которые мы рассмотрели ранее):
Или, если он попадает в молекулу озона:
Поскольку радикал хлора продолжает регенерироваться, каждый из них может разрушить тысячи молекул озона.
Как работают каталитические нейтрализаторы | HowStuffWorks
В химии катализатор — это вещество, которое вызывает или ускоряет химическую реакцию, не затрагивая себя. Катализаторы участвуют в реакциях, но не являются ни реагентами, ни продуктами реакции, которую они катализируют. В организме человека ферменты являются природными катализаторами, ответственными за многие важные биохимические реакции [источник: Chemicool].
Катализаторы участвуют в реакциях, но не являются ни реагентами, ни продуктами реакции, которую они катализируют. В организме человека ферменты являются природными катализаторами, ответственными за многие важные биохимические реакции [источник: Chemicool].
В каталитическом нейтрализаторе работают два различных типа катализатора: катализатор восстановления и катализатор окисления .Оба типа состоят из керамической структуры, покрытой металлическим катализатором, обычно платиной, родием и / или палладием. Идея состоит в том, чтобы создать структуру, которая подвергает максимальную площадь поверхности катализатора потоку выхлопных газов, а также минимизирует необходимое количество катализатора, поскольку материалы чрезвычайно дороги. Некоторые из новейших конвертеров даже начали использовать золото, смешанное с более традиционными катализаторами. Золото дешевле, чем другие материалы, и может увеличивать окисление, химическую реакцию, которая снижает количество загрязняющих веществ, до 40 процентов [источник: Kanellos].
Объявление
Большинство современных автомобилей оборудовано трехкомпонентными каталитическими нейтрализаторами . Это относится к трем регулируемым выбросам, которые он помогает уменьшить.
Катализатор восстановления — первая ступень каталитического нейтрализатора. В нем используются платина и родий для снижения выбросов NOx. Когда молекула NO или NO2 контактирует с катализатором, катализатор вырывает атом азота из молекулы и удерживает его, высвобождая кислород в форме O2.Атомы азота связываются с другими атомами азота, которые также прилипают к катализатору, образуя N2. Например:
2НО => N2 + O2 или 2НО2 => N2 + 2O2
2НО => N 2 + O 2 или 2НО 2 => N 2 + 2O 2
Катализатор окисления — вторая ступень каталитического нейтрализатора. Он уменьшает количество несгоревших углеводородов и окиси углерода, сжигая (окисляя) их над платиновым и палладиевым катализатором. Этот катализатор способствует реакции CO и углеводородов с оставшимся кислородом в выхлопных газах. Например:
Он уменьшает количество несгоревших углеводородов и окиси углерода, сжигая (окисляя) их над платиновым и палладиевым катализатором. Этот катализатор способствует реакции CO и углеводородов с оставшимся кислородом в выхлопных газах. Например:
2CO + O 2 => 2CO 2
В каталитических нейтрализаторах используются два основных типа структур — соты и керамические шарики . Сегодня в большинстве автомобилей используется сотовая структура.
В следующем разделе мы рассмотрим третий этап процесса конверсии и то, как получить максимальную отдачу от катализатора.
.
