Анодная защита кузова от корозии » Полезные самоделки ✔тысячи самоделок для всей семьи
Общеизвестно, что если не принимать определенных мер, то кузов автомобиля в течение четырех-пяти лет может превратиться буквально в ржавое решето. Зачастую не помогают ни лакокрасочные покрытия, ни мастики, поскольку кузов имеет немало закрытых полостей, пазух, карманов, коробов, в которых дорожная грязь и сырость, замешанные на поваренной соли, создают великолепные условия для электрохимической коррозии. А при современной толщине автомобильного стального листа это приводит к весьма быстрому его выходу из строя.
Но от коррозии можно не только защищаться броней из лака или хрома, ее можно и обмануть, подсунув в виде приманки такой лакомый кусочек, как металл с более высоким электродным потенциалом.
О катодной защите кузова ранее писалось в здесь>>> но в этот раз немного дополним эту статью.
Ржавчина — враг номер один почти любого металла. «Рыжая чума», с завидным упорством и постоянством превращающая сотни тонн сверкающей высокосортной, легированной стали в груды коричневого порошка. Болезнь, для которой не существует преград… Но существуют лекарства и от нее: гальванические покрытия, лаки и краски, битумы и мастики — все они в принципе должны защитить металл. Но на деле все не так просто.
Болезнь, для которой не существует преград… Но существуют лекарства и от нее: гальванические покрытия, лаки и краски, битумы и мастики — все они в принципе должны защитить металл. Но на деле все не так просто.
Очень остро проблема защиты от коррозии стоит, к примеру, перед автомобилистами. Общеизвестно, что если не принимать определенных мер, то кузов автомобиля в течение четырех-пяти лет может превратиться буквально в ржавое решето. Зачастую не помогают ни лакокрасочные покрытия, ни мастики, поскольку кузов имеет немало закрытых полостей, пазух, карманов, коробов, в которых дорожная грязь и сырость, замешанные на поваренной соли, создают великолепные условия для электрохимической коррозии. А при современной толщине автомобильного стального листа это приводит к весьма быстрому его выходу из строя.
Но от коррозии можно не только защищаться броней из лака или хрома, ее можно и обмануть, подсунув в виде приманки такой лакомый кусочек, как металл с более высоким электродным потенциалом.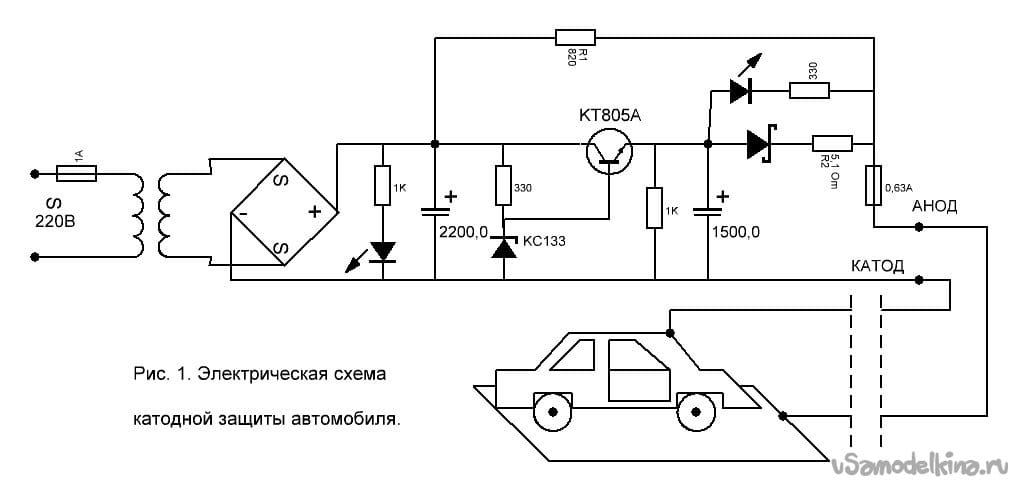
Электродный потенциал? А какое он, собственно, имеет отношение к коррозии металлов? Оказывается, самое непосредственное.
Если опустить в сосуд с электролитом два электрически связанных между собой металлических электрода, то один из них начнет растворяться, другой же останется в неприкосновенности. Так вот, оказывается, растворяется металл, электродный потенциал которого выше. Это свойство гальванической пары и дало возможность использовать эффект сохранения катода для предохранения от электрохимической коррозии кузова автомобиля.
Судостроители давно уже используют этот принцип предохранения внутренней части трюма от коррозии — они размещают внутри корпуса специальные металлические аноды (из металла с более высоким электродным потенциалом, чем у металла корпуса). Этот способ недавно взяли на вооружение и автомобилисты.
Для анодной защиты применяют оребренные (для увеличения поверхности) куски цинка С помощью вделанных в них постоянных магнитов они прикрепляются в наиболее труднодоступных и загрязняемых местах кузова. Электрическая связь осуществляется многожильным проводом: с помощью винтов цинковый анод подсоединяется к кузову.
Электрическая связь осуществляется многожильным проводом: с помощью винтов цинковый анод подсоединяется к кузову.
На его ребрах собирается дорожная грязь, влага, поваренная соль и комплект «цинк — сталь» начинает работать так, как работает всем известный гальванический элемент. При работе такой «батареи» происходит растворение цинкового анода, катод в данном случае не расходуется.
Рис. 1. Комплект для анодной защиты кузова автомобиля:
1 — оребренный цинковый электрод, 2 — соединительный провод.
Процесс коррозии напоминает работу гальванического элемента, поскольку сталь представляет собой, в основном, сплав железа и углерода, то есть веществ с различными электродными потенциалами. При попадании на поверхность такого сплава электролита между молекулами железа и углерода начинает идти электрохимическая реакция, сопровождающаяся растворением анода (железа) и переходом его в гидраты, а затем и в окислы.
Рис. 2. Установка электрода в колесной нише.
Присутствие же электрически связанного с основным металлом цинкового электрода в корне меняет картину. По отношению, как к железу, так и к углероду цинк представляет собой металл с более высоким электродным потенциалом, то есть выступает в роли анода. Поэтому при наличии электропроводной среды, которая практически всегда присутствует на поверхностях автомобильного кузова, электрохимическая реакция идет с растворением анода (цинка), при сохранении катода, то есть металла кузова.
Рис. 3. Установка электродов в этих точках наиболее эффективна:
1 — коробчатые усилители брызговиков, 2 — места крепления корпусов фар и подфарников, 3 — нижняя часть передней панели, 4 — полости за щитками-усилителями передних крыльев, 5 — внутренние поверхности дверей, 6, 7 — передняя нижняя часть заднего крыла и арка колеса по стыку с крылом, 8 — фартук задней панели.
Как показали эксперименты, цинкового электрода величиной со спичечную коробку хватает на 3-5 лет.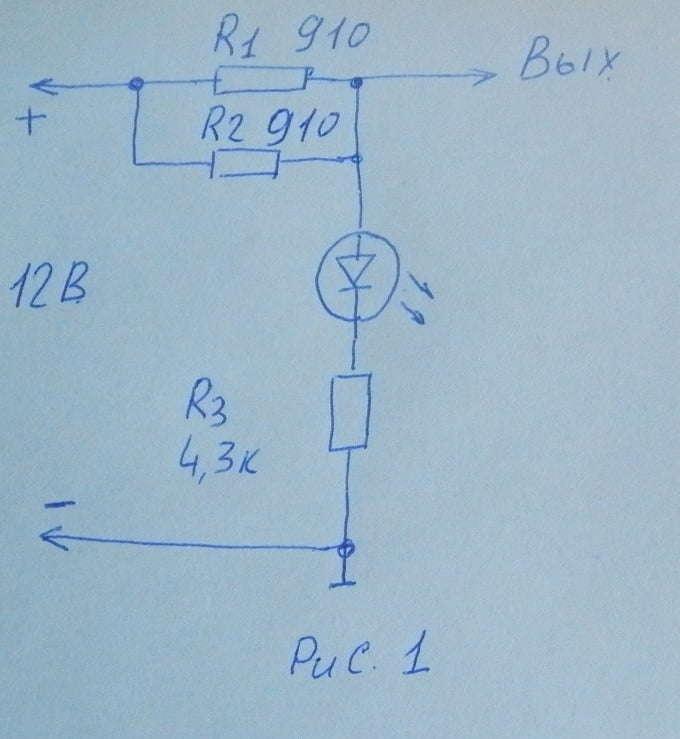
Обманите «рыжую чуму». Подсуньте ей приманку — кусочек металла с электродным потенциалом выше, чем у стали. Коррозия охотно вцепится в него, забыв про кузов вашего автомобиля как минимум на три год.
В. В. Бородин «Защита автомобиля от коррозии электрохимическим способом»
Оглавление
1. Механизм корозии корпуса автомобиля.
2. Корозия автомобиля во время эксплуатации и пассивные методы борьбы с ней.
3. Корозия автомобиля на открытой стоянке.
4. Корозия автомобиля при хранении в гараже.
5. Корозия движущегося автомобиля.
6. Протекторная защита от корозии.
7. Электрохимическая защита от корозии.
8. Устройство для электрохимической защиты кузова автомобиля от корозии.
9. Правила установки и эксплуатации устройства.
10. Электрохимическая защита.
11. Защита поврежденных в результате аварии частей кузова.
12. Заключение Приложения.
13. Приложение 1. Скрытые полости автомобиля.
14. Приложение 2. Использование защитных покрытий для предотвращения корозии кузова автомобиля.
Прежде
чем пытаться защититься от коррозии,
необходимо ответить на вопрос о том,
что же такое коррозия металла. В обиходе
коррозией называют появление ржавчины
на поверхности металла. Каковы же
основные механизмы появления
ржавчины?
Необходимо признать, что до
настоящего времени полного ответа на
этот вопрос нет, а результаты проводимых
исследований показывают, что процесс
коррозии является очень сложным,
поскольку на его протекание оказывает
влияние большое число факторов —
химический состав металла среда, в
которой он находится температура
давление наличие газов и т.д. По этой
причине в книге изложены только самые
начальные сведения из теории коррозии,
знание которых необходимо для правильной
защиты корпуса автомобиля. Более полное
представление о механизмах коррозии
читатель может почерпнуть из рекомендуемой
литературы. Коррозия железа (а именно
этот процесс мы будем рассматривать в
дальнейшем) осуществляется, если
дополнительно имеются, по крайней мере,
еще две составляющие электролит, с
которым граничит железо, и другой
проводник, также граничащий с электролитом.
Электролитом в обычных условиях является
дождевая вода атмосферная влага снег,
дорожная грязь. Вторым, по отношению к
кузову автомобиля проводником чаще
всего является поверхность земли,
атмосфера, какой либо другой внешний
проводник, расположенный вблизи
автомобиля. Два проводника (которые в
данном случае называются электродами)
погруженные в электролит образуют так
называемый гальванический элемент.
Основное свойство гальванического
элемента состоит в том, что если электроды
выполнены из различных металлов, то
такой элемент является источником
напряжения. При этом положительный,
электрод называется анодом отрицательный
— катодом.
Проделайте простой
эксперимент. В стакане теплой воды
растворите ложку поваренной соли и
опустите две пластины — одну медную
другую стальную.
Коррозия железа (а именно
этот процесс мы будем рассматривать в
дальнейшем) осуществляется, если
дополнительно имеются, по крайней мере,
еще две составляющие электролит, с
которым граничит железо, и другой
проводник, также граничащий с электролитом.
Электролитом в обычных условиях является
дождевая вода атмосферная влага снег,
дорожная грязь. Вторым, по отношению к
кузову автомобиля проводником чаще
всего является поверхность земли,
атмосфера, какой либо другой внешний
проводник, расположенный вблизи
автомобиля. Два проводника (которые в
данном случае называются электродами)
погруженные в электролит образуют так
называемый гальванический элемент.
Основное свойство гальванического
элемента состоит в том, что если электроды
выполнены из различных металлов, то
такой элемент является источником
напряжения. При этом положительный,
электрод называется анодом отрицательный
— катодом.
Проделайте простой
эксперимент. В стакане теплой воды
растворите ложку поваренной соли и
опустите две пластины — одну медную
другую стальную.
 Полученная
разность потенциалов между стандартным
электродом и металлом получила название
стандартного электродного потенциала
(СЭП).
Ниже приведены стандартные
электродные потенциалы некоторых
металлов, расположенные в порядке
снижения их активности, т.е. чем более
отрицательным является СЭП тем
выше активность металла.
Полученная
разность потенциалов между стандартным
электродом и металлом получила название
стандартного электродного потенциала
(СЭП).
Ниже приведены стандартные
электродные потенциалы некоторых
металлов, расположенные в порядке
снижения их активности, т.е. чем более
отрицательным является СЭП тем
выше активность металла.Стандартные электродные потенциалы металлов, В
Магний | -2,38 | Танталл | -0,34 |
Алюминий | -1,66 | Никель | -0,24 |
Марганец | -1,18 | Молибден | -0,2 |
Хром | -0,91 | Свинец | -0,13 |
Цинк | -0,76 | Медь | 0,34 |
Железо | -0,44 | Серебро | 0,8 |
Кадмий | -0,4 |
|
|
Наибольший
интерес представляет процесс коррозии
железа в электролите при наличии менее
активного металла.

Fe + 20Н— = Fe2+ + 2е + 20Н— = Fe(OH)2 + 2е.
Под действием ионов железа на катоде возникают ионы водорода (Н+), с которыми и соединяются электроны анода. Схематически этот процесс описывается в следующем виде:
Н+ + 2е = 2Н = Н2
т.е. на катоде происходит выделение водорода. Если анодная и катодная реакции объединяются, они приводят к общей реакции коррозии
Fе + 2Н20 = Fе(ОН)2 + Н2
Таким
образом, железо в сочетании с водой и
менее активным металлом переходит в
гидроокись железа, которая в обиходе и
называется ржавчиной.
Наличие в воде
дополнительной соли приводит к повышению
проводимости электролита и, как следствие,
к увеличению скорости окисления анода.
При этом дополнительно образуются
хлорное железо и раствор соляной кислоты.
 Этот метод в литературе называется
катодной защитой.
Катодная защита
металлов основана на том, что скорость
коррозии пропорциональна активности
металлов, образующих гальваническую
пару. В обычных условиях корпус автомобиля
является анодом и поэтому корродирует.
Если же изменить потенциал корпуса
относительно внешней среды либо с
помощью внешнего источника напряжения
либо приведя в контакт с более активным
металлом, то сам корпус автомобиля
станет катодом и корродировать вообще
не будет (по крайней мере скорость
коррозии уменьшится в сотни раз), а
разрушаться станет анод. В соответствии
со способом изменения потенциала
защищаемого металла различают протекторную
и электрохимическую защиту. Однако
прежде чем рассматривать методы защиты,
целесообразно описать особенности
коррозии автомобиля в различных условиях
его эксплуатации.
Этот метод в литературе называется
катодной защитой.
Катодная защита
металлов основана на том, что скорость
коррозии пропорциональна активности
металлов, образующих гальваническую
пару. В обычных условиях корпус автомобиля
является анодом и поэтому корродирует.
Если же изменить потенциал корпуса
относительно внешней среды либо с
помощью внешнего источника напряжения
либо приведя в контакт с более активным
металлом, то сам корпус автомобиля
станет катодом и корродировать вообще
не будет (по крайней мере скорость
коррозии уменьшится в сотни раз), а
разрушаться станет анод. В соответствии
со способом изменения потенциала
защищаемого металла различают протекторную
и электрохимическую защиту. Однако
прежде чем рассматривать методы защиты,
целесообразно описать особенности
коррозии автомобиля в различных условиях
его эксплуатации.Стоит ли электронная защита от ржавчины? – LINE-X of South Central PA
Возможно, было время, когда вам предлагали сделку, которая казалась решением всех проблем с ржавчиной вашего автомобиля. За один простой платеж, будь то дилеру или третьему лицу, ваш автомобиль может быть защищен на долгие годы, а может быть, и на всю жизнь автомобиля. Звучит хорошо, не так ли? Для многих это так, и они пошли вперед с этим. Что это? Это катодная защита (CP), или более известная как электронная защита от ржавчины, и мы здесь, чтобы сообщить вам, что она не работает с вашим автомобилем.
За один простой платеж, будь то дилеру или третьему лицу, ваш автомобиль может быть защищен на долгие годы, а может быть, и на всю жизнь автомобиля. Звучит хорошо, не так ли? Для многих это так, и они пошли вперед с этим. Что это? Это катодная защита (CP), или более известная как электронная защита от ржавчины, и мы здесь, чтобы сообщить вам, что она не работает с вашим автомобилем.
Он работает по простой идее, а именно: если электроны продолжают течь через металл, не возникает ржавчины. Благодаря этому непрерывному отрицательному заряду (обеспечиваемому устройством, установленным в автомобиле) ржавчина не сможет образоваться. Этот процесс работает и может широко использоваться для защиты мостов и кораблей от ржавчины. Это преподносится как доказательство того, что процесс работает и что он может работать и с вашим автомобилем.
Почему катодная защита не работает Эти устройства зависят от замыкания цепи. Для мостов влажная почва замыкает цепь. Для кораблей соленая вода замыкает цепь. Воздух вокруг вашего автомобиля не замыкает цепь для вашего автомобиля. Если вы постоянно не ездите по воде или не паркуете свой автомобиль в почве (или в соленой воде), вы не можете завершить круг, и поэтому CP бесполезен, когда речь идет о защите вашего автомобиля.
Для мостов влажная почва замыкает цепь. Для кораблей соленая вода замыкает цепь. Воздух вокруг вашего автомобиля не замыкает цепь для вашего автомобиля. Если вы постоянно не ездите по воде или не паркуете свой автомобиль в почве (или в соленой воде), вы не можете завершить круг, и поэтому CP бесполезен, когда речь идет о защите вашего автомобиля.
использует коробку, которая устанавливается на автомобиль, соединенную с металлом с помощью анодов. Он получает заряд от аккумулятора вашего автомобиля. Эти устройства обычно стоят до 150 долларов, хотя в Интернете их можно найти намного дешевле, и, конечно, дилеры, как правило, в некоторых случаях завышают цену до 600%. Очевидно, что это огромные затраты, но предполагается, что это единовременный платеж, который решит проблему на десятилетие. Вам не нужно будет платить деньги и каждый год тратить время на то, чтобы наносить и повторно наносить средства защиты от ржавчины, как утверждает Krown. Звучит неплохо, и многие люди подхватили их.
Когда дилер продает катодную защиту, он обычно продает ее вместе с новым автомобилем, и у него есть целевая аудитория (вы). В этот момент покупатель уже потратил тысячи долларов, так что же такое еще одна тысяча в этот момент, верно? Когда клиент возражает и говорит, что его интересует другой продукт для защиты от ржавчины, такой как Krown, вместо этого он говорит им, что Krown аннулирует гарантию на их новый автомобиль. Мы подробно упоминали об этом несколько недель назад, не поддавайтесь на это!
Ржавчины не бывает, когда металл влажный или когда металл сухой. Это происходит там, где встречаются влажный и сухой металл. Это происходит во всех маленьких закоулках автомобиля, о которых вы, вероятно, даже не подозреваете и куда точно не можете добраться. В этом превосходство Krown, и именно поэтому необходимо сверление отверстий в кузове автомобиля.
Krown может выглядеть неряшливо, но благодаря тому, что он может добраться до каждого уголка и закоулка автомобиля, он защищен еще больше. Отверстия, просверленные с помощью специального сверла, небольшие и заполняются после завершения. После завершения ваш автомобиль защищен от ржавчины на следующий год!
Отверстия, просверленные с помощью специального сверла, небольшие и заполняются после завершения. После завершения ваш автомобиль защищен от ржавчины на следующий год!
Электронная защита от ржавчины может звучать хорошо. Это может звучать слишком хорошо, чтобы быть правдой. Конечно, есть люди, которые будут клясться этим, но в конце концов это не сработает. Если вам предложили электронную защиту от ржавчины, изучите ее самостоятельно, прежде чем приступать к ней. Если продавец говорит, что это разовое предложение, он просто пытается получить ваши деньги, создавая ощущение срочности. Они не хотят, чтобы вы проводили какие-либо исследования, потому что если вы это сделаете, то обнаружите, что потребители чаще предпочитают такие услуги, как Krown, чем нет.
Следует также знать, что многие варианты электронной защиты от ржавчины были запрещены в некоторых частях США в Канаде, поскольку они не работают. Если вы ищете превосходную защиту от ржавчины, обратите внимание на Krown!
О компаниях LINE-X и Krown из Южно-Центральной Пенсильвании LINE-X и Krown из Южно-Центральной Пенсильвании являются лидерами в области защиты автомобильных покрытий с использованием продуктов Krown и покрытий для грузовых автомобилей с использованием напыляемых покрытий LINE-X. Мы обслуживаем округ Йорк, помогая обслуживать и продлевать срок службы автомобилей. Если вы находитесь в Ганновере или Халламе, Якобусе или Джефферсоне, Стюартстауне или Шайло, или в любом другом месте между ними, остановитесь в нашем офисе на Фогельсонг-роуд, чтобы узнать, что мы можем сделать для защиты вашего автомобиля. Никто не разбирается в защите лучше, чем LINE-X, а также в превосходной производительности и исключительной ценности, которые она обеспечивает.
Мы обслуживаем округ Йорк, помогая обслуживать и продлевать срок службы автомобилей. Если вы находитесь в Ганновере или Халламе, Якобусе или Джефферсоне, Стюартстауне или Шайло, или в любом другом месте между ними, остановитесь в нашем офисе на Фогельсонг-роуд, чтобы узнать, что мы можем сделать для защиты вашего автомобиля. Никто не разбирается в защите лучше, чем LINE-X, а также в превосходной производительности и исключительной ценности, которые она обеспечивает.
Система защиты автомобилей от ржавчины
Где мир собирается длягальванопокрытий, анодирования и отделки Вопросы и ответы с 1989 г.
——
2003
Уважаемые господа,
Я инженер-химик и докторант в области КП. Между тем, как новичок, я думал о том, чтобы приложить руку к «электронной системе защиты от ржавчины» в качестве дилера, но я не смог ответить на вопрос (ы), действительно ли эта система защитит автомобили, как это было обещано. Я хочу, чтобы кто-нибудь помочь ответить мне, я буду рад.
— Афины, Аттика, Греция
2003
Если это похоже на электронные системы защиты от ржавчины для лодок, я не понимаю, как это может работать, поскольку автомобиль не погружается в воду или какой-либо другой ионный путь, а это одна из необходимых частей системы гальванической коррозии. или система гальванической защиты.
Но часто появляются новые изобретения, которые кажутся невозможным волшебством, пока они не объяснены, и здесь может быть именно так. Как это должно работать?
Тед Муни, ЧПСтремление жить Алоха
Finishing.com — Пайн-Бич, Нью-Джерси
2003
В продаже имеется множество систем защиты от ржавчины. Те, которые работают, обрабатывая металлический предмет, который нужно защитить от окисления, как катод в цепи электролиза постоянного тока, имеют ограниченную эффективность. Как заявил г-н Муни, основным недостатком является необходимость электролитического раствора между катодом и анодом для замыкания последовательной цепи. Даже при размещении нескольких анодов вокруг транспортного средства мало гарантий того, что будет присутствовать необходимый ионный путь для замыкания электрической цепи, необходимой для предотвращения коррозии.
Даже при размещении нескольких анодов вокруг транспортного средства мало гарантий того, что будет присутствовать необходимый ионный путь для замыкания электрической цепи, необходимой для предотвращения коррозии.
Существует система катодной защиты, основанная на емкостной связи, которая отлично подходит для транспортных средств, устраняя упомянутые выше недостатки. В основном положительная пластина, несущая импульсное постоянное напряжение, размещается рядом с диэлектрическим материалом, который размещается рядом с кузовом автомобиля. Положительная пластина и кузов автомобиля имеют общую землю. Во время каждого импульса на положительной пластине возникает положительный заряд, а на соседнем кузове автомобиля возникает соответствующий отрицательный заряд, который действует на отрицательную пластину в емкостной связи. По окончании каждого импульсного цикла избыточные электроны на отрицательной пластине отталкиваются и создают импульсный ток в кузове автомобиля. Эти избыточные электроны удаляются и становятся доступными в местах коррозии, чтобы уменьшить количество химических веществ на поверхности автомобиля, которые в противном случае могли бы вызвать окисление стали.
Автомобильная краска действует как диэлектрическое покрытие и становится потенциально емкостной поверхностью. Когда водный раствор контактирует с поверхностью краски, образуется емкостная поверхность. Кузов автомобиля является отрицательной пластиной, краска является диэлектрическим материалом, а водный раствор действует как положительная пластина. Если электролит вступает в контакт с какой-либо открытой частью кузова автомобиля (например, с царапиной на краске) и создает окислительную среду, химическое вещество в электролите, которое обычно удаляет электроны из стали, с большей вероятностью будет уменьшено избытком. электроны, накачиваемые емкостной связью. Что делает этот процесс настолько эффективным, так это то, что не требуется ионного пути между местом коррозии и анодом (соединяющим положительную пластину конденсатора). Полная окислительно-восстановительная реакция происходит между катодным корпусом автомобиля и анодным электролитом, действующим как отрицательная и положительная пластины конденсатора соответственно.
— Чатсуорт, Калифорния
«Справочник по катодной защите от коррозии»
от
Книги Эйба
или Amazon
[аффил ссылки]
Привет Майкл. Это было удивительно подробное объяснение. Я знаю, что я впечатлен. Не могли бы вы рассказать нам о своем прошлом и о том, как вы узнали так много о продукте? Это сделало бы ваше объяснение более полезным.
В благодарность,
Дэвид С. Хантер— Торонто, Онтарио, Канада
2007
Как называется упомянутый вами продукт для предотвращения ржавчины и где его можно купить?
Дин Шелви— Морден, МБ, Канада
этот текст заменяется на bannerText (Здесь нет «мертвых тем»! Если эта страница в настоящее время не находится на горячей линии, ваши вопросы, ответы или комментарии будут восстановлены ит)
Вопрос, ответ или комментарий в ЭТОЙ теме -или- Начать НОВУЮ тему
Отказ от ответственности: На этих страницах невозможно полностью диагностировать проблему отделки или опасность операции.
